Clear Sky Science · de
Transkriptomischer Signatur-geführter Abbau intermediärer alveolärer Epithelzellen verbessert die Lungenfibrose bei Mäusen
Warum vernarbte Lungen wichtig sind
Lungenfibrose ist eine schwere Lungenerkrankung, bei der empfindliche Lungenbläschen allmählich in starres Narbengewebe umgewandelt werden, sodass jeder Atemzug zur Anstrengung wird. Ärztinnen und Ärzte wissen, dass diese Vernarbung beginnt, wenn normale Reparaturprozesse aus dem Ruder laufen; welche spezifischen Zellen dafür verantwortlich sind und wie man sie entfernt, ohne gesundes Lungengewebe zu schädigen, war jedoch unklar. Diese Studie untersucht einen neuen Weg, die molekularen Signale in Lungenzellen „zu lesen“, diese Informationen zu nutzen, um schädliche Übergangszellen zu identifizieren, und sie selektiv zu eliminieren, um die Vernarbung bei Mäusen zu verringern.
Zellen, die bei fehlgeschlagener Reparatur ertappt wurden
Nach einer Lungenschädigung vermehren sich normalerweise spezialisierte, surfactantproduzierende Typ‑II‑Zellen und reifen dann zu dünnen Typ‑I‑Zellen heran, die die Lungenbläschen auskleiden und den Sauerstoffaustausch ermöglichen. Bei Fibrose bleiben viele dieser Zellen in einem Zwischen‑ oder Übergangszustand stecken, anstatt diese Umwandlung abzuschließen. Frühere Einzelzell‑RNA‑Sequenzierungsstudien hatten diese intermediären Zellen sowohl in Mäusen als auch in Menschen gefunden, doch es war nicht klar, ob sie bloße Zuschauer oder treibende Kräfte der Krankheit sind. Die Autoren konzentrierten sich auf einen Maus‑Übergangszellentyp namens Krt8+ alveoläre Differenzierungsintermediäre und auf die menschlichen Gegenstücke, die als aberrante basaloide Zellen bekannt sind und in vernarbten Lungen in großer Zahl vorkommen.
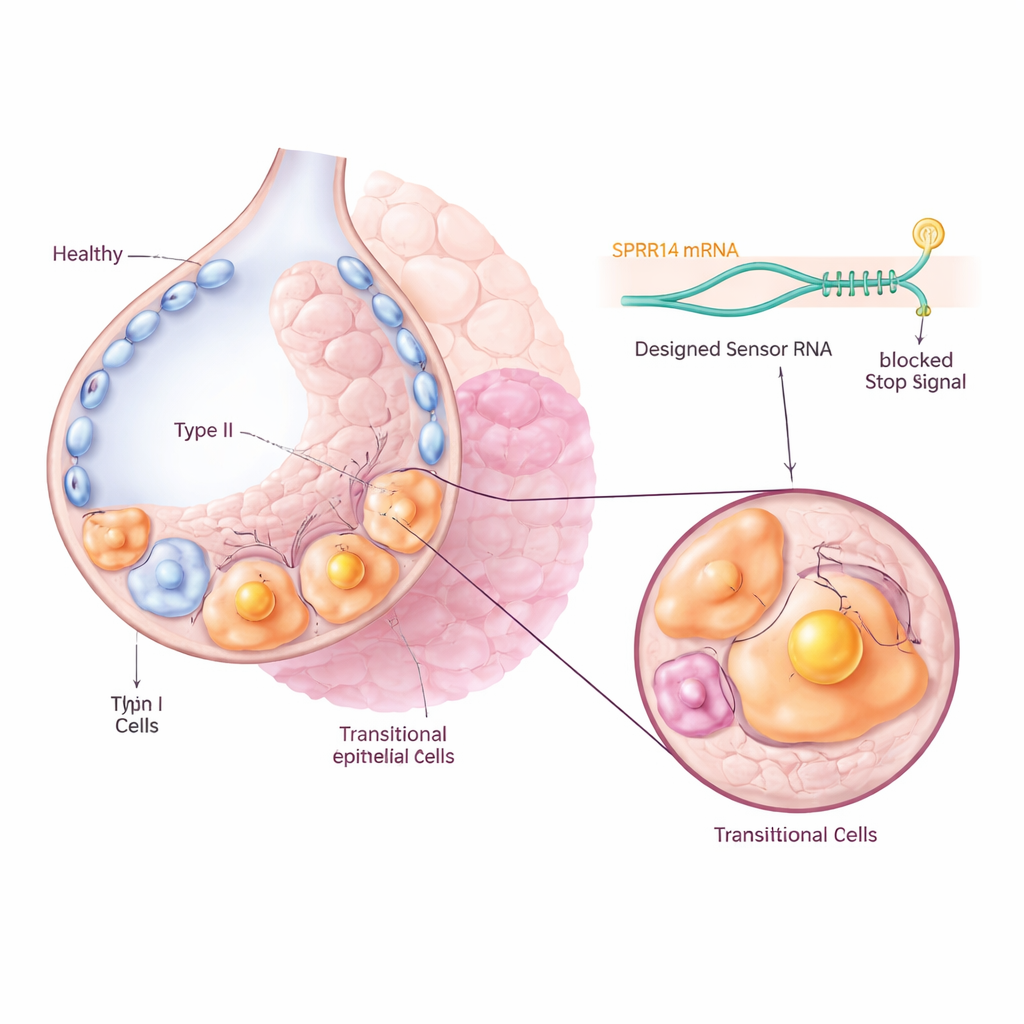
Ein einzigartiges molekulares Namensschild finden
Um diese problematischen Zellen zu erfassen, ohne ihre gesunden Nachbarn zu berühren, suchte das Team zunächst in großen Genexpressionsdatenbeständen nach einem Marker, der in der Übergangs‑Population stark und spezifisch aktiviert ist. Sie identifizierten ein Molekül namens SPRR1A als auffälliges „Namensschild“: Es war stark angereichert in Krt8+ Intermediärzellen in fibrotischen Lungen von Mäusen und in KRT5‑/KRT17+ aberranten basaloiden Zellen von Patientinnen und Patienten mit idiopathischer Lungenfibrose, aber weitgehend in normalen Lungenzellen fehlend. Mikroskopische Untersuchungen von Maus‑ und menschlichem Lungengewebe bestätigten, dass SPRR1A vor allem in verletzten, umgebauten Bereichen und nicht in gesunden Lungenbläschen auftrat, was darauf hindeutet, dass es als präziser Griff zur Identifizierung der schuldigen Zellen dienen könnte.
Zellen mit einem RNA‑Sensor programmieren
Die Forschenden nutzten dann eine kürzlich entwickelte Technologie namens CellREADR, die wie ein internes molekulares Sensorgerät funktioniert. Sie entwarfen kurze RNA‑Sequenzen, die mit SPRR1A‑RNA in einer Zelle Basenpaare bilden können. Wenn der Sensor SPRR1A erkennt, löst er die Produktion eines angehängten „Effektor“-Proteins aus, etwa eines fluoreszenten Tags oder eines Rezeptors, der die Zelle für ein Medikament empfindlich macht. Bei Mäusen wurden Viren eingesetzt, um diese Sensor‑Effektor‑Konstrukte in Lungenzellen zu bringen. Nur Zellen, die aktiv SPRR1A produzierten, schalteten das fluoreszente Signal ein, sodass das Team Übergangszellen direkt aus fibrotischen Lungen verfolgen und isolieren konnte. Einzelzellsequenzierung zeigte, dass die markierten Zellen dem bekannten Übergangs‑Genexpressionsprofil sehr nahe kamen, was bestätigte, dass der RNA‑Sensor genau die beabsichtigte Population ansprach.
Schädliche Intermediäre ausschalten
Als Nächstes wurde der Effektor von einem harmlosen fluoreszenten Protein auf den Diphtherie-Toxin-Rezeptor umgestellt, sodass SPRR1A‑positive Zellen durch Verabreichung von Diphtherie‑Toxin selektiv getötet werden konnten. Durch das Timing der Behandlung auf den Zeitpunkt der höchsten Häufigkeit der Übergangszellen nach chemischer Lungenschädigung konnten die Autoren etwa ein Drittel dieser Population entfernen. Diese gezielte Depletion führte zu deutlich weniger Lungenvernarbung: es gab weniger Kollagenablagerung, niedrigere Spiegel fibrotischer Proteine und normaler aussehende Lungenbläschenstrukturen. Detaillierte Analysen zeigten, dass die meisten SPRR1A‑positiven Zellen Anzeichen eines gestressten, alternsähnlichen Zustands trugen, während eine kleine Untergruppe zu hoher Proliferation fähig war, was darauf hindeutet, dass diese Intermediäre sowohl die Gewebereparatur misslingen lassen als auch den fibrotischen Prozess aufrechterhalten.
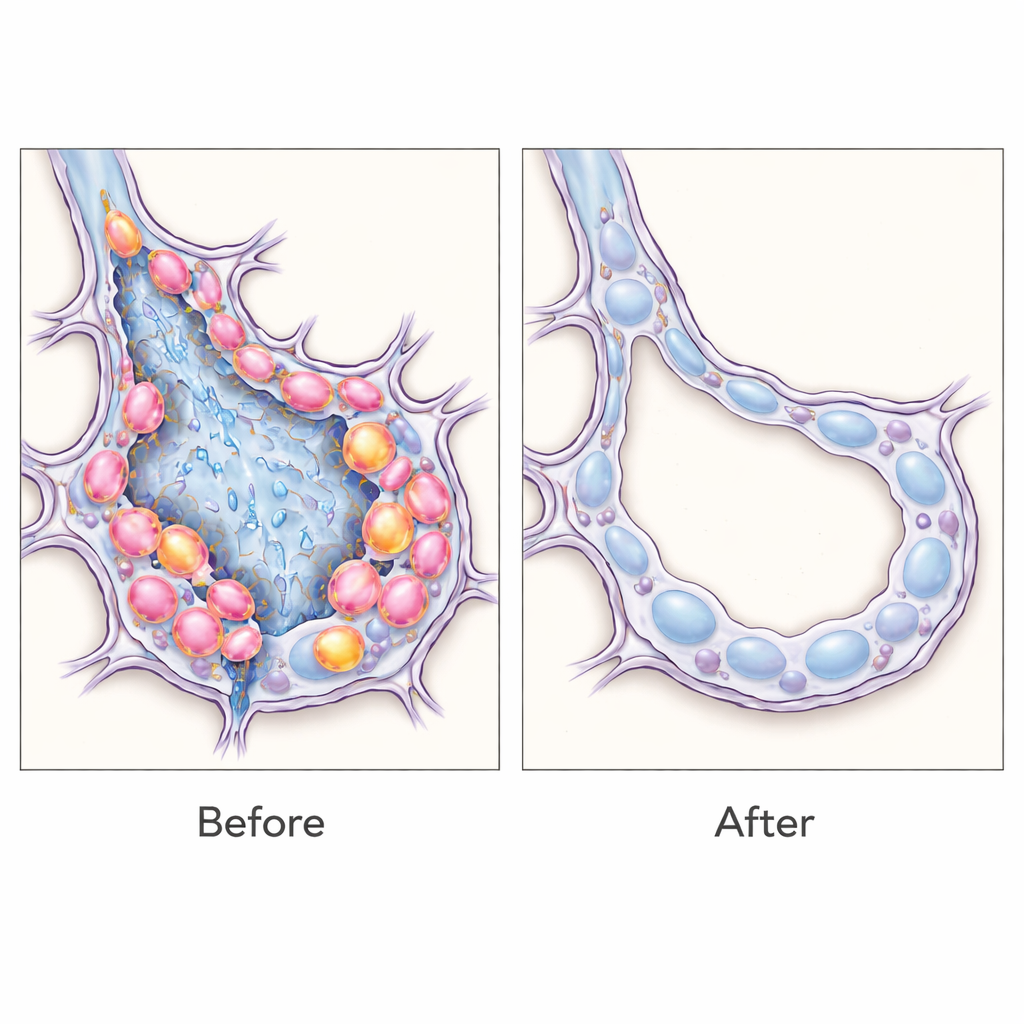
Was das für künftige Behandlungen bedeutet
Diese Befunde sprechen dafür, dass Übergangs‑Epithelzellen nicht nur Marker, sondern aktive Treiber der Lungenfibrose sind und dass ihre selektive Entfernung das Gleichgewicht bei Mäusen wieder zugunsten einer gesünderen Lungenarchitektur verschieben kann. Allgemeiner zeigt die Arbeit eine flexible Strategie: Indem man zellspezifische RNA‑Signaturen „liest“, können Forschende eng definierte Zellpopulationen in lebendem Gewebe markieren, untersuchen und sogar eliminieren, ohne dafür jedes Mal spezielle Tierlinien erzeugen zu müssen. Zwar bleibt noch viel zu tun, bevor solche RNA‑sensitive Werkzeuge sicher beim Menschen angewendet werden könnten, doch dieser Ansatz eröffnet einen Weg zu präzisen Therapien, die genau die Zelltypen anvisieren, die die Heilung bei chronischer Lungenvernarbung und möglicherweise anderen fibrotischen Erkrankungen entgleisen lassen.
Zitation: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Schlüsselwörter: Lungenfibrose, alveoläre Epithelzellen, Einzelzell-RNA-Sequenzierung, RNA-Sensortechnologie, zelluläre Seneszenz