Clear Sky Science · de
Ein Einzelkern-Atlas der zentralen Amygdala zeigt Chromatin- und Gen-Transkriptionsdynamik beim alkoholbedingten Gebrauchsstörung
Warum diese Forschung für den Alltag wichtig ist
Alkoholgebrauchsstörung (AUD) betrifft Millionen von Menschen und ihre Familien, doch wir wissen überraschend wenig darüber, was langjähriger starker Alkoholkonsum auf Ebene einzelner Zellen im menschlichen Gehirn bewirkt. Diese Studie fokussiert eine kleine, aber zentrale Region — die zentrale Amygdala, ein Knotenpunkt für Angst, Stress und Motivation — und kartiert, wie Alkohol Gehirnzellen und ihre genetischen Kontrollsysteme umgestaltet. Durch die Kombination modernster "Single-Cell"-Sequenzierung mit genetischen Studien zum Suchtrisiko beginnen die Autoren zu erklären, warum manche Menschen anfälliger für AUD sind und wie Alkohol bleibende molekulare Spuren im Gehirn hinterlassen kann.
Genauer Blick auf einen winzigen Gehirnknoten
Die zentrale Amygdala ist eine wichtige Ausgangsstation im emotionalen und stressbezogenen Netzwerk des Gehirns und steht in starkem Zusammenhang mit Angstreduktion, Verlangen und zwanghaftem Alkoholkonsum. In dieser Arbeit analysierten Forschende etwa 175.000 einzelne Zellkerne aus der zentralen Amygdala von 50 postmortalen Spendern — 22 mit einer Vorgeschichte von Alkoholgebrauchsstörung und 28 ohne AUD. Mithilfe einer Technik, die in derselben Zelle sowohl Genaktivität (RNA) als auch Chromatinzugänglichkeit (wie "offen" oder "geschlossen" DNA ist) liest, erstellten sie einen detaillierten Atlas aller wichtigen Zelltypen in dieser Region, einschließlich verschiedener Neuronenarten und Stützzellen wie Astrozyten und Mikroglia. Sie fanden heraus, dass inhibitorische Neuronen — die Gehirnaktivität dämpfen oder formen — besonders zahlreich in der zentralen Amygdala sind und bei Menschen mit AUD offenbar besonders betroffen sind. 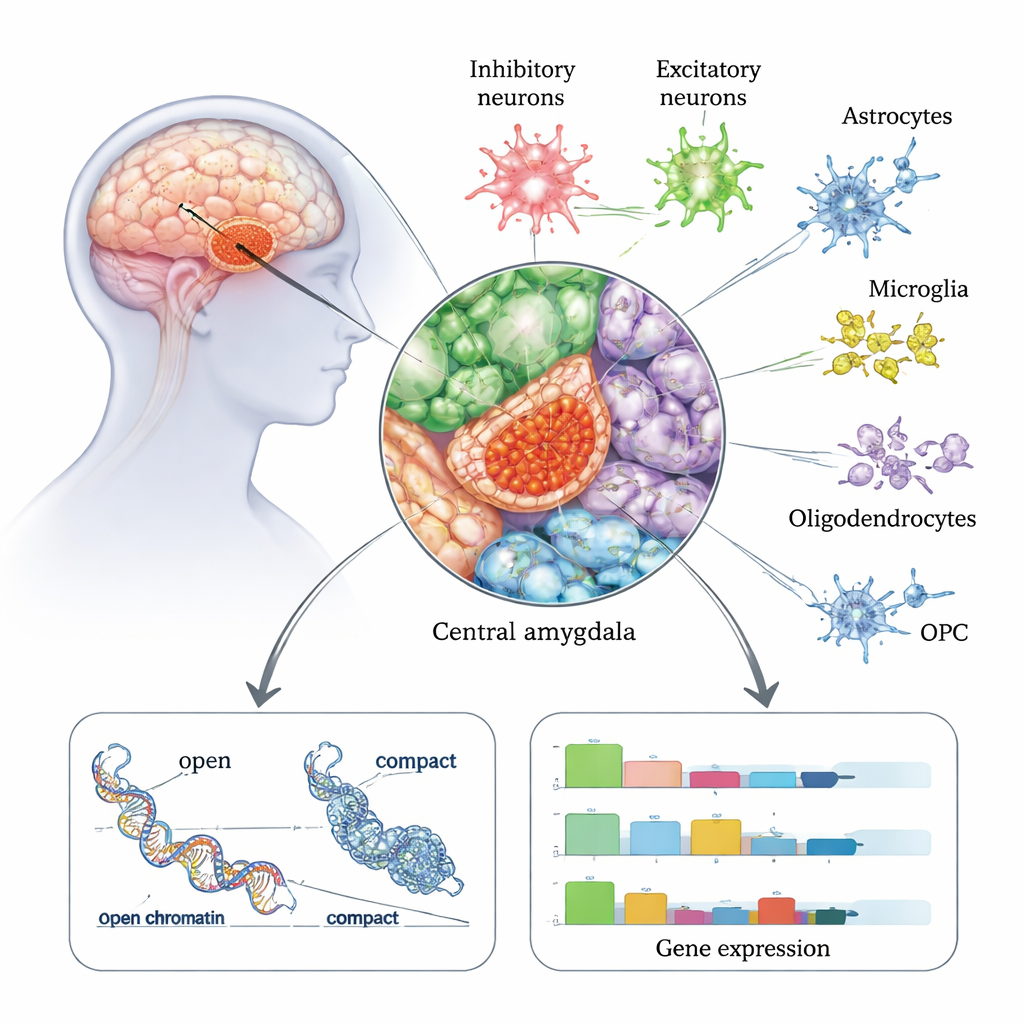
Welche Zellen und Gene verändern sich bei Alkoholgebrauchsstörung?
Das Team verglich systematisch die Genaktivität von Menschen mit und ohne AUD, Zelltyp für Zelltyp. Sie entdeckten mehr als 1.800 Gene, deren Aktivität in spezifischen Zellpopulationen verändert war, wobei die größten Verschiebungen in inhibitorischen Neuronen auftraten, gefolgt von exzitatorischen Neuronen und Astrozyten. Ein Subtyp inhibitorischer Neuronen, gekennzeichnet durch das Peptid Proenkephalin (PENK), zeigte besonders starke Veränderungen. Viele der betroffenen Gene sind an der Kommunikation zwischen Nervenzellen beteiligt, insbesondere am Gleichgewicht zwischen dem exzitatorischen Signal Glutamat und dem inhibitorischen Signal GABA. So war beispielsweise das Gen GABRA2, das beim Aufbau eines wichtigen Typs von GABA-Rezeptoren hilft, in bestimmten inhibitorischen Neuronen erhöht, während GRM8, ein Glutamatrezeptor, und NCAM1, ein für Synapsen wichtiges Zelladhäsionsmolekül, sich in unterschiedlichen Neuronentypen entgegengesetzt veränderten. Diese Muster deuten darauf hin, dass die Feinabstimmung von Erregung und Hemmung in der zentralen Amygdala bei AUD gestört ist.
Die Kontrollschalter des Gehirns: Chromatin und regulatorische Elemente
Gene wirken nicht allein; sie werden von DNA-Abschnitten gesteuert, die wie Schalter oder Dimmregler funktionieren. Durch die Betrachtung des Chromatins — der Art, wie DNA verpackt ist — identifizierten die Forschenden mehr als eine halbe Million potenzieller regulatorischer Elemente und verknüpften sie in zelltypspezifischer Weise mit benachbarten Genen. Fast die Hälfte dieser Elemente war einzigartig für einen einzelnen Zelltyp, was die Spezialisierung verschiedener Gehirnzellen unterstreicht. Viele regulatorische Elemente, die bei AUD verändert waren, standen in Verbindung mit Genen, die am Kalziumhaushalt und an Glutamatsignalen beteiligt sind, wie etwa CALN1, ein kalziumbindendes Gen, das in Neuronen stark aktiv ist. In inhibitorischen Neuronen zeigte CALN1 sowohl erhöhte Expression als auch dichte Cluster regulatorischer Schleifen, was nahelegt, dass Alkoholexposition die lokale DNA-Architektur dieses Gens umgestaltet. 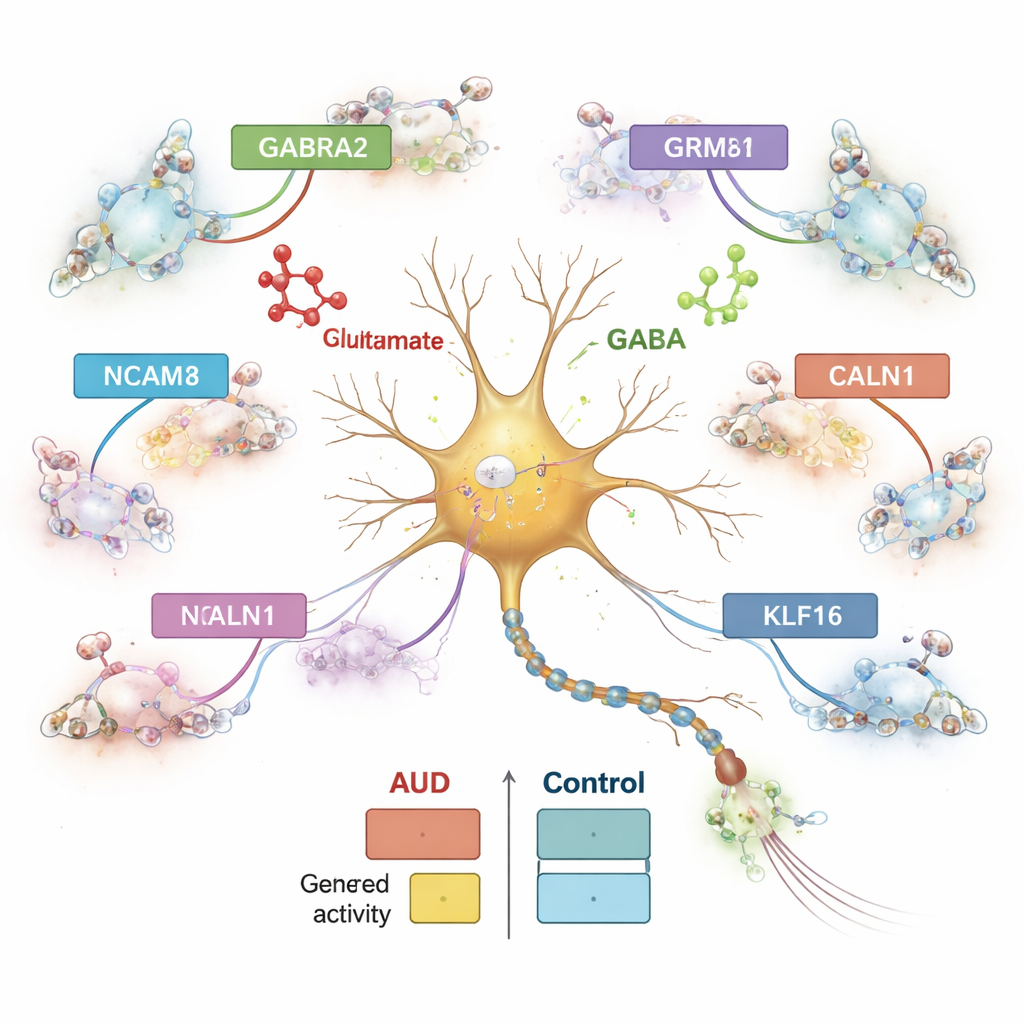
Von Risikogenen zu tatsächlichen Gehirnveränderungen
Genetische Studien haben viele DNA-Varianten identifiziert, die das Risiko für Alkoholprobleme erhöhen, doch wo und wie sie im Gehirn wirken, war lange unklar. Durch das Überlagern ihrer Einzelzell-Karten mit großen genomweiten Assoziationsstudien zum problematischen Alkoholkonsum fanden die Autoren heraus, dass Risikogene überproportional in Neuronen der zentralen Amygdala aktiv und dysreguliert sind, besonders in inhibitorischen Neuronen. Sie lokaliserten über 200 wahrscheinliche kausale Risikovarianten, die sich in regulatorischen Elementen befinden, die in spezifischen Zelltypen offen sind. Einige lagen in oder nahe bei Genen, die bereits mit Sucht in Verbindung gebracht wurden, wie CACNA1C und DRD2, die an der Kontrolle neuronaler Erregbarkeit und der Dopamin-Signalgebung beteiligt sind. Andere, darunter SEMA6D und NF1, tauchten als neue Kandidaten auf. Das Team identifizierte außerdem eine Familie von Transkriptionsfaktoren, die Kruppel-like-Faktoren genannt werden (insbesondere KLF16), die offenbar weitreichende Veränderungen in kalzium- und glutamatbezogenen Genen koordinieren, und bestätigte Teile dieses Regulationsnetzwerks in einem Mausmodell akuter Alkoholexposition.
Was das für das Verständnis und die Behandlung von AUD bedeutet
Einfach ausgedrückt zeigt diese Studie, dass Alkoholgebrauchsstörung nicht nur ein diffus verteiltes Gehirnproblem ist, sondern eine hochgradig organisierte Störung, die sich auf bestimmte Zelltypen und molekulare Pfade innerhalb eines kritischen emotionalen Knotenpunkts konzentriert. Inhibitorische Neuronen der zentralen Amygdala sowie Astrozyten und andere Stützzellen weisen koordinierte Veränderungen in der Genaktivität und in den DNA-Schaltern auf, die diese Gene steuern — insbesondere in Systemen, die Glutamat-, GABA- und Kalziumsignale regeln. Durch die Verbindung dieser zellulären Veränderungen mit genetischen Risikovarianten bietet die Arbeit eine Landkarte, die ererbte Verwundbarkeit mit konkreten molekularen Ereignissen im Gehirn verknüpft. Im Laufe der Zeit könnten solche zellspezifischen Karten die Entwicklung präziserer Therapien leiten, die das Gleichgewicht von Erregung und Hemmung wiederherstellen, statt breit auf das gesamte Gehirn einzuwirken.
Zitation: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Schlüsselwörter: Alkoholgebrauchsstörung, zentrale Amygdala, Einzelzell-Genomik, inhibitorische Neuronen, Genregulation