Clear Sky Science · de
Molekulare Heterogenität der Cochlea von nicht-menschlichen Primaten
Warum die verborgene Welt des Innenohrs wichtig ist
Hören wirkt mühelos, beruht aber auf einer erstaunlich komplexen Maschine, die tief im Schädel verborgen liegt: der Cochlea des Innenohrs. Versagt diese empfindliche Struktur, führt das häufig zu dauerhaftem Hörverlust. Vieles, was wir über Cochleas wissen, stammt aus Mausstudien, doch Behandlungen müssen letztlich beim Menschen funktionieren. Diese Studie öffnet ein seltenes Fenster in die Cochlea eines nicht-menschlichen Primaten, des Makaken, dessen Hörsystem unserer viel näher steht. Durch das Katalogisieren von Zehntausenden einzelner Zellen zeigen die Forschenden, wie die Primaten-Cochlea aufgebaut ist, wie sie dem Mausohr ähnelt und wo sie sich entscheidend unterscheidet – insbesondere bei Zelltypen, die mit erblichen Taubheiten und künftigen Gentherapien verknüpft sind.
Jede Zelle in einer winzigen Spirale kartieren
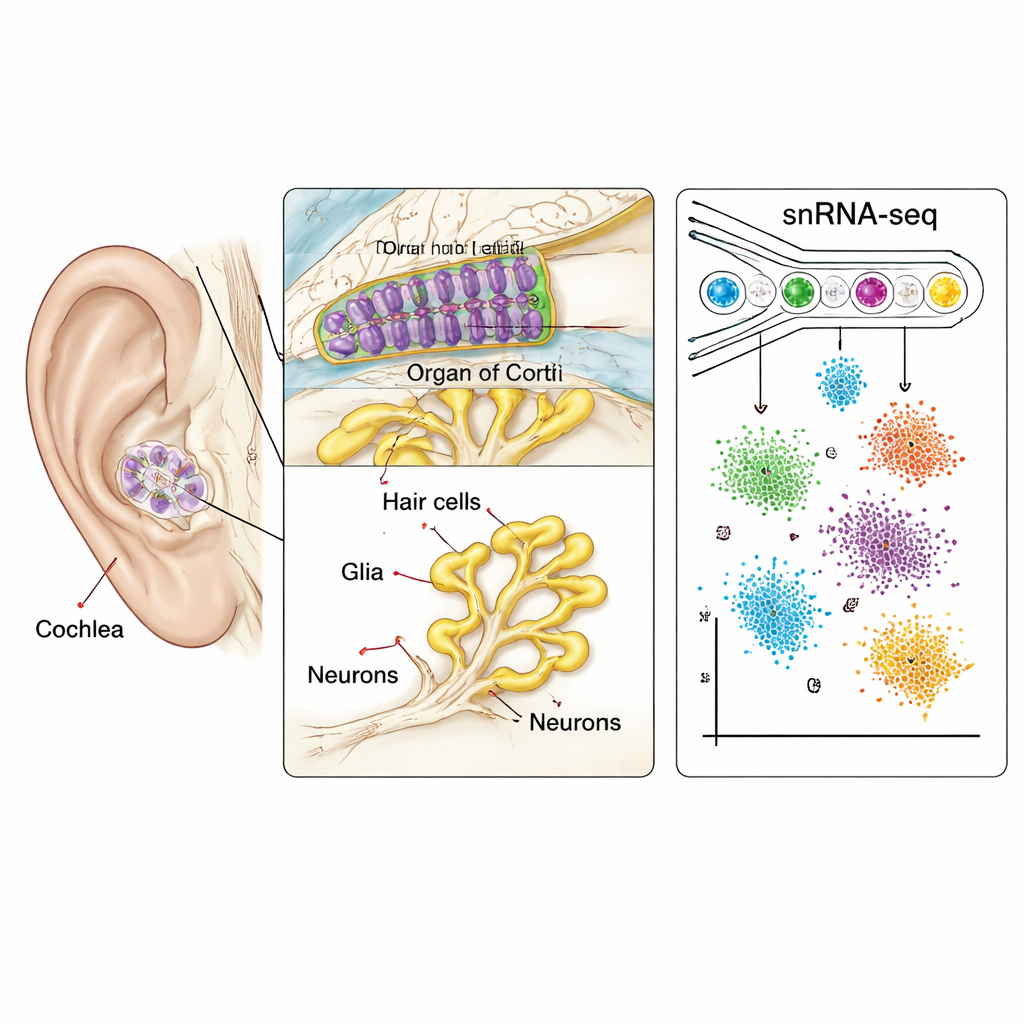
Die Cochlea ist eine mit Flüssigkeit gefüllte Spirale, die Schallvibrationen in elektrische Signale umwandelt. In ihr liegt ein Gewebestreifen, das Organon Corti, das mit sensorischen Haarzellen, Stützzellen und Neuronen ausgekleidet ist, die Informationen zum Gehirn leiten. Weil diese Zellen selten, fragil und von Knochen umgeben sind, waren sie bei Primaten sehr schwer zu untersuchen. Hier nutzten die Wissenschaftler Single-Nucleus-RNA-Sequencing, eine Hochdurchsatzmethode, die abliest, welche Gene in einzelnen Zellkernen aktiv sind. An Cochleas juvenilem und adultem Makakenmaterial profilierten sie mehr als 36.000 Kerne aus nahezu allen wichtigen Regionen: dem sensiblen Epithel, dem Nervenknoten namens Spiralganglion und dem umliegenden Gewebe, das Flüssigkeit und Blutversorgung reguliert.
Ein konservierter Bauplan fürs Hören
Jeder Kern wurde basierend auf seiner Genaktivität zu Zelltypen gruppiert und so ein „Zellatlas“ der Makaken-Cochlea erstellt. Beim Vergleich dieses Atlasses mit ähnlichen Mausdaten erschien der grundsätzliche Bauplan überraschend vertraut. Die sensorischen Haarzellen, die Schall detektieren, und die Spiralganglionneurone, die Signale an das Gehirn senden, zeigten stark konservierte molekulare Signaturen. Schlüssengene, die innere Haarzellen (die Informationen senden) von äußeren Haarzellen (die Schall verstärken) unterscheiden, zeigten in beiden Arten ähnliche Aktivitätsmuster. Selbst spezialisierte Motorproteine wie Prestin, das äußeren Haarzellen erlaubt, sich elektrisch bedingt in der Länge zu verändern, waren bei Makaken wie bei Mäusen vorhanden und funktionell. Das deutet darauf hin, dass die Kernmaschinerie des Hörens über die Säugetier-Evolution hinweg weitgehend erhalten geblieben ist.
Glia und Neurone zeigen primatenspezifische Abweichungen
Unterhalb dieses gemeinsamen Bauplans entdeckte die Studie jedoch wichtige primatenspezifische Besonderheiten. Insbesondere waren Gliazellen – Stützzellen, die Neurone umhüllen, nähren und mit ihnen kommunizieren – auf molekularer Ebene bei Makaken deutlich vielfältiger als bei Mäusen. Obwohl ihre Form und Lage im Mikroskop ähnlich erschienen, divergierten ihre Genexpressionsmuster, vor allem bei Genen, die an Ionenhaushalt, Abfallbeseitigung und chemischer Signalübertragung beteiligt sind. Auch Spiralganglionneurone zeigten feingliedrige Diversität. Das Team identifizierte Subtypen dieser sensorischen Neurone und fand, dass einige Marker-Gene, die in Mäusen zur Definition von Neuronenklassen dienen, bei Makaken nicht sauber übereinstimmten. Ein Transkriptionsfaktor, PBX3, trat als bei Primaten angereicherter Regulator in bestimmten Neuronensubtypen hervor und deutet auf evolutionäre Feinabstimmungen hin, wie primatenspezifische Ohren Schall codieren.
Eine genetische Landkarte für Hörverlust
Um diesen Atlas mit menschlichen Erkrankungen zu verknüpfen, überlagerten die Forschenden Hunderte bekannter Taubheitsgene – entnommen aus klinischen Genetikdatenbanken – mit ihrer Makaken-Zellkarte. Viele dieser Gene erwiesen sich als scharf auf bestimmte Zelltypen beschränkt, etwa Haarzellen, Stützzellen oder Lateralwandzellen, die helfen, die Innenspannung des Ohrs zu erzeugen. Andere konzentrierten sich in Glia oder Neuronen. Die Gesamtverteilung spiegelte weitgehend das Bild aus Mäusen wider und bestärkt, dass Makaken ein relevantes Modell für das menschliche Hören darstellen. Indem der Atlas aufführt, wo jedes Taubheitsgen normalerweise aktiv ist, liefert er eine Art „Krankheitskarte“, die gezielte Gentherapien und Strategien für die Wirkstoffabgabe leiten kann, insbesondere wenn solche Behandlungen von Mausmodellen in größere Tiere überführt werden.
Was das für künftige Hörtherapien bedeutet
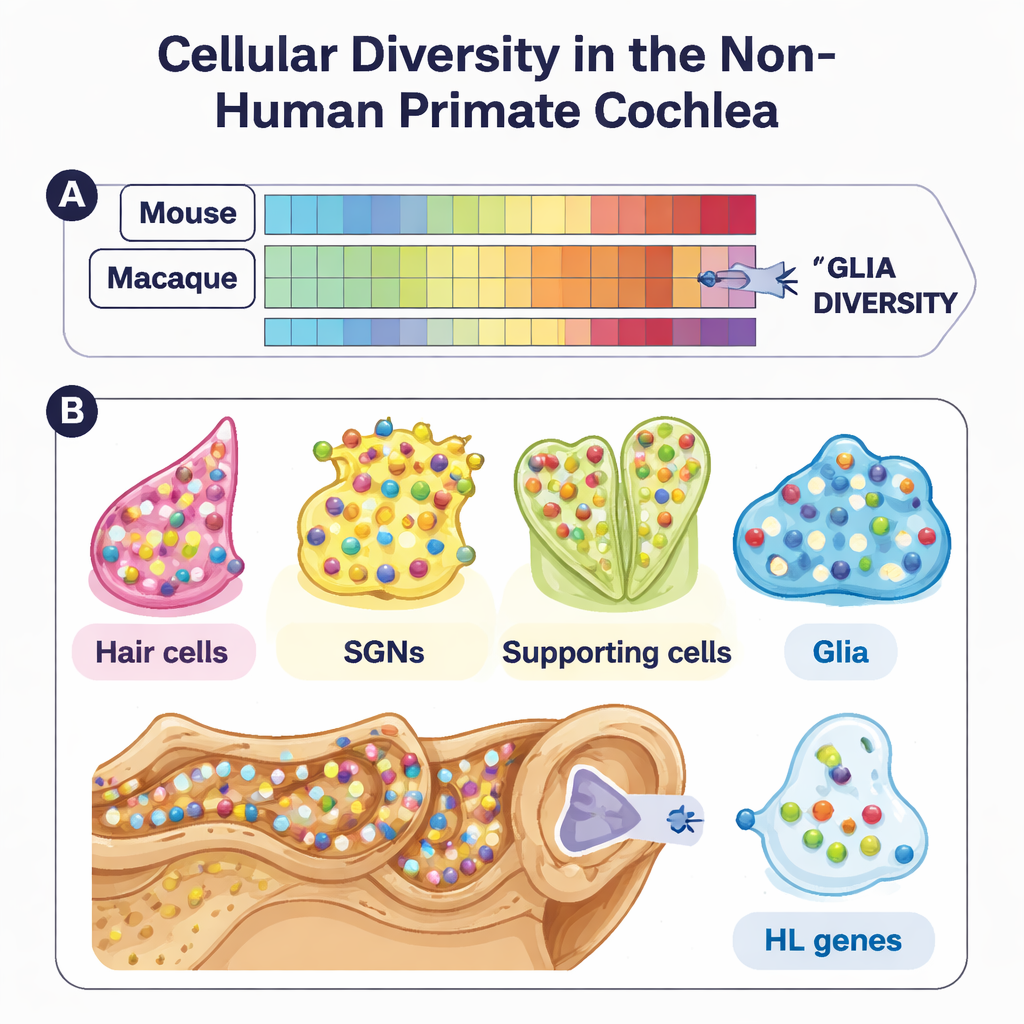
Für Nicht-Spezialisten ist die Kernbotschaft: Wissenschaftler haben erstmals eine detaillierte Zell-für-Zell-Karte der Primaten-Cochlea erstellt und diese direkt mit dem gut untersuchten Mausohr verglichen. Die Schlussfolgerung ist zugleich beruhigend und mahnend: Die wesentliche Hörmaschinerie ist stark konserviert, was die Verwendung von Mausstudien zur Entwicklung von Therapien untermauert, doch wichtige Unterschiede – besonders in Gliazellen und bestimmten Neuronen – könnten beeinflussen, wie Therapien beim Menschen wirken. Dieser Makaken-Cochlea-Atlas dient nun als entscheidende Brücke zwischen Grundlagenforschung an Nagetieren und klinischen Fortschritten für Menschen mit Hörverlust.
Zitation: Chen, X., Che, Y., Qi, J. et al. Molecular heterogeneity of the non-human primate cochlea. Nat Commun 17, 1633 (2026). https://doi.org/10.1038/s41467-026-68350-2
Schlüsselwörter: Cochlea, Einzelzell-Atlas, Hörverlust, nicht-menschlicher Primat, Genexpression