Clear Sky Science · de
Von der Bildung von TDP-43/RNA-Komplexen zur krankheitsassoziierten TDP-43-Aggregation: ein struktureller und zellulärer Ansatz
Warum dieses Hirnprotein wichtig ist
Neurodegenerative Erkrankungen wie die amyotrophe Lateralsklerose (ALS) und die frontotemporale Demenz zeigen häufig Ablagerungen fehlgefalteter Proteine in Nervenzellen. Einer der häufigsten Täter ist das Protein TDP-43, das normalerweise bei der Verarbeitung von RNA hilft — der funktionsfähigen Kopie unserer Gene. Die vorliegende Studie stellt eine zentrale Frage: Was macht TDP-43 in gesunden Zellen, und was geht schief, sodass ein nützlicher RNA-Helfer zu einem toxischen, aggregationsfähigen Protein wird?
Wie TDP-43 in gesunden Nervenzellen arbeitet
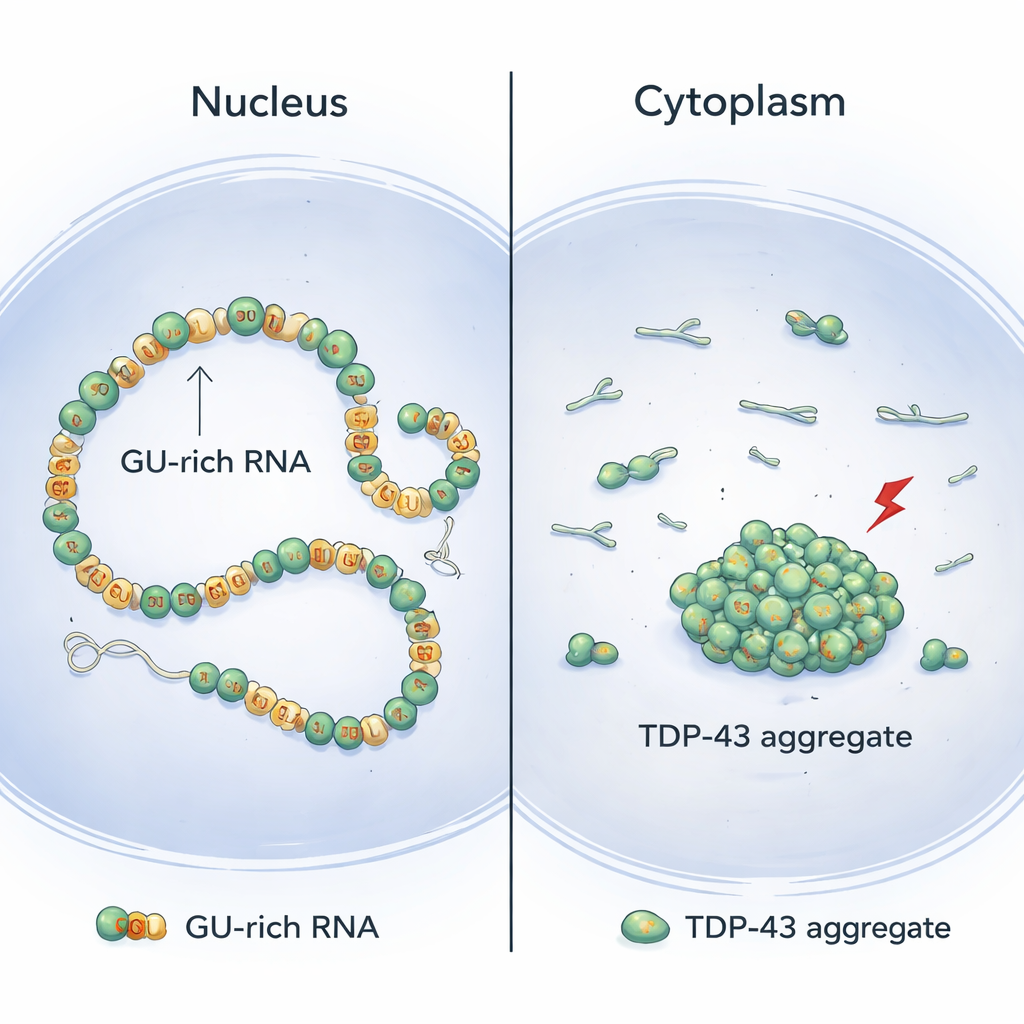
TDP-43 befindet sich meist im Zellkern, wo es lange RNA-Abschnitte bindet, die reich an wiederholten „GU“-Bausteinen sind. Mithilfe einer Kombination aus Strukturbiologie und zellulären Experimenten zeigen die Autoren, dass sich TDP-43-Moleküle kooperativ entlang dieser GU-reichen Regionen anordnen und glatte, kontinuierliche Ketten auf der RNA bilden. In dieser Anordnung bleibt das N-terminale Ende des Proteins — seine N-terminale Domäne — physisch zwischen benachbarten Molekülen getrennt. Dadurch sind diese N-terminalen Segmente verfügbar, um weit entfernte GU-reiche Abschnitte derselben RNA zu überbrücken und so lange Introns (die nicht-kodierenden Abschnitte innerhalb von Genen) sanft zu schleifen und zu kompaktieren, ohne zu verklumpen.
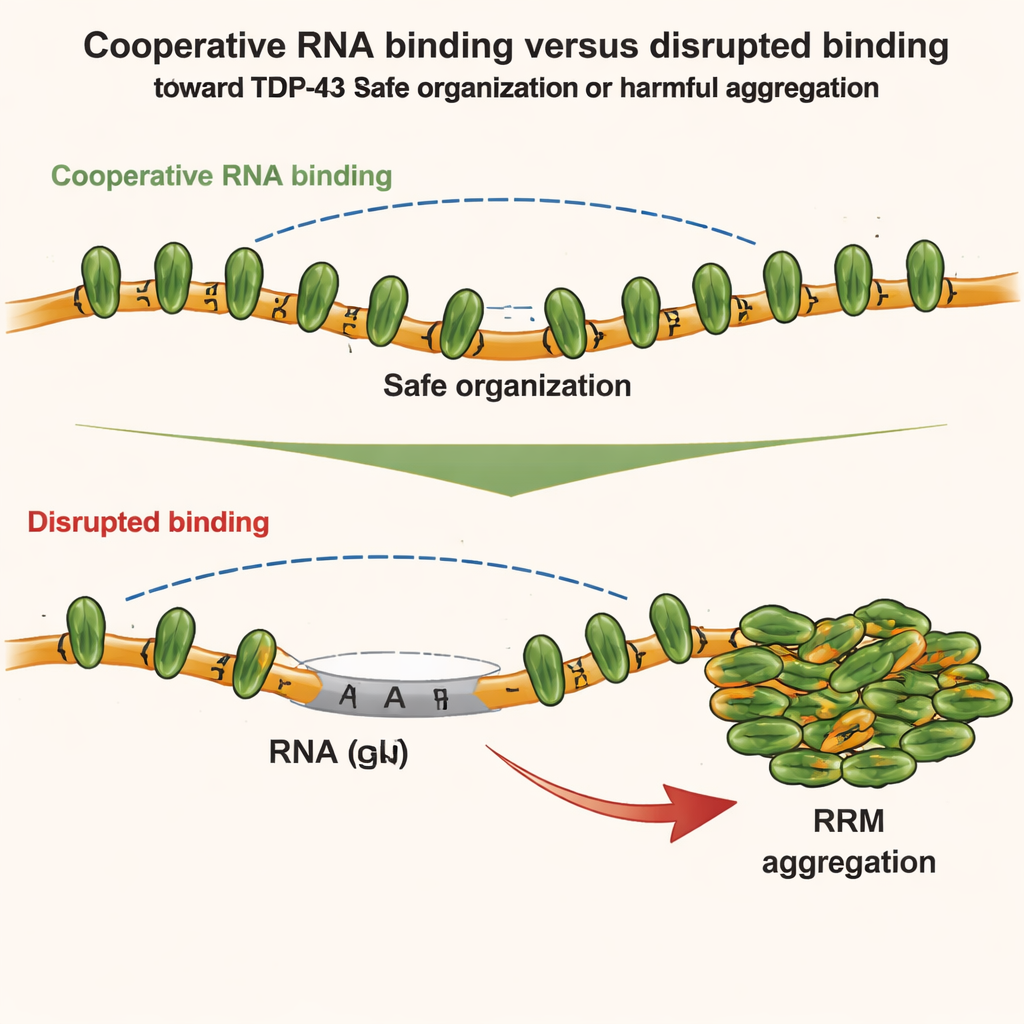
Ein eingebautes Tauziehen im Protein
Die Forscher untersuchten dann, wie verschiedene Bereiche von TDP-43 miteinander konkurrieren oder kooperieren. Sie konzentrierten sich auf zwei Regionen: die N-terminale Domäne, die an andere N-terminale Domänen binden kann, und die zentralen RNA-bindenden Module, die die kooperative Bindung entlang GU-reicher RNA antreiben. Mit empfindlichen Methoden wie NMR-Spektroskopie, Kalorimetrie und Kleinwinkel-Röntgenstreuung fanden sie heraus, dass bei kooperativer RNA-Bindung die Geometrie der Kette die direkten N-terminalen Kontakte zwischen benachbarten Molekülen tatsächlich abschwächt. Anders gesagt: Starke kooperative RNA-Bindung hält lokale N-terminale Wechselwirkungen unter Kontrolle. Wird diese Kooperativität jedoch gestört — etwa durch Einfügen nicht-GU-haltiger Abschnitte in die RNA oder durch Mutationen in TDP-43 — rücken N-terminale Bereiche benachbarter Proteine näher zusammen und können nun aneinander andocken.
Von hilfreicher Kompaktierung zu schädlicher Verklumpung
Diese strukturellen Erkenntnisse wurden in lebenden Zellen getestet. Die Autoren nutzten gentechnisch veränderte Zellmodelle, um zu verfolgen, wie sich verschiedene TDP-43-Mutanten in künstlichen RNA-reichen Kompartimenten mischen oder trennen. Sie fanden heraus, dass sowohl die kooperative RNA-Bindung als auch N-terminale Wechselwirkungen dabei helfen, TDP-43 in höher geordnete Assemblies zu organisieren, aber auf unterschiedliche Weise. Kooperative Bindung reiht Proteine entlang GU-reicher RNA auf, während N-terminale Kontakte entfernte Cluster miteinander verbinden. Unter leichter oxidativer Belastung verschiebt sich das Gleichgewicht jedoch. Ein chemischer Stressor (Arsenit) verursacht spezifische chemische Modifikationen — Acetylierung — an den zentralen RNA-bindenden Motiven, wodurch diese zur gegenseitigen Anlagerung neigen. Wenn die kooperative Bindung an RNA intakt ist, bleibt TDP-43 größtenteils löslich. Ist die Kooperativität geschwächt, wirken N-terminale Verknüpfungen zwischen benachbarten TDP-43-Molekülen wie ein Gerüst, das die acetylierten Kerne zusammenführt und irreversible Aggregation fördert.
Warum TDP-43 sich im Zytoplasma stärker verklumpt
Das aus dieser Arbeit entwickelte Modell hilft zu erklären, warum TDP-43-Aggregate bei erkrankten Neuronen häufiger im Zytoplasma als im Zellkern zu finden sind. Im Kern sind lange Introns mit vielen GU-Wiederholungen verbreitet, was kontinuierliche, kooperative Bindung begünstigt, die riskante N-terminale Kontakte zwischen Nachbarn reduziert und stattdessen sichere Langstrecken-Schleifen ermöglicht. Im Zytoplasma hingegen haben reife RNAs deutlich weniger GU-reiche Abschnitte. Das führt zu einer patchigeren und weniger kooperativen TDP-43-Bindung, erhöht die Wahrscheinlichkeit, dass benachbarte N-terminale Domänen interagieren, und bereitet so den Boden für Aggregation, sobald stressinduzierte chemische Veränderungen eintreten. Diese Sicht wird durch Experimente gestützt, in denen eine künstliche Zufuhr zusätzlicher GU-reicher Introns im Zellkern die TDP-43-Aggregation unter Stress verringerte.
Was das für zukünftige Therapien bedeutet
Kurz gesagt zeichnet die Studie TDP-43 als ein Protein, das zwischen nützlicher RNA-Organisation und schädlicher Verklumpung balanciert, wobei die kooperative Bindung an GU-reiche RNA als Sicherheitsmechanismus fungiert. Versagt dieses Sicherheitsnetz — wegen veränderter RNA-Sequenzen, Proteinmutationen oder zellulärem Stress — können dieselben Domänen, die normalerweise lange RNA-Segmente kompaktieren, stattdessen die Bildung toxischer Aggregate antreiben. Für Nichtfachleute ist die zentrale Erkenntnis, dass die Aufrechterhaltung der richtigen Art von Wechselwirkungen zwischen TDP-43 und RNA eine vielversprechende Strategie sein könnte, um die Proteinverklumpung bei ALS und verwandten Hirnerkrankungen zu verhindern oder zu verlangsamen.
Zitation: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Schlüsselwörter: TDP-43-Aggregation, RNA-bindende Proteine, ALS, Protein–RNA-Interaktionen, Neurodegeneration