Clear Sky Science · de
Atomgenaue Ligandenmodifikation von Goldnanopartikeln durch Interphasen-Massentransfer
Warum winzige Goldpartikel für die Gesundheit wichtig sind
Die medizinische Bildgebung nutzt zunehmend Nanopartikel — winzige Teilchen, die tausende Male kleiner sind als ein menschliches Haar — um Organe und Tumore tief im Körper sichtbar zu machen. Diese Studie zeigt, wie Forschende nun die äußere Hülle ultrasmaller Goldpartikel nahezu atomgenau feinabstimmen können, sodass derselbe leuchtende Kern gezielt zu unterschiedlichen Organen gelenkt werden kann, insbesondere von Leber und Milz hin zu den Nieren. Solche Kontrolle könnte helfen, sicherere Bildgebungsagentien und Wirkstoffträger zu entwerfen, die genau dorthin gelangen, wo Ärzte sie benötigen, und den Körper sauberer wieder verlassen.
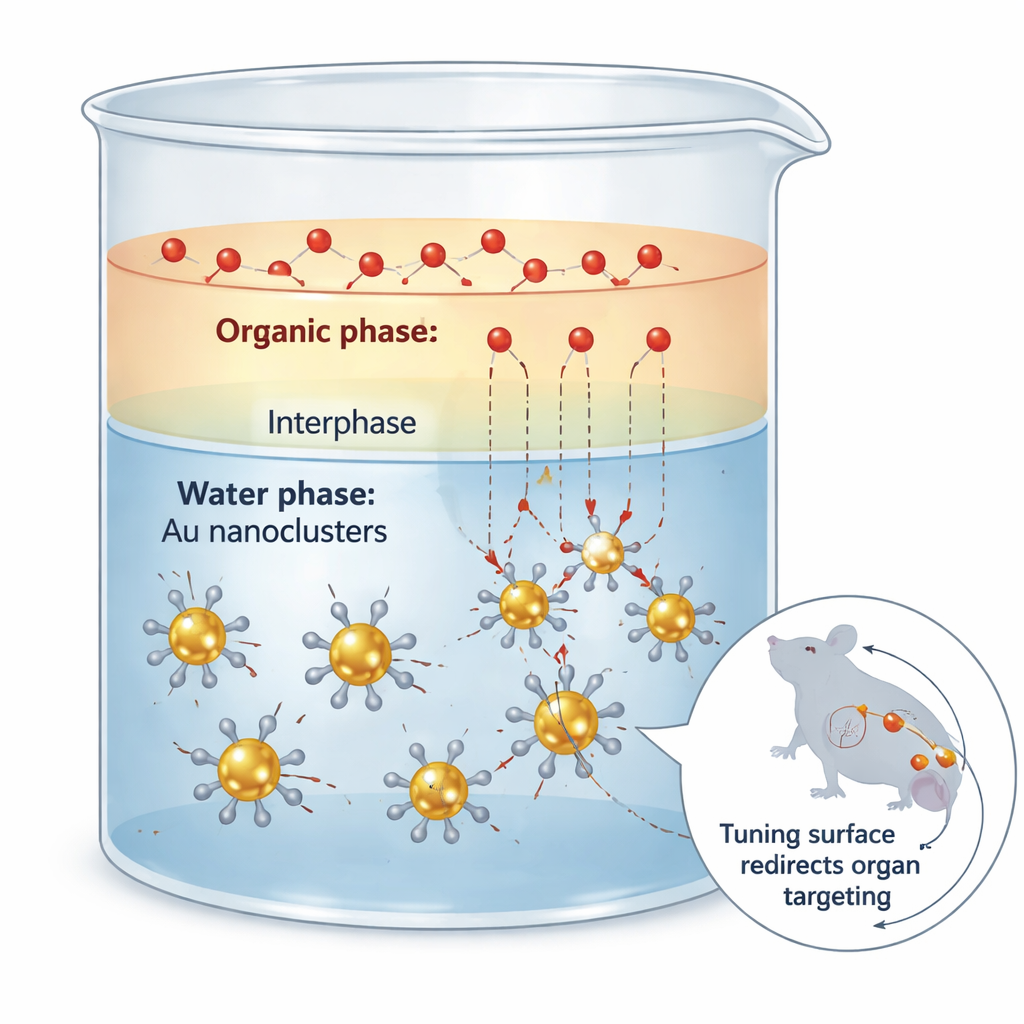
Die Herausforderung, winzige Goldcluster umzukleiden
Goldnanocluster sind ultrasmalles Gold, das sich eher wie große Moleküle als wie metallische Körner verhält. Sie können im nahen Infrarot-II-Bereich Licht emittieren, das tief ins Gewebe eindringt und scharfe Bilder mit geringem Hintergrund liefert. Fast alles daran, wie diese Cluster sich im Körper verhalten — wohin sie wandern, wie lange sie zirkulieren und wie sie eliminiert werden — hängt jedoch nicht vom Goldkern, sondern von den organischen Liganden oder der „Hülle“ ab, die an ihrer Oberfläche sitzen. Traditionelle Methoden, diese Hülle zu verändern, wirken oft wie grobe Chirurgie: Die Reaktion verläuft zu schnell, die Beschichtung wird ungleichmäßig, und der Goldkern kann teilweise angegriffen werden, wodurch Struktur und optische Eigenschaften zerstört werden.
Den Verkehr zwischen zwei Flüssigkeiten verlangsamen
Die Forschenden gingen dieses Problem mit einer einfachen physikalischen Idee an: dem Widerstand des Massentransfers an der Grenze zwischen zwei Flüssigkeiten, die sich nicht vollständig mischen. Sie platzierten die Goldcluster in Wasser und die eintretenden schwefelhaltigen Liganden in einem organischen Lösungsmittel wie Ethylacetat. In der dünnen Zone, in der sich die beiden Flüssigkeiten teilweise vermischen, diffundieren die Liganden langsam zu den Clustern und tauschen sich mit der ursprünglichen Hülle aus. Sorgfältige kinetische Messungen zeigten, dass das unerwünschte „Ätzen“ des Goldkerns extrem empfindlich auf die Ligandkonzentration reagiert, während der gewünschte Austausch deutlich weniger sensitiv ist. Durch den Zwei-Phasen-Aufbau, der freie Liganden niedrig, aber kontinuierlich nachliefert, unterdrückte das Team das Ätzen um etwa das Sechzigfache, während die nützliche Austauschrate größtenteils erhalten blieb.
Ein präzises molekulares Werkzeugset aufbauen
Mit dieser interphasenunterstützten Methode konnten die Autorinnen und Autoren die Oberflächenliganden eines Modell-Goldclusters, Au25, sehr kontrolliert austauschen. Sie begannen mit Clustern, die durch einen negativ geladenen Sulfonsäure-Liganden geschützt waren, und ersetzten diesen schrittweise durch verschiedene neue Thiol-Liganden mit Carbonsäuren, Aminen, Hydroxylgruppen, Nitrogruppen und hydrophoben aromatischen Ringen. Massenspektrometrie zeigte saubere, klar definierte Mischungen wie Au25-Cluster mit bestimmten Anzahlen jedes Ligandtyps, statt breiten, unübersichtlichen Verteilungen. Die Methode funktionierte außerdem für andere Clustergrößen und Ligandenfamilien, was darauf hindeutet, dass es sich um eine allgemeine Strategie handelt, robuste, maßgeschneiderte Goldnanocluster für verschiedene Anwendungen zu erzeugen.
Nanopartikel von der Leber zu den Nieren lenken
Der eindrücklichste Test dieser Präzision stammte aus In-vivo-Bildgebungsexperimenten an Mäusen. Indem sie schrittweise einen positiv geladenen Liganden, p-Aminothiophenol, in die ansonsten negativ geladene Hülle einführten, erzeugte das Team eine Serie von Clustern, deren gesamte Oberflächenladung sich von stark negativ zu nahezu zwitterionisch (ausgeglichenen positiven und negativen Gruppen) verschob. Alle Varianten leuchteten im Laborversuch ähnlich, doch ihre Biodistribution in Mäusen unterschied sich dramatisch. Rein negative Cluster akkumulierten hauptsächlich in Leber und Milz. Mit zunehmendem Anteil positiver Liganden nahm das Signal in diesen Organen ab und stieg in Nieren und Blase an, was auf eine verstärkte renale Ausscheidung hinweist. Wurde statt des Amins ein neutrales Hydroxyl-Ligand verwendet, trat diese Verschiebung nicht auf, was die besondere Rolle positiver Ladungen bei der Umlenkung der Teilchen unterstreicht.
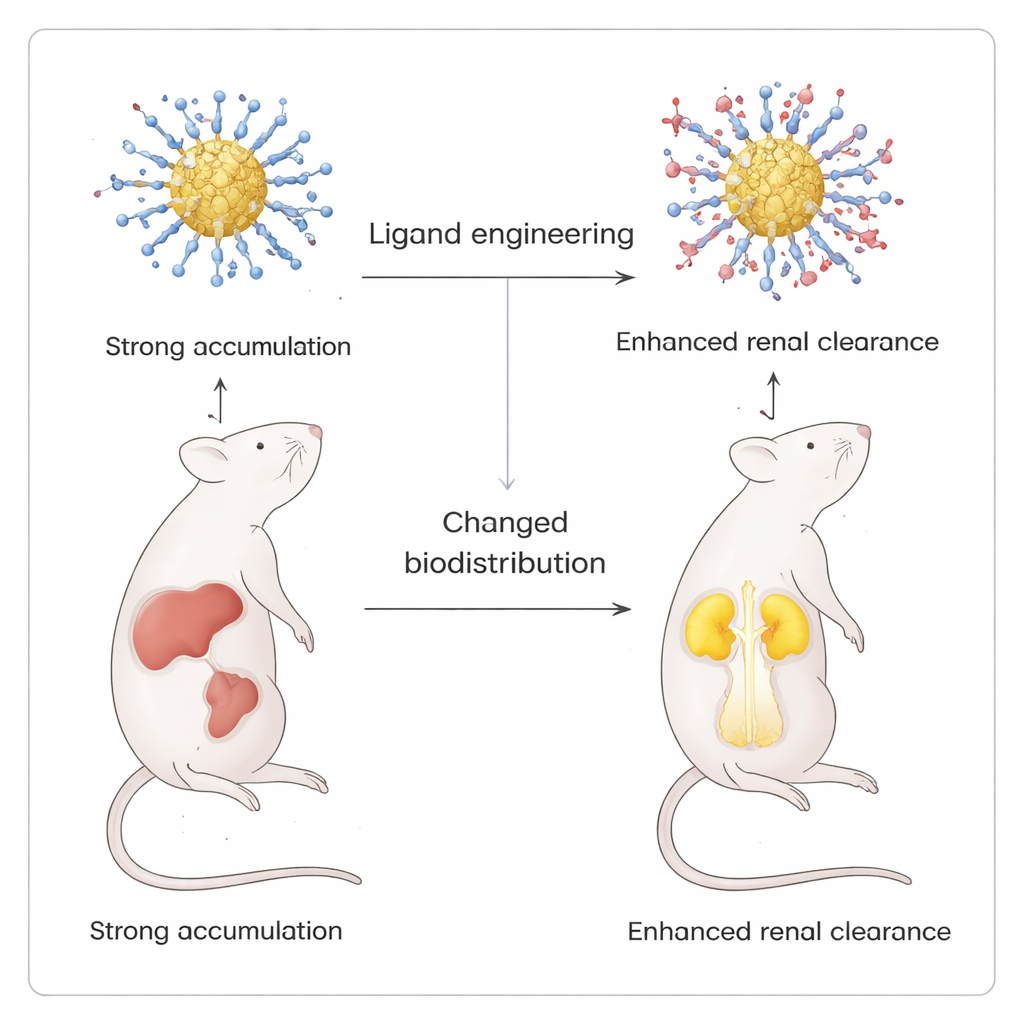
Was das für künftige Medizin bedeutet
Für Nicht‑Spezialisten ist die zentrale Erkenntnis, dass Forschende einen Weg gefunden haben, leuchtende Goldnanocluster mit molekularen Mänteln zu „bekleiden“, die sich nahezu ein Molekül nach dem anderen feinabstimmen lassen, ohne das zugrundeliegende Partikel zu beschädigen. Durch eine schonende Zwei‑Flüssigkeiten‑Anordnung können sie sowohl die Chemie als auch das Schicksal dieser Partikel im Körper kontrollieren. Dieses Maß an Steuerung ermöglicht es, Bildgebungsagentien und potenzielle Wirkstoffträger zu entwerfen, die gezielt bestimmte Organe anstrahlen und anschließend über die Nieren statt in Leber und Milz verbleiben, und ebnet so den Weg für sicherere und besser vorhersagbare Nanomedizin.
Zitation: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Schlüsselwörter: Gold-Nanocluster, Liganden-Engineering, Bioimaging, Nanotherapie, Biodistribution