Clear Sky Science · de
Die Aktivität von DOT1L begrenzt die Geschwindigkeit der Transkriptions-Elongation und begünstigt RNAPII-Pausen, um die Mutagenese durch AID zu erleichtern
Wie unsere Immunzellen riskante DNA-Edits feinabstimmen
Unser Immunsystem erzeugt hochwirksame Antikörper, indem es seine eigene DNA gezielt mutiert — eine riskante Strategie, die gelegentlich Krebs begünstigen kann. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Was steuert, wo und wie effizient diese absichtlichen Mutationen auftreten? Die Antwort fokussiert ein Protein namens DOT1L, das die Lesegeschwindigkeit von Genen in B-Zellen justiert und so hilft, die Mutationsmaschinerie an die richtigen Stellen zu lenken.
Mutation einschalten, um Antikörper zu schärfen
Wenn B-Zellen auf eine Infektion treffen, verbessern sie ihre Antikörper auf zwei Arten. Sie führen kleine Veränderungen in der Bindungsregion des Antikörpers ein, um die Bindungsstärke an Erreger zu erhöhen, und sie tauschen das Antikörper-Fc‑Fragment aus, um die Art der Immunantwort zu verändern. Beide Anpassungen beginnen mit einem Enzym namens AID, das in aktiv abgelesenen Genen die DNA einritzt und verändert. Während AID für eine effektive Immunität unverzichtbar ist, kann es auch andere Gene treffen und dort gefährliche Brüche erzeugen, die blutige Krebserkrankungen antreiben. Frühere Arbeiten zeigten, dass AID Gene bevorzugt, die stark abgelesen werden und von mächtigen DNA-Schaltern, sogenannten Super‑Enhancern, reguliert sind — das erklärt jedoch nicht vollständig, warum nur eine begrenzte Untergruppe von Genen besonders anfällig ist.
Ein Chromatinmarker, der AID-empfindliche Gene kennzeichnet
Die Autorinnen und Autoren konzentrierten sich auf Proteine, die in der Nähe von AID im Zellkern sitzen. Mithilfe einer Proximity‑Labeling‑Technik in menschlichen Zellen fanden sie, dass AID in der Nähe von DOT1L vorkommt — einem Enzym, das eine spezifische Stelle an den Histonproteinen, um die die DNA gewickelt ist, modifiziert. Diese Modifikation, ein chemisches Mark an Histon H3 an Position K79, kommt auf aktiven Genen häufig vor. In Maus‑B‑Zellen tragen die Gene, die AID häufig mutiert — einschließlich Antikörpergenen und krebssensitiven Off‑Targets — besonders hohe Level dieser DOT1L‑vermittelten Markierungen. Wenn die Forschenden DOT1L in B‑Zelllinien deaktivierten oder seine Aktivität mit einem Wirkstoff hemmten, ging das Antikörper‑«Class‑Switching» zurück, ebenso wie AID‑vermittelte DNA‑Brüche und krebsvorstufenfördernde Fusionen zwischen Antikörpergenen und dem Wachstumsgen cMyc. Wichtig war, dass die katalytische Funktion von DOT1L, nicht nur seine Anwesenheit, erforderlich war: Mutante Versionen, die das Histonmark nicht mehr setzen konnten, stellten das normale Antikörper‑Switching nicht wieder her.
Den Genleser verlangsamen, um AID Zeit zu geben
Auf den ersten Blick erscheint das paradox, weil DOT1L mit aktiven Genen assoziiert ist, doch sein Entfernen nicht einfach Gene abschaltete. Mit einer Methode, die neu entstandene RNA abbildet, entdeckte das Team, dass B‑Zellen ohne DOT1L tatsächlich an vielen DOT1L‑markierten Genen mehr naszierende Transkripte produzierten — obwohl etwas weniger des Hauptgenleseenzym Ribonukleinsäure‑Polymerase II auf diesen Genen nachweisbar war. Durch die Kombination dieser naszierenden RNA‑Messung mit Karten der Polymerase‑Belegung schlossen sie, dass unter normalen Bedingungen DOT1L‑Histonmarkierungen wie sanfte Schwellen wirken. Sie verlangsamen die Polymerase beim Entlanglaufen des Gens und verlängern kurze Pausen nahe dem Start und innerhalb des Genkörpers von DOT1L‑markierten Genen. Ohne DOT1L rast die Polymerase schneller und pausiert kürzer. Da AID kurze Zeitfenster braucht, in denen die DNA exponiert ist und die Polymerase verweilt, reduziert diese Beschleunigung paradoxerweise AIDs Fähigkeit, sich festzusetzen und zu wirken, selbst wenn die Gesamttranskription steigt.
Genaktivität vom Mutationsrisiko entkoppeln
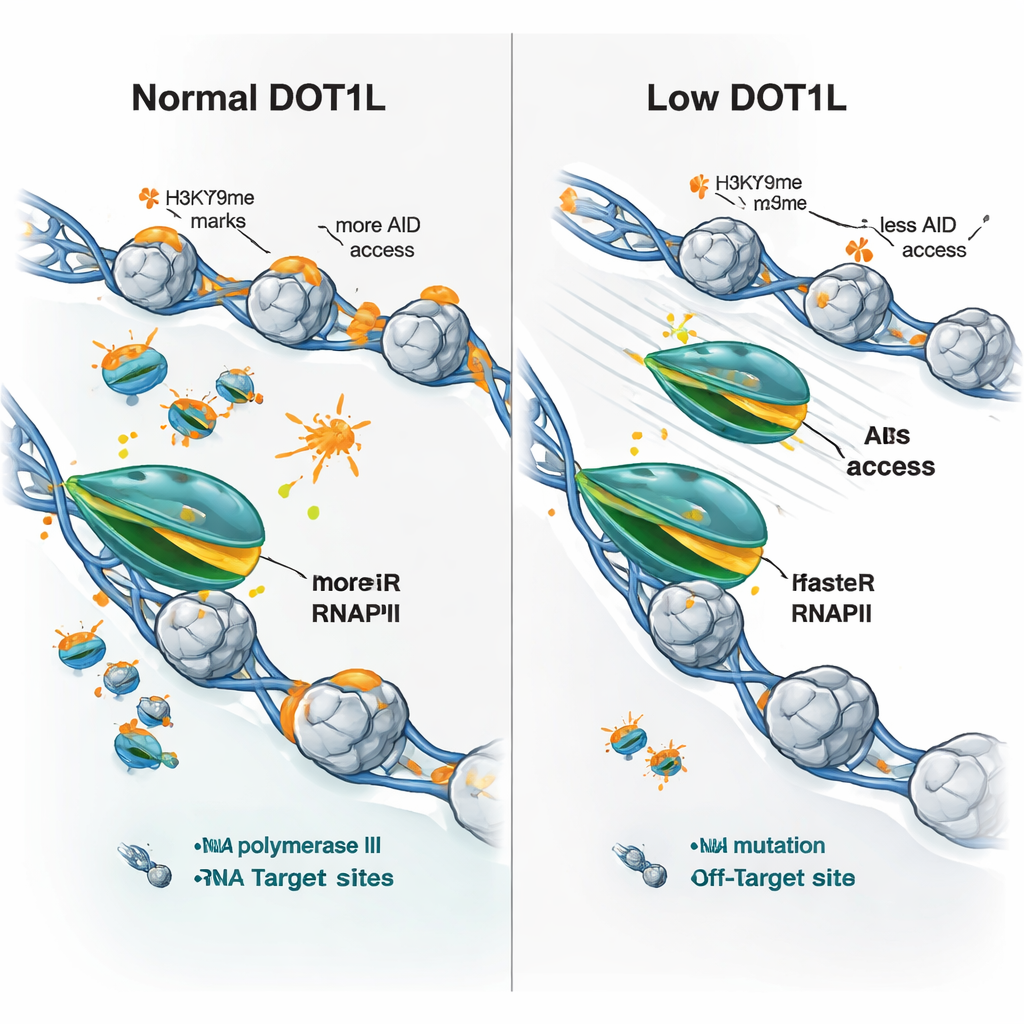
Die Forschenden fragten dann, ob diese Geschwindigkeitsänderungen das gemischte Muster der Genexpression erklären könnten, das beim Verlust von DOT1L beobachtet wird — einige Gene werden stärker, andere schwächer exprimiert. Sie fanden, dass nahezu alle DOT1L‑markierten Gene in Knockout‑Zellen ein gemeinsames Merkmal teilten: eine schnellere Elongation durch RNA‑Polymerase II. Das Ergebnis hing jedoch vom Ausgangszustand ab. Langsame, schwach exprimierte Gene produzierten tendenziell mehr RNA, wenn die Polymerase schneller lief, während hochaktive, lange Gene mit bereits schnellen Polymerasen manchmal weniger produzierten, vermutlich weil zu schnelles Durchlaufen eine effiziente Prozessierung oder Fertigstellung stört. Entscheidend ist: Sowohl an Antikörpergenen als auch an klassischen AID‑Off‑Targets führte der Verlust von DOT1L zu schnellerer Polymerase‑Bewegung, weniger Hinweisen auf Polymerase‑«Stalling» und deutlich reduzierter AID‑Belegung, selbst wenn die betreffenden Gene nicht herunterreguliert waren.
Warum das für Immunität und Krebs wichtig ist
Zusammenfassend zeichnen die Ergebnisse das Bild von DOT1L als subtilen Verkehrsregler für die Genlesemaschinerie in B‑Zellen. Durch das Anbringen spezifischer Histonmarken verlangsamt DOT1L geringfügig RNA‑Polymerase II und verlängert deren Pausen, sodass ein transkriptionelles Umfeld entsteht, in dem AID produktiv an Antikörpergenen — und bedauerlicherweise auch an einer begrenzten Auswahl anderer verwundbarer Gene — wirken kann, um Mutationen einzuführen. Fehlt DOT1L oder wird es gehemmt, rast die Polymerase hindurch und bietet AID weniger Gelegenheiten, was die Antikörperdiversifizierung abschwächt und zugleich das Risiko bestimmter schädlicher Umordnungen verringert. Diese mechanistische Einsicht erklärt, warum der Verlust von DOT1L sowohl zu Anstiegen als auch zu Abnahmen der Genexpression führen kann, und verbindet die feine Kontrolle der Transkriptionsgeschwindigkeit direkt mit den Stellen, an denen unser Immunsystem wagt, seine eigene DNA umzuschreiben.
Zitation: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Schlüsselwörter: Antikörperdiversifizierung, AID-Enzym, DOT1L, Gen-Transkription, B-Zellen