Clear Sky Science · de
Glycerol-3-phosphat-Acyltransferase verschärft α-Synuclein-induzierte Toxizität durch Erhöhung der Lipidperoxidation
Warum Fette im Gehirn für Parkinson wichtig sind
Die Parkinson-Krankheit wird meist als ein Problem mit einem Protein namens Alpha‑Synuclein beschrieben, das verklumpt und Nervenzellen, die Bewegungen steuern, schädigt. Diese Studie zeigt, dass Gehirnfette — insbesondere deren Synthese und Schäden — eine überraschend starke Rolle dabei spielen, wie toxisch Alpha‑Synuclein wird. Indem sie ein fettbildendes Enzym identifizieren, das Nervenzellschäden verschlimmert, weist die Arbeit auf einen neuen, medikamentös ansprechbaren Weg hin, der bestehende Ansätze zur Bekämpfung von Parkinson ergänzen könnte.
Ein Protein, das bei Parkinson fehlverhält
Menschen mit Parkinson verlieren nach und nach Dopamin-produzierende Nervenzellen in einer tiefen Hirnregion, die die Bewegung koordiniert. In diesen sterbenden Zellen finden Forscher häufig dichte Ablagerungen, sogenannte Lewy-Körper, die mit dem Protein Alpha‑Synuclein gefüllt sind. In seltenen Familien verursachen Mutationen oder zusätzliche Kopien des Alpha‑Synuclein-Gens direkt Parkinson, während häufige genetische Varianten in diesem Gen das Risiko nur moderat erhöhen. Das deutet darauf hin, dass andere Gene und Signalwege beeinflussen, wie schädlich Alpha‑Synuclein wird. Zunehmend sprechen Hinweise dafür, dass Lipide — Fette und fettähnliche Moleküle, die Zellmembranen und Energiespeicher bilden — entscheidende Partner sowohl bei der Verklumpung von Alpha‑Synuclein als auch beim Untergang von Nervenzellen sind.
Ein mächtiges Lipid‑Enzym in Fruchtfliegen-Modellen finden
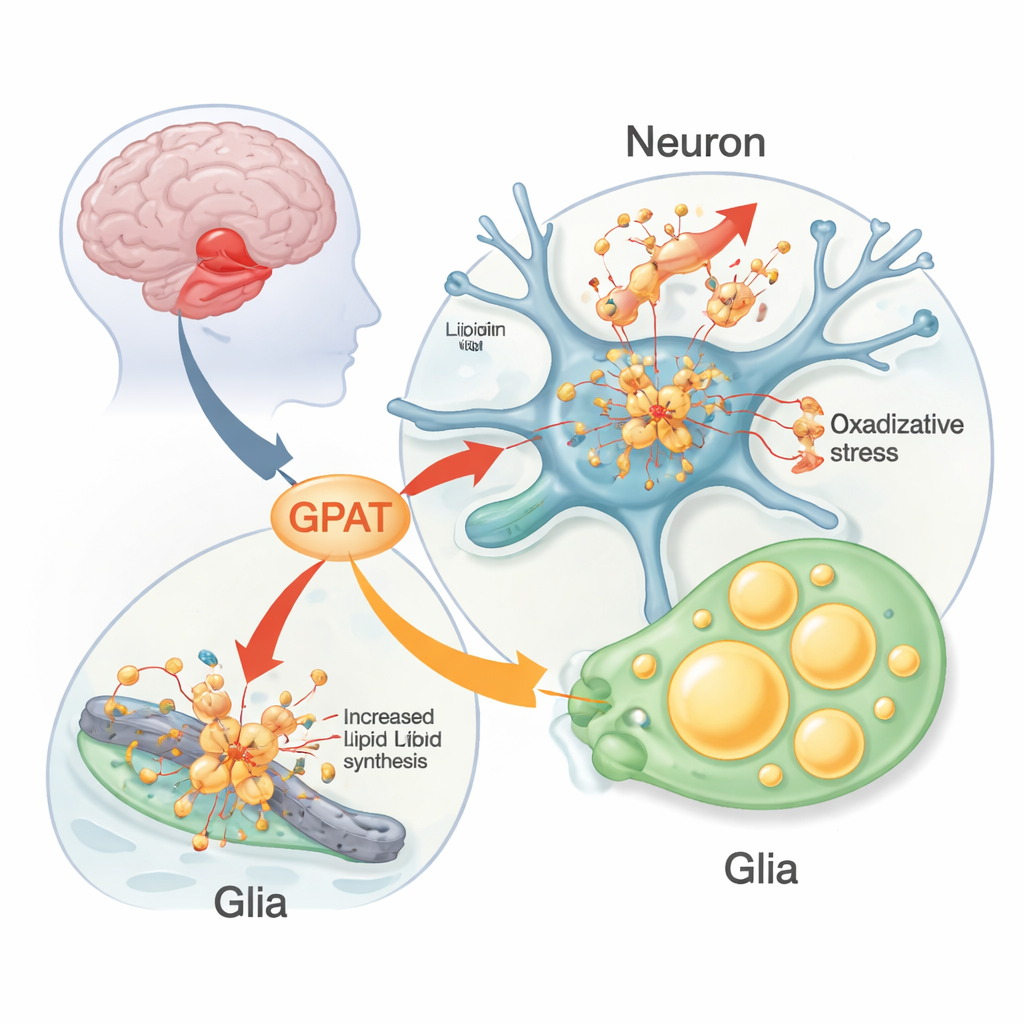
Die Forscher verwendeten Fruchtfliegen, die so gentechnisch verändert wurden, dass sie menschliches Alpha‑Synuclein in ihrem Nervensystem produzieren, als lebendigen Versuchsmaßstab. Diese Fliegen entwickeln Parkinson-ähnliche Probleme: Verlust dopaminproduzierender Neurone, Kletterstörungen und gestörte Tagesrhythmen. Das Team veränderte systematisch Fliegen-Versionen menschlicher Parkinson-Risiko-Gene, um zu sehen, welche die Wirkung von Alpha‑Synuclein veränderten. Ein Gen stach hervor: mino, das eine mitochondriale Form des Enzyms Glycerol-3-phosphat-Acyltransferase (GPAT) produziert. GPAT sitzt am Einstiegspunkt der Synthese von Phospholipiden und Triglyceriden — den Lipiden, die Membranen und Fetttröpfchen bilden. Wenn das Team die mino-Aktivität in Neuronen verringerte, behielten die Alpha‑Synuclein-Fliegen mehr ihrer Dopamin-Neurone und bewegten sich länger besser; eine Steigerung von mino hatte den gegenteiligen, schädlichen Effekt.
Beschädigte Fette, gestresste Mitochondrien und gliale Fetttropfen
Bei eingehender Untersuchung stellten die Wissenschaftler fest, dass GPAT beeinflusst, wie viel oxidative Schäden sich in Gehirnlipiden ansammeln. In Alpha‑Synuclein-Fliegen, die bei höherer Temperatur gehalten wurden (was die Krankheitsmerkmale verschlimmert), stieg die Lipidperoxidation — das chemische "Rosten" von Fetten — in Membranen des Gehirns an. Die Reduktion von mino verringerte diesen Schaden, während eine Überexpression ihn vergrößerte; ohne Alpha‑Synuclein hatte eine Veränderung von mino kaum einen Effekt. Marker für Zelltod in der visuellen Gehirnregion spiegelten dieses Muster wider. Das Team beobachtete außerdem eine auffällige Ansammlung von Fetttropfen — winzigen Fettspeicherkugeln — nicht in den Neuronen selbst, sondern in benachbarten Gliazellen. Diese Tropfen vergrößerten sich mit dem Alter in Alpha‑Synuclein-Fliegen und wurden durch Enzyme moduliert, die Triglyceride aufbauen oder abbauen, was eine aktive metabolische Partnerschaft zwischen Neuronen und Glia unter Stress hervorhebt.
Metabolische Umprogrammierung und Alpha‑Synuclein-Verklumpung
Metabolitmessungen aus Fliegengehirnen zeigten, dass die Expression von Alpha‑Synuclein mit einem Flaschenhals im energieproduzierenden Zyklus der Zelle verbunden war: Zitrat und Isocitrat, zwei Zwischenprodukte des Tricarbonsäurezyklus (TCA), häuften sich stark an, während weiter unten liegende Schritte nur moderat verschoben waren. Auch die Laktatwerte stiegen, was mit einer verstärkten Glykolyse vereinbar ist. Gleichzeitig zeigte eine detaillierte Lipidprofilierung Veränderungen im Gleichgewicht der Membranphospholipide und ihrer Fettsäurezusammensetzung, zugunsten von Spezies, die anfälliger für oxidative Schäden sind. Als das Team mehrere GPAT-Enzyme verringerte — mino in den Mitochondrien und verwandte Enzyme am endoplasmatischen Retikulum — akkumulierte Alpha‑Synuclein zwar weiterhin, seine Neigung, höher geordnete Oligomere (Mehrproteinbündel) zu bilden, nahm jedoch ab, und die Mitochondrien zeigten weniger Anzeichen reaktiven Sauerstoffstresses und "Alterns".
GPAT blockieren als Schutzstrategie
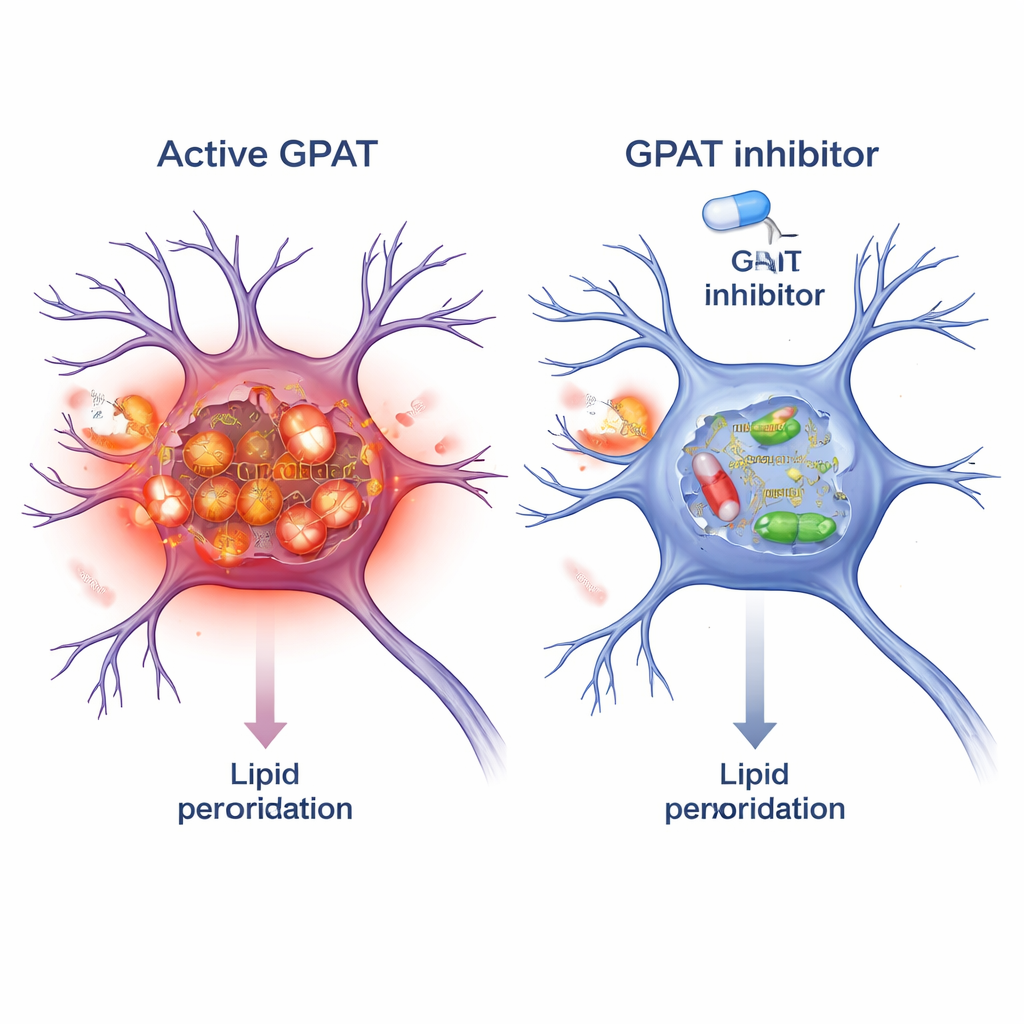
Da GPAT ein Enzym ist, lässt es sich durch niedermolekulare Wirkstoffe ansteuern. Die Forscher testeten FSG67, einen vorhandenen GPAT-Inhibitor, der ursprünglich für Adipositas und Diabetes entwickelt wurde. Bei Alpha‑Synuclein-Fliegen führte die Zugabe von FSG67 zum Futter zu denselben Vorteilen wie die genetische Herunterregulierung von GPAT: verbesserte Bewegung, besseres Überleben der Dopamin-Neurone, weniger schädliche Alpha‑Synuclein-Oligomere und verringerter oxidativer Stress in den Mitochondrien. Um zu prüfen, ob sich dieses Konzept auf Säuger überträgt, behandelten sie in Kultur gehaltene Maus-Hirnneurone mit vorgeformten Alpha‑Synuclein-Fibrillen, die toxische Aggregate anregen. Die gleichzeitige Behandlung mit FSG67 verringerte die Anhäufung phosphorylierten Alpha‑Synucleins und senkte mehrere unabhängige Marker der Lipidperoxidation in diesen Neuronen.
Was das für Menschen mit Parkinson bedeutet
Einfach gesagt zeigt diese Arbeit, dass die Art und Weise, wie das Gehirn mit Fetten umgeht, die Toxizität von Alpha‑Synuclein hoch- oder herunterschalten kann. Bei hoher GPAT-Aktivität werden anfälligere Lipide in Membranen und Speichertropfen eingebaut, was sie leichter oxidierbar macht; diese beschädigte Fettumgebung scheint schädliche Formen von Alpha‑Synuclein zu begünstigen und die Mitochondrien, die Kraftwerke der Zelle, zu belasten. Die Reduktion von GPAT — genetisch oder pharmakologisch — verschiebt das Gleichgewicht hin zu weniger Lipid-"Rost", weniger toxischen Proteinversammlungen und gesünderen Neuronen. Obwohl diese Befunde vorläufig sind und aus Fliegen und kultivierten Maus-Zellen stammen, rücken sie den Fettstoffwechsel und insbesondere GPAT als vielversprechenden neuen Ansatz für Parkinson-Therapien in den Fokus, der Strategien, die direkt Alpha‑Synuclein ansprechen, ergänzen könnte.
Zitation: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Schlüsselwörter: Parkinson-Krankheit, alpha-Synuclein, Lipidperoxidation, GPAT-Inhibitor, Neurodegeneration