Clear Sky Science · de
Mutante KRAS-Impfung mit dualer Checkpoint-Blockade bei reseziertem Pankreaskarzinom: eine Phase-I-Studie
Neue Hoffnungen gegen eine tödliche Krebserkrankung
Das Pankreaskarzinom zählt zu den tödlichsten Krebsarten, vor allem weil es früh streut und auch nach Operation und Chemotherapie häufig wiederkehrt. Diese Studie untersucht eine neue Art von "Training" für das Immunsystem: einen Impfstoff, der häufige Mutationen in dem krebsfördernden Gen KRAS erkennt, kombiniert mit zwei modernen Immuntherapie-Medikamenten. Bei Menschen, denen der Pankreastumor bereits entfernt wurde, zielt dieser Ansatz darauf ab, unsichtbare Krebskeime auszumerzen, bevor sie wieder wachsen.
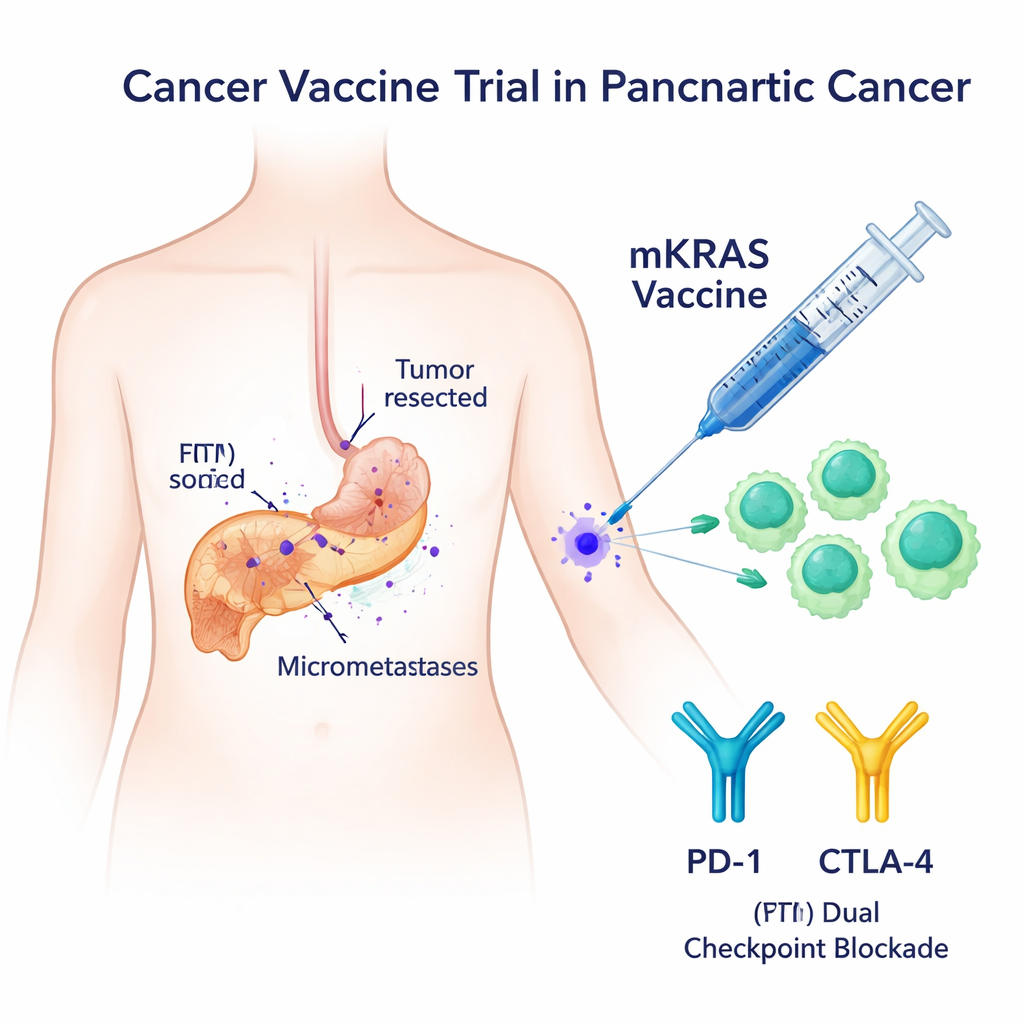
Ein klares Ziel: mutiertes KRAS
Die meisten Pankreastumoren tragen Veränderungen im KRAS-Gen, die wie ein klemmendes Gaspedal für das Zellwachstum wirken. Diese mutierten Varianten – etwa G12V, G12D, G12R, G12C, G12A und G13D – kommen in gesundem Gewebe nahezu nie vor und sind daher attraktive Zielscheiben für das Immunsystem. Frühere Versuche mit KRAS-gezielten Impfstoffen zeigten nur mäßige Immunantworten und konzentrierten sich meist auf ein oder zwei Mutationen. In dieser Phase-I-Studie testeten die Forschenden einen breiteren Impfstoff, mKRAS-VAX genannt, der sechs lange Peptidfragmente der häufigsten KRAS-Mutationen kombiniert und mit den beiden Checkpoint-Medikamenten Nivolumab und Ipilimumab paarte, die T‑Zellen helfen, die sonst gebremst würden.
Entwurf und Verabreichung der Impfstrategie
In die Studie wurden 12 Personen aufgenommen, deren Pankreastumoren chirurgisch entfernt worden waren und die die Standardchemotherapie abgeschlossen hatten, die jedoch weiterhin ein hohes Rückfallrisiko trugen. Bei jedem Teilnehmenden fand sich eine der sechs im Impfstoff enthaltenen KRAS-Mutationen im Tumor. In einer anfänglichen "Prime"-Phase erhielten die Patientinnen und Patienten vier Zyklen des Peptidcocktails, gemischt mit einem immunstimulierenden Adjuvans, zusammen mit den beiden Checkpoint-Medikamenten. Darauf folgten Auffrischungsdosen, und einige Patienten, die nach einem Jahr krebsfrei blieben, setzten ausschließlich Impfstoff-Booster fort. Die Hauptfragen waren, ob diese Kombination sicher ist und ob sie die KRAS-gerichteten T‑Zellen im Blut deutlich verstärkt.
Trainieren und Nachverfolgen von Immunzellen
Anhand von Blutproben, die vor und nach der Impfung entnommen wurden, setzten die Forschenden jeweils die KRAS-Peptide zu, um zu messen, wie viele T‑Zellen Interferon‑Gamma produzierten, einen Schlüsselboten der Immunaktivität. Die Ergebnisse waren für eine kleine Studie bemerkenswert: 11 von 12 Patientinnen und Patienten zeigten insgesamt einen deutlichen Anstieg an T‑Zellen, die die mutierten KRAS-Peptide erkannten, und 10 von 12 entwickelten eine starke Reaktion gegen die spezifische KRAS-Mutation ihres eigenen Tumors. Viele Personen reagierten auf mehrere der sechs KRAS‑Varianten, und einige T‑Zellen erkannten mehr als eine Mutation, was auf eine nützliche Kreuzreaktivität hindeutet. Detaillierte Analysen zeigten, dass die meisten dieser durch den Impfstoff induzierten Zellen CD4‑Helferzellen mit Gedächtnismerkmalen waren, ergänzt durch eine kleinere, aber wichtige Gruppe zytotoxischer CD8‑Zellen mit Kill-Fähigkeit. Das Team kartierte und klonte außerdem Hunderte KRAS‑spezifische T‑Zell-Rezeptoren, darunter einige "öffentliche" Rezeptoren, die bei verschiedenen Patienten geteilt wurden und für künftige zellbasierte Therapien wertvoll sein könnten.
Frühe klinische Signale und Unterschiede je Mutation
Obwohl die Studie nicht groß genug war, um einen Überlebensvorteil nachzuweisen, gab es ermutigende Hinweise. Patientinnen und Patienten mit KRAS‑gerichteten T‑Zell‑Antworten im oberen Dreiviertel blieben tendenziell länger frei von nachweisbarem Krebs als solche mit schwächeren Antworten. Nach etwa drei Jahren Nachbeobachtung blieben ein Drittel der Teilnehmenden krankheitsfrei. Alle vier Patientinnen und Patienten, die bei der letzten Kontrolle noch krebsfrei waren, hatten Tumoren mit KRAS G12V oder G12R, und ihre KRAS‑spezifischen T‑Zellen hielten sich länger als ein Jahr, insbesondere die Gedächtnis‑CD4‑Zellen. Im Gegensatz dazu reagierten Tumoren mit der G12D‑Mutation nicht nur immunologisch schwächer, sondern traten auch häufiger wieder auf, was andere Studien bestätigt, die G12D mit aggressiverem Krankheitsverlauf in Verbindung bringen. Wichtig ist, dass impfstoffbedingte Nebenwirkungen mild waren (hauptsächlich Schmerzen an der Einstichstelle, Müdigkeit und Fieber) und schwerere Immunkomplikationen eher von den Checkpoint‑Medikamenten als vom Impfstoff ausgingen.
Was das für künftige Patienten bedeuten könnte
Kurz gesagt zeigt diese Studie, dass ein "von der Stange"-Impfstoff, der auf mehrere mutierte KRAS‑Ziele abzielt, in Kombination mit modernen Checkpoint‑Medikamenten bei den meisten Menschen mit hohem Risiko für Pankreaskrebs sicher eine breite und anhaltende T‑Zell‑Antwort wecken kann. Obwohl viele Patientinnen und Patienten dennoch ein Rezidiv erlebten, hatten diejenigen mit stärkeren KRAS‑fokussierten Immunantworten tendenziell bessere Verläufe, was darauf hindeutet, dass eine weitere Verstärkung dieser Antworten – oder ein früherer Beginn der Impfung – die Ergebnisse verbessern könnte. Der umfangreiche Katalog KRAS‑spezifischer T‑Zell‑Rezeptoren, der hier entdeckt wurde, eröffnet zudem Möglichkeiten für gentechnisch veränderte T‑Zell‑Therapien. Zusammengenommen deuten diese Befunde darauf hin, dass die Umwandlung von KRAS vom berüchtigten Krebsantreiber zu einer für das Immunsystem erkennbaren Flagge eine Schlüsselstrategie zur Verhinderung des Wiederauftretens von Pankreaskrebs werden könnte.
Zitation: Huff, A.L., Haldar, S.D., Gergis, A.A. et al. Mutant KRAS vaccine with dual checkpoint blockade in resected pancreatic cancer: a phase I trial. Nat Commun 17, 1538 (2026). https://doi.org/10.1038/s41467-026-68324-4
Schlüsselwörter: Pankreaskarzinom-Impfstoff, mutantes KRAS, Immuntherapie, T-Zell-Antwort, Checkpoint-Blockade