Clear Sky Science · de
Struktur des SHOC2-KRAS-PP1C-Komplexes zeigt RAS-Isoform-spezifische Determinanten und Einblicke in die Beeinflussung der Komplexassemblierung durch RAS-Inhibitoren
Wie Zellen entscheiden, wann sie wachsen
Unsere Zellen verlassen sich auf ein internes Verkabelungssystem, um zu entscheiden, wann sie wachsen, sich teilen oder ruhig bleiben. Im Mittelpunkt dieses Systems stehen RAS-Proteine, winzige molekulare Schalter, die bei Krebs häufig gestört sind. Diese Studie untersucht detailliert, wie eine bestimmte Proteingruppe — SHOC2, RAS und PP1C — sich zusammenlagert, um einen entscheidenden Wachstumsschalter umzulegen, und wie moderne Krebsmedikamente so abgestimmt werden könnten, dass sie diesen Prozess effektiver blockieren und verhindern, dass Tumoren die Behandlung überlisten.
Ein Wachstumsschalter mit drei kritischen Teilen
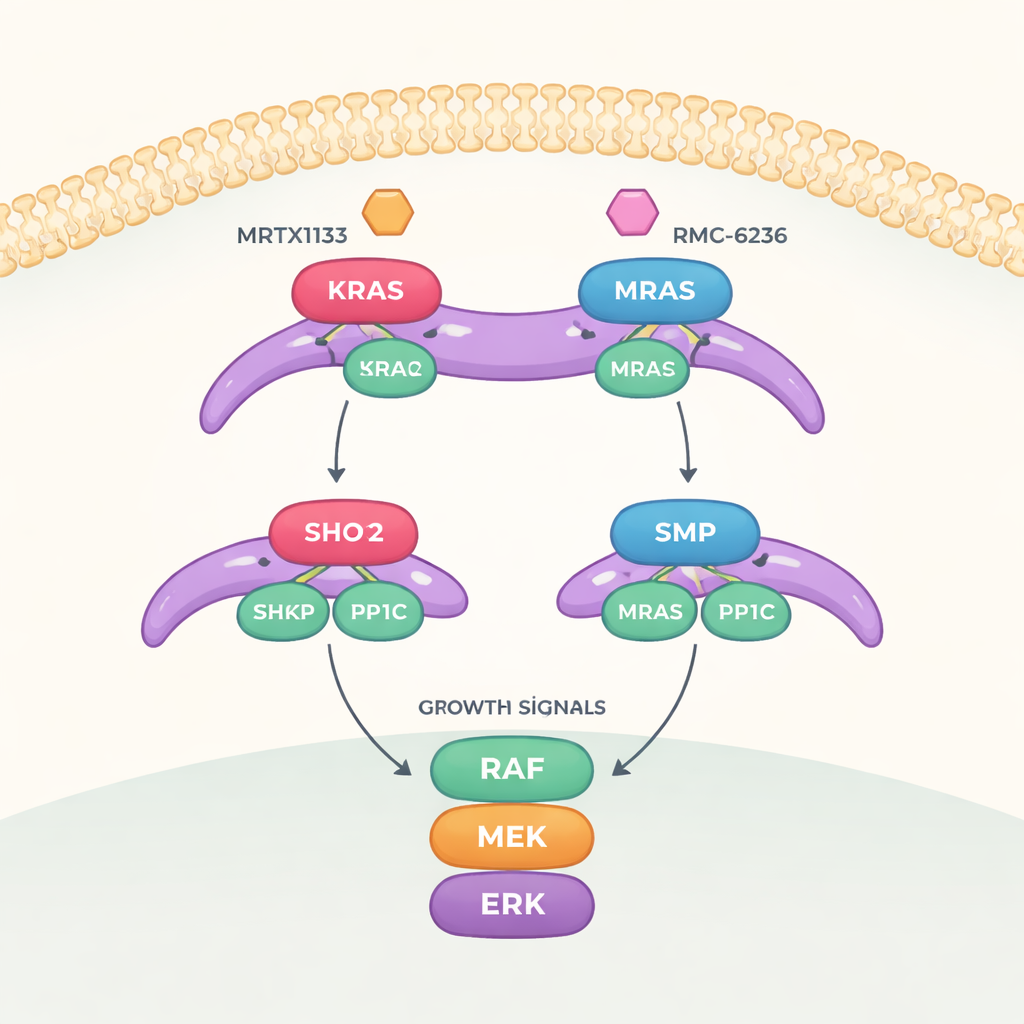
Die Arbeit konzentriert sich auf einen Signalweg namens MAPK, der Wachstumsbotschaften von der Zelloberfläche bis zum Zellkern überträgt. Damit dieser Weg vollständig eingeschaltet wird, muss ein weiteres Protein namens RAF von einem „aus“- in einen „an“-Zustand geschaltet werden. Dieser Schalter wird von einem dreiteiligen Komplex aus SHOC2 (ein Gerüst, das die Komponenten zusammenhält), PP1C (ein Enzym, das eine Phosphatmarke entfernt) und einem aktiven RAS-Protein kontrolliert. Wenn sich dieses Trio zusammenfügt, entfernt es eine spezifische Phosphatmarke von RAF und ermöglicht so dessen Aktivierung der nachgeschalteten Wachstumskaskade.
Warum ein Partner mit geringerer Affinität in Krebs trotzdem wichtig ist
Es gibt mehrere Arten von RAS-Proteinen. MRAS bildet einen sehr stabilen Komplex mit SHOC2 und PP1C, während die bekannteren Krebsantreiber KRAS, HRAS und NRAS schwächere Versionen desselben Komplexes ausbilden. Überraschenderweise sind Krebszellen, die von mutiertem KRAS, HRAS oder NRAS getrieben werden, stark von SHOC2 abhängig, obwohl ihre Komplexe weniger stabil sind. Große genetische Screening-Datensätze zeigen, dass viele Tumoren mit bestimmten RAS-Mutationen — insbesondere solche, die Schlüsselpositionen wie Q61 und G13 betreffen — hochsensibel gegenüber dem Verlust von SHOC2 sind, was bedeutet, dass diese Assemblierung für ihr Überleben essenziell ist.
Die Gestalt des KRAS-Komplexes enthüllen
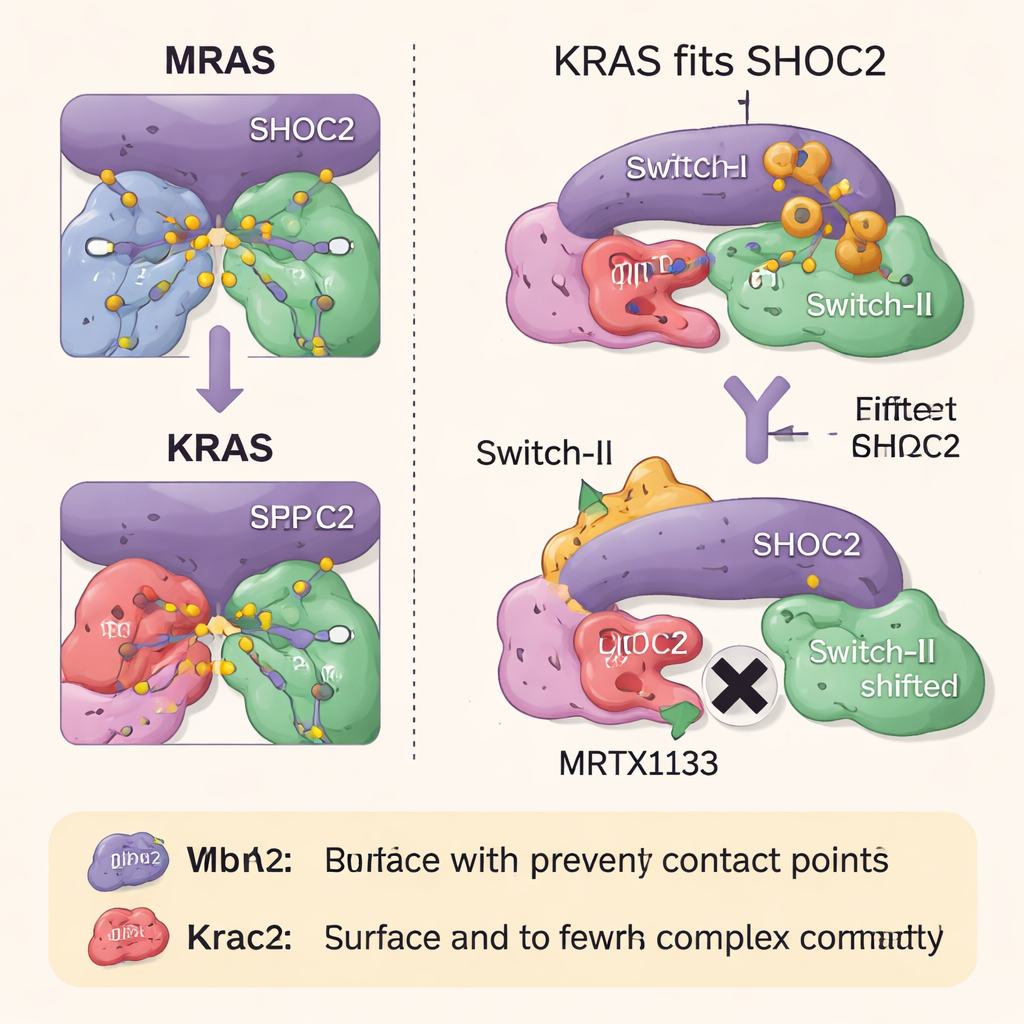
Bisher hatten Wissenschaftler nur eine hochaufgelöste Struktur des stabilen MRAS-basierten Komplexes gesehen. Die schwächere KRAS-Version zerfiel zu leicht, um erfasst zu werden. In dieser Studie nutzten die Autoren krankheitsverbundene Mutationen, die die Kontakte zwischen den Komponenten subtil verstärken, um den SHOC2–KRAS–PP1C-Komplex lange genug zu stabilisieren, um ihn mittels Kryo-Elektronenmikroskopie zu visualisieren. Sie stellten fest, dass die Gesamtarchitektur eng mit der des MRAS-Komplexes übereinstimmt, KRAS jedoch mehrere kleine strukturelle Merkmale fehlen, mit denen MRAS SHOC2 und PP1C fester greift. Infolgedessen vergräbt der KRAS-Komplex eine geringere Kontaktfläche und bildet weniger Bindungen, was erklärt, warum er von Natur aus weniger stabil ist, obwohl er in Tumoren mit überaktivem KRAS weiterhin von großer Bedeutung bleibt.
Wie RAS-Medikamente die Komplexassemblierung blockieren
Das Team untersuchte anschließend, wie zwei Klassen von RAS-zielgerichteten Medikamenten diesen dreiteiligen Komplex beeinflussen. MRTX1133, entwickelt, um eine Tasche in der Nähe einer flexiblen Region von KRAS zu binden, bekannt als Switch-II, fixiert diese Region in einer Form, die mit der SHOC2-Oberfläche kollidiert. Das verhindert stark die Neubildung von SHOC2–KRAS–PP1C-Komplexen, ist jedoch weniger wirksam darin, bereits existierende Komplexe zu zerstören. Ein zweites Medikament, RMC-6236, wirkt gemeinsam mit einem Helferprotein (Cyclophilin A) und blockiert ebenfalls dieselben KRAS-Oberflächen, die für die SHOC2-Bindung erforderlich sind. Keines der beiden Mittel bindet jedoch natürlich an MRAS, sodass der hochaffine MRAS-Komplex intakt bleibt und helfen kann, den Wachstumsweg wiederzubeleben, wenn KRAS gehemmt wird.
Auf dem Weg zu doppelter Zielrichtung, um Resistenz zu verhindern
Um zu testen, ob eine doppelte Zielrichtung möglich ist, konstruierten die Forscher eine Variante von MRAS, deren Switch-II-Tasche so verändert war, dass MRTX1133 nun binden konnte. Dieser Mutant bildete weiterhin einen starken Komplex mit SHOC2 und PP1C, aber das Medikament blockierte nun dessen Assemblierung und verringerte seine Fähigkeit, RAF in Testversuchen zu aktivieren. Zusammen mit Daten zu SHOC2-bindenden Verbindungen zeigen diese Ergebnisse, dass es realistisch ist, Wirkstoffe zu entwickeln, die sowohl die KRAS- als auch die MRAS-basierten Komplexe abschalten. Für Laien lautet die Kernbotschaft, dass Krebszellen mehrere, eng verwandte Schalter nutzen, um Wachstumssignale aufrechtzuerhalten, insbesondere wenn einer der Schalter medikamentös angegriffen wird. Durch das Verständnis der genauen Formen und Kontakte innerhalb dieser Proteinkomplexe können Forscher nun Therapien planen, die beide Ausweichrouten gleichzeitig treffen und es RAS-getriebenen Krebserkrankungen erschweren, sich anzupassen und Resistenz zu entwickeln.
Zitation: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Schlüsselwörter: RAS-Signalübertragung, KRAS-Inhibitoren, MAPK-Signalweg, Proteinkomplexe, Medikamentenresistenz