Clear Sky Science · de
Injektierbare Hydrogele zur Behandlung von Osteomyelitis induzieren metabolische Umprogrammierung zum Schutz vor Reinfektionen
Den Körper zum eigenen Infektionsbekämpfer machen
Knocheninfektionen, insbesondere solche durch antibiotikaresistente Bakterien, sind notorisch schwer zu heilen und kehren oft zurück, selbst nach langen Antibiotikakuren und Operationen. Diese Studie beschreibt ein injizierbares Gel, das direkt in infizierte Knochen eingebracht wird, wo es nicht nur Keime abtötet, sondern auch die angeborenen Abwehrkräfte des Körpers schult und den Knochen beim Wiederaufbau unterstützt. Die Arbeit weist in eine Zukunft, in der Materialien mehr tun als nur Antibiotika abgeben — sie coachen auch unser Immunsystem, um Rückfälle zu verhindern.
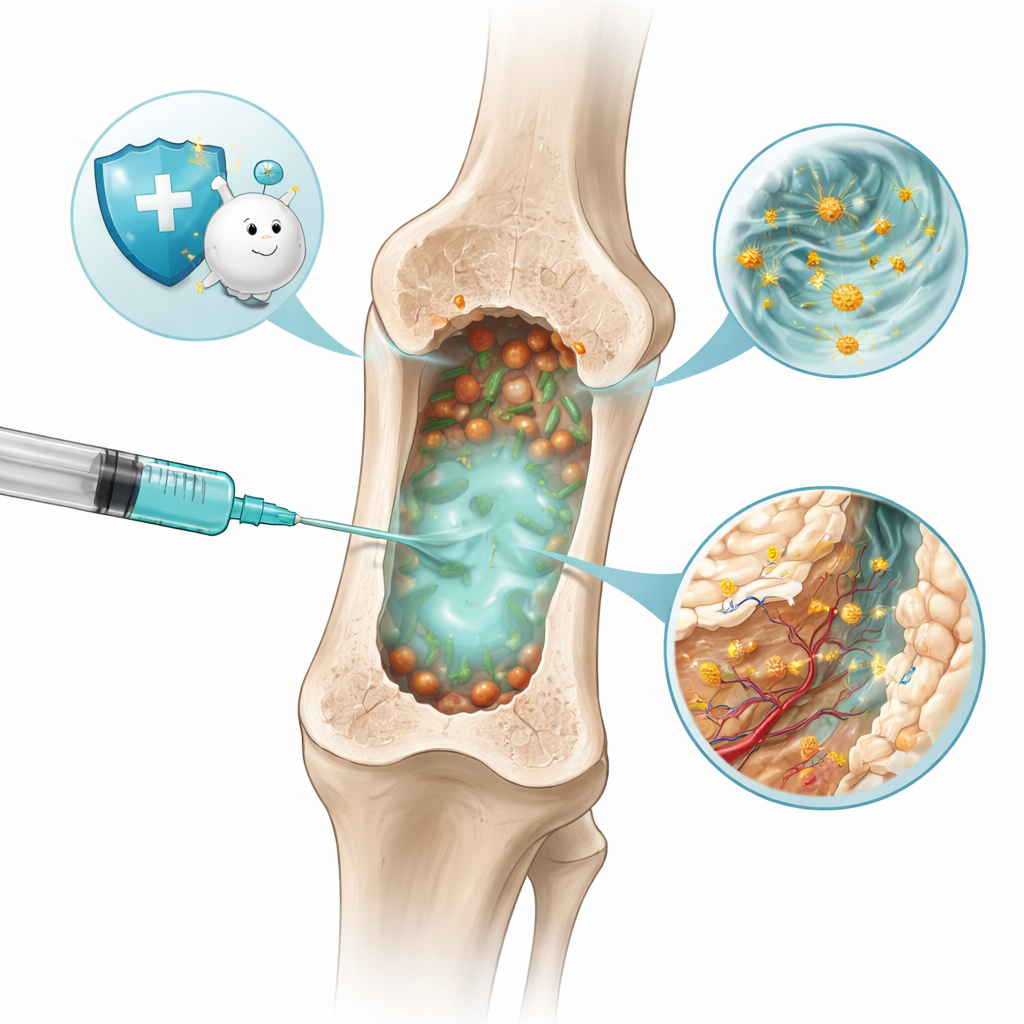
Ein klebriges Gel, das sich im Knochen bildet
Die Forschenden entwickelten ein weiches Material, ein Hydrogel, das als Flüssigkeit injiziert werden kann und sich dann schnell in der Markhöhle des Knochens verfestigt — dem schwammigen Zentrum der Knochen, in dem viele Immunzellen entstehen. Ihr Gel mit dem Namen GaCuVan&HACHO‑BSA besteht aus zwei ineinandergreifenden Netzwerken. Ein Netzwerk kombiniert ein natürliches Pflanzenmolekül aus Süßholz (Glycyrrhizinsäure), Kupferionen und das Antibiotikum Vancomycin. Das andere verwendet eine modifizierte Form von Hyaluronsäure — einem Zucker, der in unseren Gelenken vorkommt —, verbunden mit einem gängigen Blutprotein. Zusammen bilden diese Komponenten ein poröses, flexibles Gerüst, das durch eine Nadel fließt, unregelmäßige Räume ausfüllt und über etwa einen Monat langsam abgebaut wird.
Bakterien und Toxine an der Quelle fangen
Einmal im infizierten Knochen wirkt das Hydrogel wie ein intelligenter Schwamm. Seine winzigen Poren und chemischen Gruppen erlauben es, Bakterien wie methicillinresistenter Staphylococcus aureus (MRSA) sowie Teile von bakteriellen Zellwänden und entzündungsfördernden Molekülen, die im infizierten Gewebe umherschwimmen, einzufangen. Vancomycin auf der Geloberfläche hilft, die gefangenen Bakterien zu binden und abzutöten, während andere chemische Bindungen bakterielle Toxine und Signalproteine festhalten. Labortests zeigten, dass dieses Gel die meisten Bakterien und schädlichen Faktoren aus seiner Umgebung deutlich besser entfernen konnte als einfachere Gele und dabei ausreichend stabil blieb, um Defekte im Knochen zu stützen und auszufüllen.
Umprogrammierung der angeborenen Immunität
Über die Funktion als lokales Arzneimitteldepot hinaus verwandelt das Hydrogel das infizierte Mark in einen Übungsplatz für vorderste Immunzellen. Da das Gel bakterielle Fragmente und entzündliche Signale zurückhält, werden diese Hinweise kontinuierlich an nahegelegene Makrophagen und andere angeborene Zellen präsentiert, statt rasch weggespült zu werden. In Rattenversuchen führte das zu einer Welle kurzzeitiger Entzündung: Mehr weiße Blutkörperchen trafen ein, und knochenansässige Immunzellen schalteten in einen aktivierten, bakterienbekämpfenden Zustand. Tiefe genetische und metabolische Analysen des Knochenmarks zeigten, dass Schlüsselwege der Gefahrenwahrnehmung aktiviert wurden und Zellen ihren Energieverbrauch zugunsten schneller, zuckerbasierten Stoffwechselwege umstellten — Kennzeichen der sogenannten „trainierten Immunität“, einer Form angeborenen Gedächtnisses, die Zellen darauf vorbereitet, beim nächsten Kontakt mit Eindringlingen stärker zu reagieren.
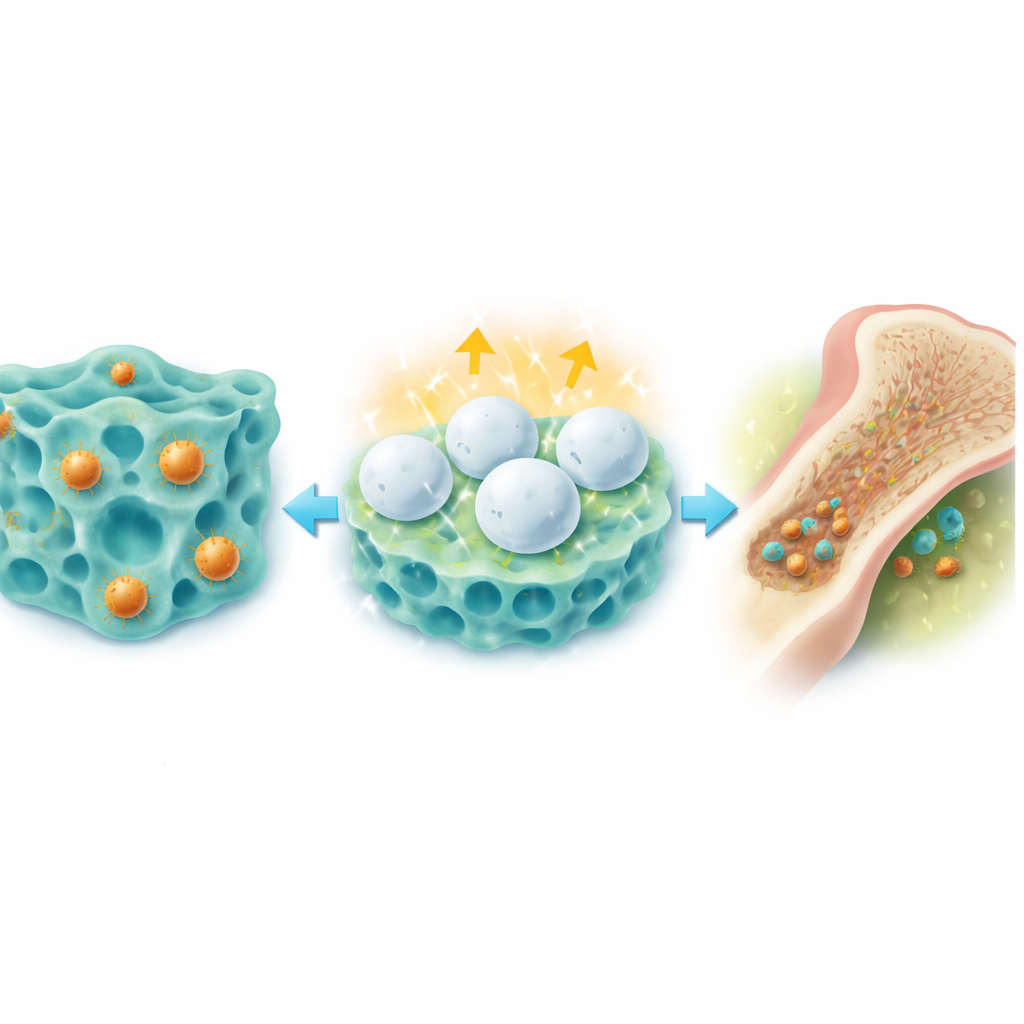
Beseitigung der Infektion und Unterstützung der Knochenheilung
Bei Ratten mit schweren MRSA‑Knocheninfektionen reduzierte eine einmalige Injektion des Hydrogels in den Knochen die Bakterienzahlen im Mark rasch auf nahezu null, während Tiere, die mit Standard‑Vancomycin oder einfacheren Gelen behandelt wurden, oft weiterhin stark infiziert blieben. Das Gel förderte außerdem das Wachstum neuen Knochens. Kupfer und die süßholzabgeleitete Komponente schubsten Stammzellen in Richtung knochenbildender Zellen, steigerten Marker der Knochenbildung und erhöhten Dichte sowie Festigkeit geschädigter Schienbeine. Bildgebende Verfahren und Gewebsfärbungen über mehrere Wochen zeigten, dass Defekte in infizierten Knochen behandelter Tiere nahezu verschlossen wurden, wobei geordneter, gesunder Neubau den beschädigten Bereich ersetzte.
Schutz vor zukünftigen Infektionen
Bemerkenswert war, dass vorbehandelte Knochen späteren Attacken widerstanden. Wenn Ratten, bei denen die Erstinfektion beseitigt worden war, erneut exponiert wurden — entweder mit demselben MRSA‑Stamm oder mit anderen Stämmen und verwandten Bakterien —, mobilisierten ihre Knochen rasch starke Entzündungsreaktionen, begrenzten das Bakterienwachstum und verhinderten oft eine Reinfektion. Das Blockieren des veränderten Zuckerstoffwechsels der Zellen beseitigte diesen Schutz, was bestätigte, dass die metabolische „Umprogrammierung“ angeborener Immunzellen wesentlich war. Der Effekt trat bei normalen und älteren Ratten auf, war aber bei diabetischen Tieren schwächer, deren Immunsystem bereits metabolisch gestört ist.
Was das für Patienten bedeuten könnte
Für Menschen mit chronischen oder medikamentenresistenten Knocheninfektionen könnte ein solches injizierbares Gel eines Tages mehr bieten als einen vorübergehenden Antibiotika‑Boost. Indem das Mark mit einem Material besät wird, das Keime einfängt, Antibiotika und knochenbildende Ionen freisetzt und angeborene Immunzellen darin trainiert, bei zukünftigen Bedrohungen schneller und stärker zu reagieren, könnten Ärzte sowohl die aktuelle Erkrankung heilen als auch das Rückfallrisiko senken. Obwohl noch weitere Arbeiten nötig sind — insbesondere in größeren Tieren und bei Menschen mit komplexen Erkrankungen —, führt die Studie eine neue Denkweise in die Behandlung von Knocheninfektionen ein: smarte Materialien nicht nur zur Wirkstoffabgabe zu verwenden, sondern die lokale Immun‑ und Reparaturumgebung langfristig umzubauen und zu schützen.
Zitation: Chen, H., Wei, L., Yu, Q. et al. Injectable hydrogels for osteomyelitis treatment induce metabolic reprogramming for protection against reinfection. Nat Commun 17, 1613 (2026). https://doi.org/10.1038/s41467-026-68318-2
Schlüsselwörter: Osteomyelitis, Hydrogel‑Therapie, trainierte Immunität, Knochenregeneration, Antibiotikaresistenz