Clear Sky Science · de
Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM
Warum winzige Zellkanäle für Gesundheit und Krankheit wichtig sind
Sekündlich tauschen unsere Zellen elektrische Signale und kleine Moleküle durch mikroskopische Tunnel aus, die Gap‑Junctions genannt werden. Diese Kanäle sorgen dafür, dass das Herz synchron schlägt, das Gehirn toxische Abbauprodukte entfernt und die Augenlinse transparent bleibt. Wenn das Zellinnere sauer wird, wie bei Schlaganfall, Herzinfarkt oder bei der Entstehung von Katarakten, schließen viele dieser Kanäle – doch wie sie Säure wahrnehmen und darauf reagieren, war lange Zeit ein Rätsel. Diese Studie nutzt hochauflösende Kryo‑Elektronenmikroskopie, um nahezu atomar zu zeigen, wie bestimmte Kanäle in der Augenlinse auf Säure schließen und wie dieser Prozess vollständig reversibel sein kann.
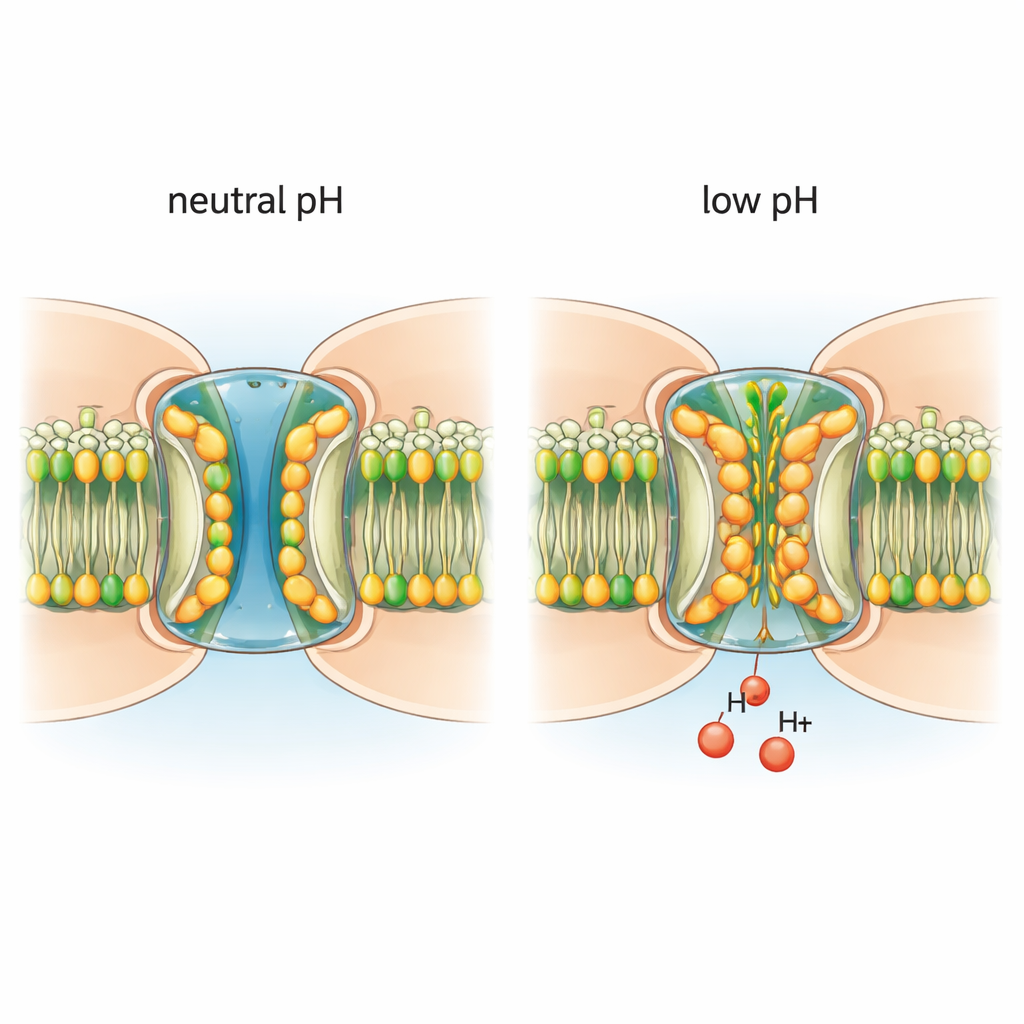
Zelluläre Tunnel, die Gewebe synchron halten
Gap‑Junctions bestehen aus Proteinen, die Connexine genannt werden und sich zu ringförmigen Kanälen zusammenschließen, die die Membranen zweier benachbarter Zellen überbrücken. Diese Arbeit konzentriert sich auf ein Paar eng verwandter Connexine, Connexin‑46 und Connexin‑50, die Kanäle in der Augenlinse bilden. Diese Kanäle erlauben Ionen und kleinen Molekülen, direkt zwischen Zellen zu fließen, und tragen so zur Klarheit der Linse und zur Gesundheit des Gewebes bei. Unter Stress können dieselben Kanäle jedoch auch Wege für schädliche Signale werden. Zum Schutz schließen sich Gap‑Junctions, wenn das Zellinnere saurer wird. Das Verständnis des fein abgestimmten Mechanismus dieses „pH‑Gatings“ ist wichtig, um nachzuvollziehen, wie Gewebe Stress überstehen und warum bestimmte Mutationen zu Erkrankungen wie Katarakten führen.
Kanäle in Bewegung sehen mit Kryo‑EM
Die Forschenden reinigten native Connexin‑46/50‑Kanäle aus alten Schafslinsen und setzten sie in eine Modellmembran ein. Mithilfe der Kryo‑Elektronenmikroskopie bildeten sie die Kanäle unter nahezu atomarer Auflösung ab, sowohl unter neutralen Bedingungen, die einen offenen Porus begünstigen, als auch unter mild sauren Bedingungen, die das Schließen auslösen. Bei neutralem pH liegen die Kanäle überwiegend in einem stabilen offenen Zustand vor, mit einem zentralen Tunnel, der breit genug für Ionen und kleine Moleküle ist, und einem flexiblen Segment, der N‑terminalen Domäne, das den Poreinstieg auskleidet. Unter diesen Bedingungen ist der Porus frei: keine zusätzlichen Moleküle blockieren den Weg, und die umgebenden Membranlipide bleiben in regelmäßigen Schichten organisiert.
Säure zieht Lipide in den Porus
Wurde die Umgebung mild sauer, veränderte sich die Architektur des Kanals eindrücklich. Lipidmoleküle aus der umgebenden Membran wurden in den Porus hineingezogen und glitten zwischen und unter die N‑terminalen Segmente. Diese eindringenden Lipide bilden eine zweilagige hydrophobe „Dichtung“, die die N‑terminalen Domänen nach innen drückt, den Kanal verengt und so den Durchfluss blockiert. Weitere Lipide verkeilen sich an den Schnittstellen benachbarter Proteinuntereinheiten und dienen offenbar als Zugangswege von der Membran in den Porus. Wichtig ist, dass in einer Tensidumgebung ohne echte Lipidmembran niedriger pH diese strukturellen Veränderungen nicht mehr hervorrief. Das zeigt, dass echte Lipide nicht bloß passiv danebenstehen: Sie sind erforderliche Partner im pH‑Gating‑Prozess.
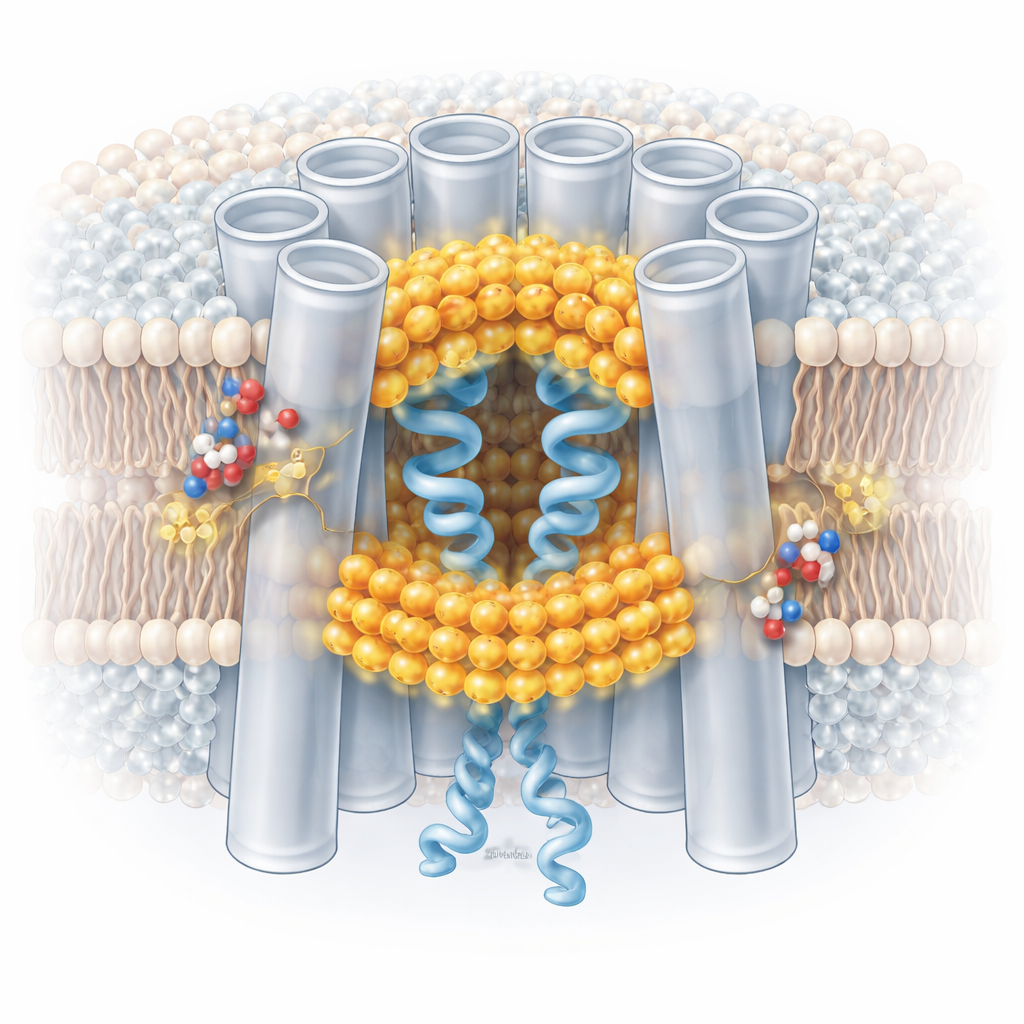
Ein reversibler und fein abgestimmter Sicherheitsschalter
Indem die Autor:innen Millionen einzelner Kanalpartikel verfolgten, fanden sie heraus, dass niedriger pH die Kanäle nicht einfach von vollständig offen zu vollständig geschlossen umschaltet. Vielmehr verschiebt er die Population zu einer Mischung von Zuständen: Einige Untereinheiten innerhalb eines Kanals zeigen lipidstabilisierte, geschlossene Konformationen, während andere offen bleiben. Das Gating-Verhalten ist weitgehend nicht‑kooperativ – jeder Baustein des Kanals kann sich einigermaßen unabhängig verhalten. Saure Bedingungen begünstigen diese geschlossenen Konformationen, doch sobald der pH wieder neutral wird, ziehen sich die Porenlipide zurück in die Membran und die Kanäle nehmen den offenen Zustand wieder ein. Konservierte Aminosäuren, sogenannte Histidine, die bei niedrigem pH positive Ladung aufnehmen, scheinen zu helfen, die interfacialen Lipide zu rekrutieren und zu stabilisieren, die diesen Prozess einleiten, und bieten somit einen plausiblen molekularen pH‑Sensor.
Folgen für Katarakte und Gewebeschutz
Diese Ergebnisse stützen ein Modell, in dem Lipide als bewegliche Stopfen wirken, die reversibel den Durchfluss durch Gap‑Junctions als Reaktion auf Säure steuern. In der Augenlinse kann ein solcher Mechanismus dazu beitragen, beschädigte Zellen zu isolieren und zu verhindern, dass toxische Signale sich ausbreiten; chronisches oder fehlreguliertes Gating könnte jedoch auch zur altersbedingten Kataraktbildung beitragen. Da ähnliche Lipideindringungen in verwandten Kanal‑Familien beobachtet wurden, legt die Arbeit ein allgemeineren Prinzip nahe: Unter Stress können Zellmembranen selbst dynamische Komponenten bereitstellen, die lebenswichtige Kanäle an‑ oder ausschalten, und damit neue Ideen für Medikamente liefern, die entweder den offenen oder den geschlossenen Zustand in Erkrankungen stabilisieren.
Zitation: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Schlüsselwörter: gap junctions, connexin 46/50, pH gating, cataract, cryo-EM