Clear Sky Science · de
Dynamische Einzelzell-Transkriptomik enthüllt lsamp-gesteuerte Bildung neuronaler Netzwerke im männlichen S. japonicum, die die weibliche Reproduktion antreiben
Warum das Liebesleben eines Parasiten wichtig ist
Die Schistosomiasis ist eine parasitäre Erkrankung, die mehr als 250 Millionen Menschen krank macht, vor allem in ärmeren Regionen mit begrenztem Zugang zu medizinischer Versorgung. Die Krankheit wird dabei nicht durch Bisse oder Gifte der Würmer verursacht, sondern durch die enorme Zahl von Eiern, die weibliche Parasiten im Körper ablegen. Überraschenderweise können weibliche Würmer erst nach dem Koppeln mit einem Männchen ausreifen und Eier legen. Diese Studie stellt eine einfache, aber entscheidende Frage: Was genau tut das Männchen, um die Fruchtbarkeit des Weibchens einzuschalten — und ließe sich dieser Schalter ausschalten, um die Krankheit zu stoppen?
Eine verborgene Welt zellgenau kartieren
Um das zu beantworten, erstellten die Forscher einen detaillierten „Zellatlas“ des Blutegels Schistosoma japonicum in dem entscheidenden Zeitraum, in dem Männchen und Weibchen paaren und sexuell reifen. Mittels Einzelzell-RNA-Sequenzierung, einer Methode, die abliest, welche Gene in einzelnen Zellen aktiv sind, analysierten sie mehr als 100.000 Zellen aus Würmern, die zu vier Zeitpunkten nach der Infektion in Mäusen gewonnen wurden. Sie identifizierten 76 verschiedene Zelltypen, darunter viele Arten von Nervenzellen, Stammzellen und Fortpflanzungszellen. So konnten sie verfolgen, wie sich bestimmte Zellpopulationen vergrößern, verkleinern oder ihre Identität ändern, während die Würmer wachsen und mit der Fortpflanzung beginnen.
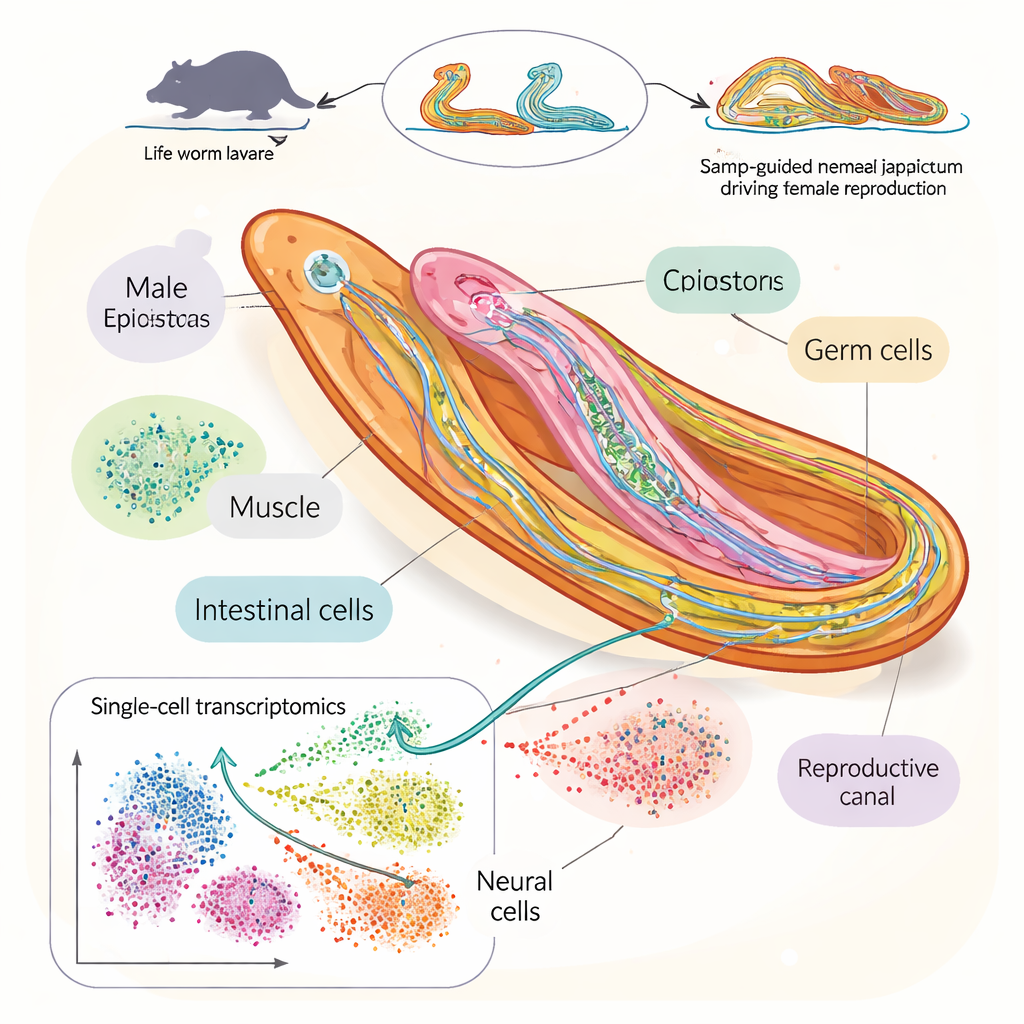
Dem Aufstieg von Eiern und Spermien folgen
Indem sie Zellen aus Hoden, Eierstöcken und verwandten Geweben genauer betrachteten, rekonstruierten die Forschenden die schrittweise Entwicklung von Spermien und Eizellen. Sie zeigten, wie keimbahnbezogene Stammzellen durch geschlechtsspezifische Genaktivitätsprogramme zu spätstadialen Spermien- und Eizellen heranreifen. Bei Weibchen betonen die Gene, die das Wachstum der Eizellen fördern, vor allem Proteinproduktion und -verpackung, während bei Männchen mehr Gewicht auf Strukturen wie Zilien und Mikrotubuli gelegt wird, die die Beweglichkeit der Spermien unterstützen. Die Studie kartierte außerdem, wie das umfangreiche eierstützende Organ der Weibchen, das Vitellarium, über Zwischenstadien entsteht, und identifizierte neue genetische Marker, die zeigen, wie ausgereift die jeweiligen Fortpflanzungsgewebe sind.
Ein männlicher Nervenschaltkreis in einem Umklammerungskanal
Einer der eindrücklichsten Befunde kam aus dem Nervensystem. Statt einer lockeren Ansammlung von Nervenzellen zeigte der Atlas fünf deutliche neuronale Abstammungslinien, darunter mehrere, die zwischen Männchen und Weibchen unterschieden. Drei Neuronentypen — bezeichnet N2.2, N3.2 und N4.3 — waren stark bei Männchen angereichert und konzentrierten sich im gynekophoralen Kanal, einer spezialisierten Rinne, die das Männchen nutzt, um das Weibchen zu umschließen. Unter diesen stachen die N4.3-Neurone hervor, weil sie ein Gen namens nrps exprimierten, das das Enzym produziert, das BATT herstellt — ein kleines Peptidpheromon, das zuvor gezeigt wurde, dass es die sexuelle Entwicklung von Weibchen anregt. Anders gesagt: Diese N4.3-Zellen sind die „Signalstationen“ des Männchens, um die Fruchtbarkeit des Weibchens einzuschalten.
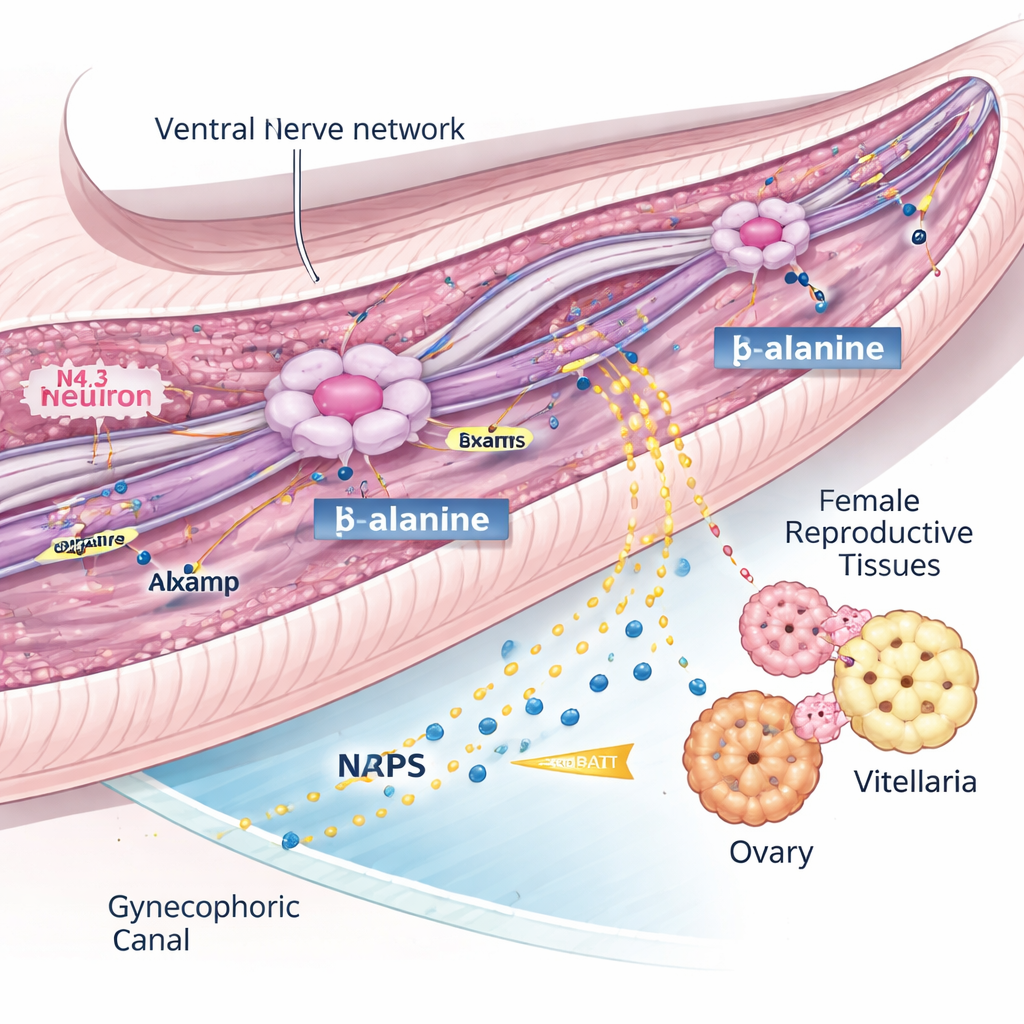
Ein Leitmolekül, das das Signal aufrechterhält
Um zu verstehen, wie diese N4.3-Neurone funktionieren, suchten die Forscher nach Genen, die deren Entwicklung und Funktion zu steuern scheinen. Sie konzentrierten sich auf lsamp, ein Gen, das bei anderen Tieren dafür bekannt ist, Nervenzellen dabei zu helfen, Verbindungen zu bilden und Axone zu stabilisieren. Bei männlichen Saugwürmern wurde lsamp in denselben N4.3-Neuronen aktiviert, die auch das BATT-Enzym herstellen, und seine Aktivität stieg stark an, als die Würmer reiften. Durch RNA-Interferenz, um lsamp in Männchen zu reduzieren, fanden die Forschenden heraus, dass gekoppelte Weibchen ihre Ovarien und das Vitellarium nicht vollständig entwickelten und nahezu keine Eier legten. Die N4.3-Neurone waren zwar weiterhin vorhanden, das nrps-Gen blieb aktiv und die chemischen Ausgangsstoffe für BATT schienen unverändert. Stattdessen zeigten lsamp-defiziente Männchen geschädigte Nervenfasern und gestörten Vesikeltransport entlang stabilisierter Mikrotubuli, und sie produzierten deutlich weniger BATT innerhalb ihres Körpers und in das umgebende Medium. Das deutet darauf hin, dass lsamp entscheidend ist, um ein ventrales Nervennetzwerk aufrechtzuerhalten, das einen wichtigen Vorläuferstoff — vermutlich β-Alanin — zu den N4.3-Neuronen liefert, damit diese genug Pheromon synthetisieren können, um das Weibchen zu aktivieren.
Den Reproduktionsschalter herunterdrehen
Für Nichtfachleute ist die Kernaussage, dass die Krankheitsfähigkeit dieses Parasiten von einem engen Dialog zwischen Männchen und Weibchen abhängt, vermittelt über ein spezialisiertes Nervennetzwerk und ein winziges Pheromon. Die Studie zeigt, dass ein einzelnes Leitmolekül, lsamp, beim Aufbau und Erhalt der ventralen Nervenverkabelung des Männchens hilft; wenn diese Verkabelung versagt, kann das Männchen kein ausreichend starkes chemisches Signal mehr senden, um die Fortpflanzungsorgane des Weibchens vollständig reifen zu lassen, und die Eiproduktion sinkt drastisch. Durch die hochauflösende Kartierung der Zellen des Parasiten und die Aufdeckung dieses nur beim Männchen vorhandenen neuronalen Schaltkreises weist die Arbeit auf neue Ansätze hin, die Eiproduktion zu blockieren — und bietet eine potenzielle Strategie zur Eindämmung der Schistosomiasis, für die derzeitige Behandlung auf ein einziges, alterndes Medikament angewiesen ist.
Zitation: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Schlüsselwörter: Schistosomiasis, Einzelzell-Transkriptomik, Parasitenreproduktion, neurale Schaltkreise, Pheromon-Signalübertragung