Clear Sky Science · de
Mechanismus der SARS-CoV-2-Resistenz gegenüber nukleotidanalogbasierten antiviralen Mitteln
Wie das Virus wichtige antivirale Wirkstoffe austrickst
Das COVID-19-Virus gehört zu einer seltenen Gruppe von RNA-Viren, die ihr genetisches Material korrigieren können; dadurch sind sie ungewöhnlich gut darin, einigen unserer besten antiviralen Medikamente zu widerstehen. Diese Studie untersucht die atomaren Details, wie SARS-CoV-2 eine weit verbreitete Wirkstoffklasse — die Nukleotidanaloga — erkennt und entfernt, und erklärt, warum Medikamente, die gegen andere Viren gut funktionieren, bei Coronavirus-Infektionen oft weniger wirksam sind.
Ein Tauziehen um die virale RNA
SARS-CoV-2 kopiert sein etwa 30.000 Basen umfassendes RNA-Genom mit einer großen molekularen Maschine, dem Replikations–Transkriptions-Komplex. Im Zentrum steht die RNA-abhängige RNA-Polymerase (RdRp), die neue RNA-Stränge synthetisiert, und eine separate Einheit, die Exonuklease (ExoN), die Fehler korrigiert und abschneidet. Viele antivirale Pillen, einschließlich solcher, die ursprünglich gegen Hepatitis C entwickelt wurden, ahmen die natürlichen RNA-Bausteine so nach, dass die RdRp sie einbaut, aber mit kleinen Modifikationen, die das Weiterkopieren stoppen oder Fehler einführen. Unglücklicherweise besitzt das Coronavirus ExoN, das diese Betrüger erkennen kann, sobald sie in die RNA-Kette eingebaut sind, und sie wieder herausschneidet, wodurch die virale Replikation gerettet wird.
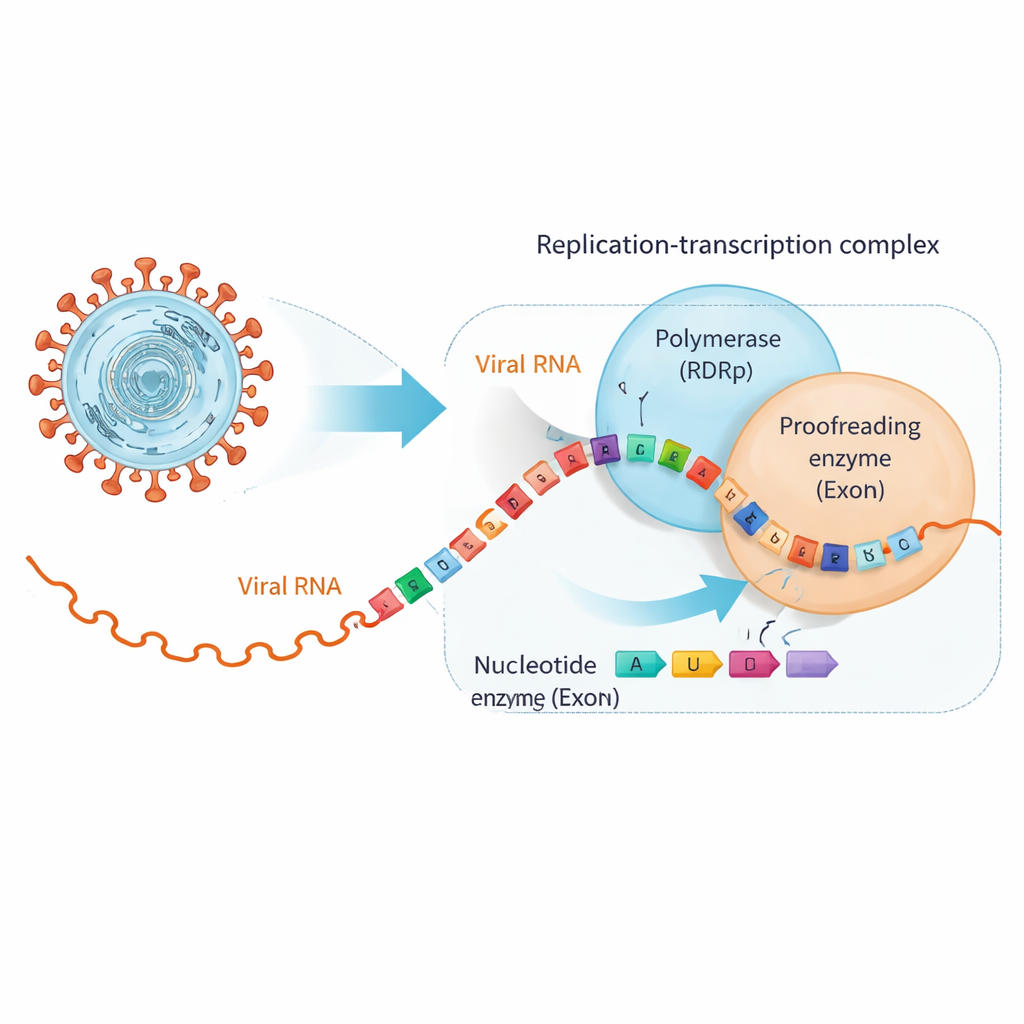
Wenn nützliche Medikamente die RNA den Partner wechseln lassen
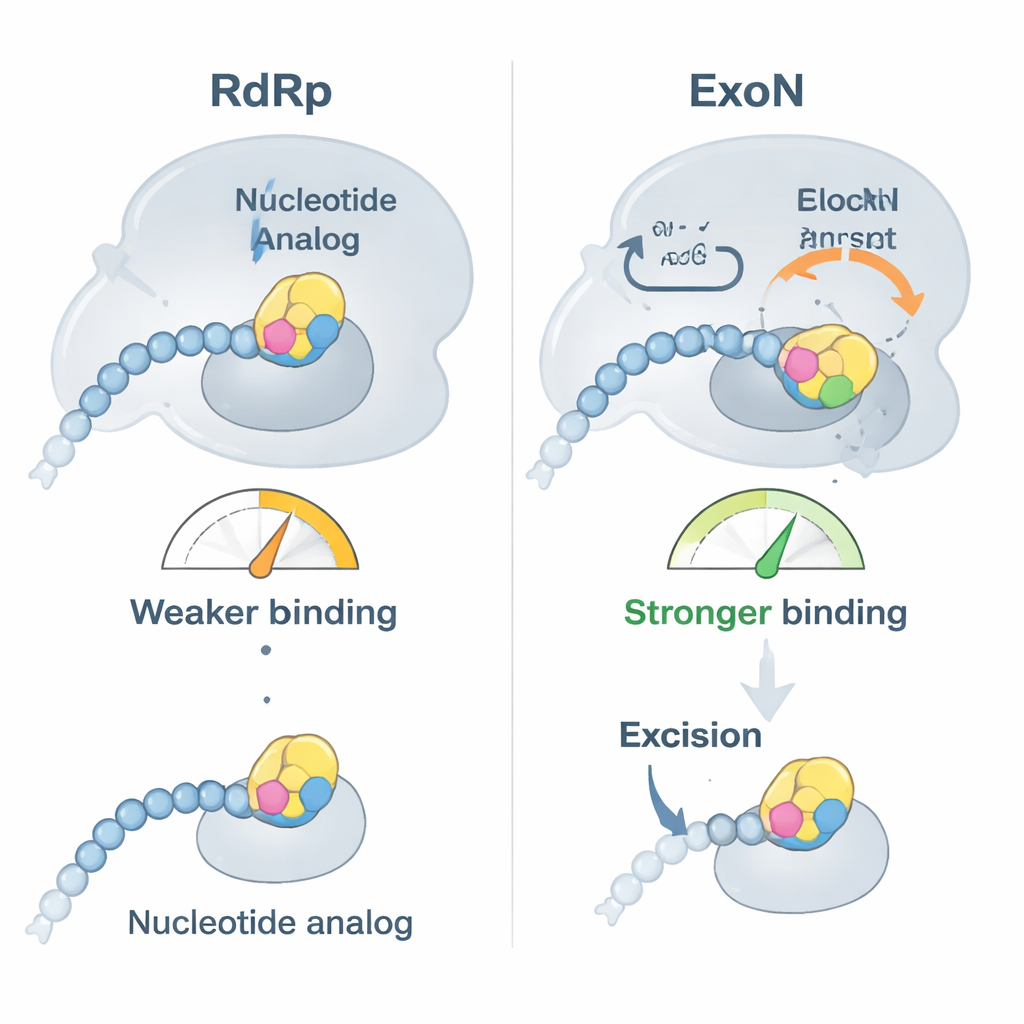
Die Forscher konzentrierten sich auf zwei klinisch wichtige antivirale Wirkstoffe, Bemnifosbuvir und Sofosbuvir, die beide als fehlerhafte RNA-Bausteine konzipiert sind. Zunächst zeigten sie, dass die Polymerase von SARS-CoV-2 diese Analoga am Ende eines RNA-Strangs bereitwillig einfügt und dann weitgehend aufhört, die Kette weiter zu verlängern, wie beabsichtigt. Bindungstests enthüllten jedoch eine Wendung: Sobald ein Analog an der RNA-Spitze sitzt, haftet die RNA nicht mehr so fest an der Polymerase, sondern bindet stattdessen stärker an ExoN. Effektiv wird die mit dem Wirkstoff veränderte RNA vom Kopierapparat weggeschoben und dem Korrekturleser übergeben, der dann die Möglichkeit hat, das problematische Nukleotid abzuschneiden und die Replikation fortzusetzen.
Korrekturlesen, das verlangsamt, aber nicht gestoppt wird
Biochemische Zeitverlaufs-Experimente zeigten, dass ExoN Bemnifosbuvir und Sofosbuvir aus der RNA entfernt, jedoch langsamer als normale Nukleotide. In zellfreien Reaktionen blockierten beide Analoga die weitere RNA-Synthese stark — doch als eine aktive ExoN hinzugefügt wurde, wurde ein erheblicher Anteil der gestoppten RNA-Ketten gerettet und verlängert. Ein inaktiver ExoN-Mutant konnte dies nicht leisten, was bestätigte, dass die Korrekturlese-Aktivität größtenteils für das Rückgängigmachen der Wirkung der Medikamente verantwortlich ist. Die Anwesenheit der Polymerase zusammen mit ExoN beschleunigte tatsächlich die Entfernung der Analoga, was darauf hindeutet, dass die beiden viralen Enzyme zusammenarbeiten, um Hindernisse zu beseitigen und die Replikation aufrechtzuerhalten.
Den Korrekturleser in atomarer Auflösung beobachten
Um zu verstehen, wie ExoN diese Wirkstoffe erkennt und darauf reagiert, verwendete das Team hochauflösende Kryo-Elektronenmikroskopie, um Strukturen des ExoN-Komplexes gebunden an RNA-Stränge zu lösen, die entweder in Bemnifosbuvir oder Sofosbuvir enden. Diese Strukturen, scharf genug, um einzelne chemische Gruppen zu erkennen, zeigten, dass der modifizierte Zucker in jedem Wirkstoff in eine hydrophobe Tasche passt, die von einer kurzen Schleife des ExoN-Proteins gebildet wird. Diese zusätzliche enge Passung erklärt die stärkere Bindung der wirkstoffhaltigen RNA an ExoN. Sie hat aber auch einen unerwarteten Nebeneffekt: Indem sie an dieser Schleife zieht, stören die Wirkstoffe die präzise Anordnung einer benachbarten katalytischen Schleife, die eine wichtige Histidin-Restgruppe an Ort und Stelle hält. Wenn dieses Histidin vom Schnittzentrum wegschwingt, wird das aktive Zentrum von ExoN teilweise deaktiviert, was die Entfernung des Analogs verlangsamt, aber nicht vollständig verhindert.
Ein eingebauter Schalter, der das virale Korrekturlesen abstimmt
Mutationen einzelner Aminosäuren innerhalb der empfindlichen Schleife bestätigten ihre Bedeutung. Änderungen an vier konservierten Resten reduzierten ExoNs Fähigkeit stark, sowohl normale RNA-Enden als auch wirkstoffterminierte Enden zu schneiden, und veränderten auch, welches Endnukleotid ExoN bevorzugt entfernt. Das identifiziert die Schleife als allosterischen Regulator — einen eingebauten mechanischen Schalter, der wahrnimmt, welche Art von Nukleotid an der RNA-Spitze sitzt, und die Aktivität des Enzyms anpasst. Die Strukturen zeigen weiter, dass ExoN verschiedene Basen (A, U, C oder G) durch flexible Wasserstoffbrücken erkennt, allerdings fällt es ihm am schwersten, guaninähnliche Basen zu akzeptieren, was relevant ist, weil Bemnifosbuvir Guanosin nachahmt.
Was das für zukünftige COVID-19-Pillen bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft: SARS-CoV-2 verfügt über einen ausgeklügelten „Rechtschreibprüfer“, der bestimmte Medikamente nachträglich aus seinem Genom entfernen kann, nachdem diese ihre Wirkung des Replikationsstopps entfaltet haben. Bemnifosbuvir und Sofosbuvir schwächen zwar die Kopiermaschine des Virus, lenken die RNA aber gleichzeitig zum Korrekturleser, der ihre Wirkung teilweise rückgängig machen kann. Indem diese Arbeit genau zeigt, wie der virale Korrekturleser diese Wirkstoffe greift und wie eine winzige Regulationsschleife das Enzym zwischen aktiven und weniger aktiven Zuständen umschaltet, liefert sie einen Fahrplan für das Design neuer antiviraler Nukleotide, die entweder schlecht an ExoN binden, es in eine inaktive Konformation verriegeln oder dessen Schwierigkeit ausnutzen, mit guaninähnlichen Strukturen umzugehen. Solche Next‑Generation-Moleküle könnten für das Virus wesentlich schwerer zu „tilgen“ sein und so unsere Fähigkeit verbessern, COVID-19 und künftige Coronavirus-Ausbrüche zu behandeln.
Zitation: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Schlüsselwörter: SARS-CoV-2, antivirale Resistenz, Nukleotidanaloga, RNA-Korrekturlesen, Coronavirus-Replikation