Clear Sky Science · de
Lewis‑Säure‑induziertes Hydroxyl‑Spillover ermöglicht selektive elektrochemische Urea‑Oxidation zu Nitrit bei gleichzeitiger energieeinsparender Wasserstofferzeugung
Aus Abfall nützliche Chemikalien und sauberen Brennstoff machen
Urea ist vor allem als Bestandteil von Urin und Dünger bekannt, stellt in Abwässern jedoch einen hartnäckigen Schadstoff dar. Diese Studie zeigt, wie Urea von einer Last in eine Ressource verwandelt werden kann: Mit einem intelligent gestalteten Katalysator wandeln die Autoren Urea in Nitrit um, eine wertvolle Chemikalie für Dünger und Pharmazeutika, und erzeugen gleichzeitig Wasserstoff‑Brennstoff unter geringerem Energieaufwand als bei herkömmlicher Wasserelektrolyse. Die Arbeit skizziert mögliche künftige Kläranlagen, die Wasser reinigen, nützliche Produkte herstellen und saubere Energie zugleich liefern.
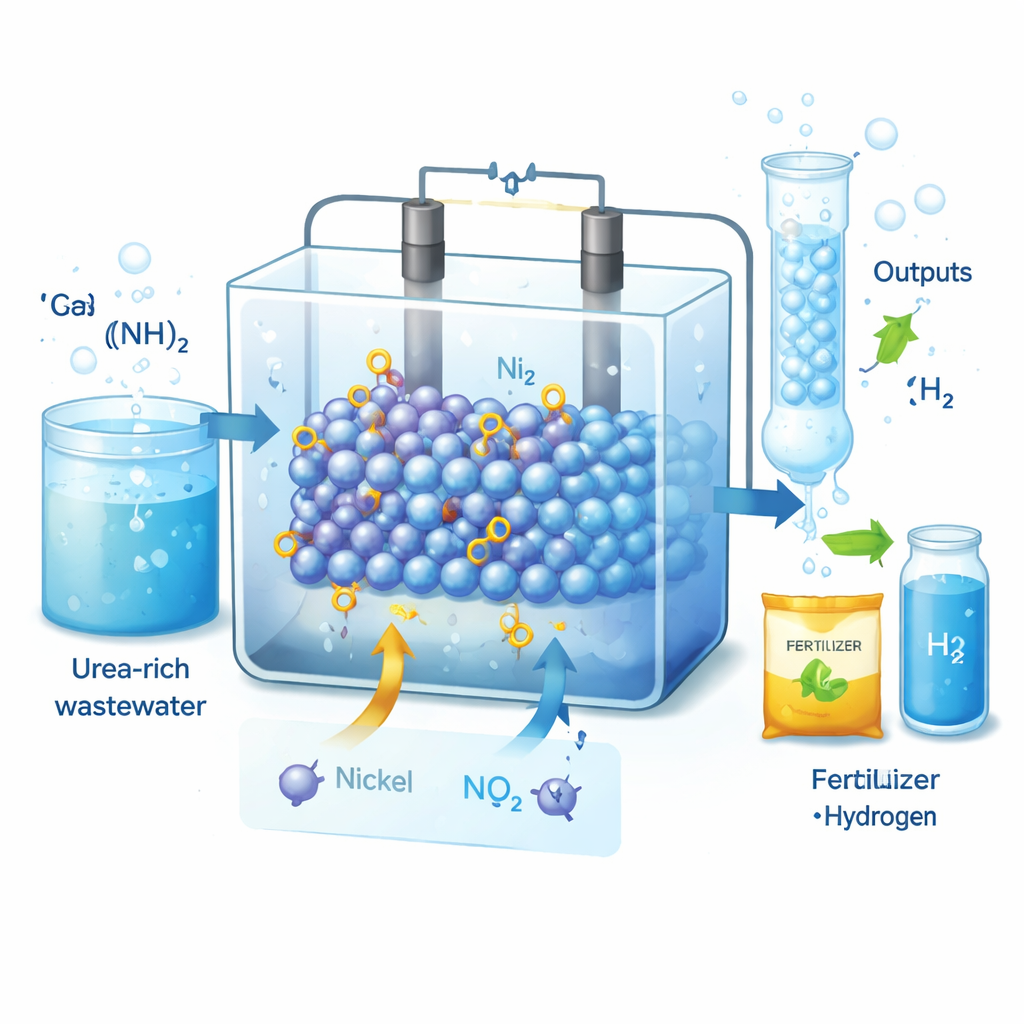
Warum Nitrit und Wasserstoff wichtig sind
Nitrit ist ein zentraler Baustein in Landwirtschaft, Lebensmittelkonservierung und Pharmazie; die weltweite Nachfrage liegt im Bereich von Millionen Tonnen pro Jahr. Heute wird Nitrit hauptsächlich im Ostwald‑Verfahren hergestellt, das bei hohen Temperaturen läuft, viel Energie verbraucht und stickstoffhaltige Oxide freisetzt. Zugleich enthalten Haushalts‑ und Industrieabwässer große Mengen Urea und machen 70–80 % der stickstoffhaltigen Schadstoffe aus. Wenn dieses Urea elektrochemisch zu Nitrit aufgewertet werden könnte und dabei Wasserstoffgas erzeugt, ließen sich sowohl Wasser reinigen als auch zwei hochpreisige Produkte liefern — vorausgesetzt, Prozess und Selektivität sind ausreichend effizient.
Reaktionen auf den richtigen Pfad lenken
Bei der Oxidation von Urea in alkalischer Lösung sind zwei Hauptwege möglich. Der eine führt zu unschädlichem Stickstoffgas und Kohlendioxid; der andere, wünschenswertere Weg liefert Nitrit und Nitrat, die als Chemikalien verkaufbar sind. Das Problem ist, dass die meisten nickelbasierten Katalysatoren, die bei dieser Reaktion eingesetzt werden, nicht sehr wählerisch sind — sie erzeugen meist eine Produktmischung und verschwenden Energie, indem sie die Sauerstoffentwicklungsreaktion antreiben, die nur Sauerstoffgas produziert. Die Autoren verfolgten deshalb das Ziel, die Katalysatoroberfläche so zu modifizieren, dass Hydroxidionen (die reaktiven OH⁻‑Spezies in alkalischem Medium) konzentriert und gelenkt werden, um bevorzugt C–N‑Bindungen zu knacken und Nitrit zu bilden, statt Stickstoffatome zu N₂ zu koppeln.
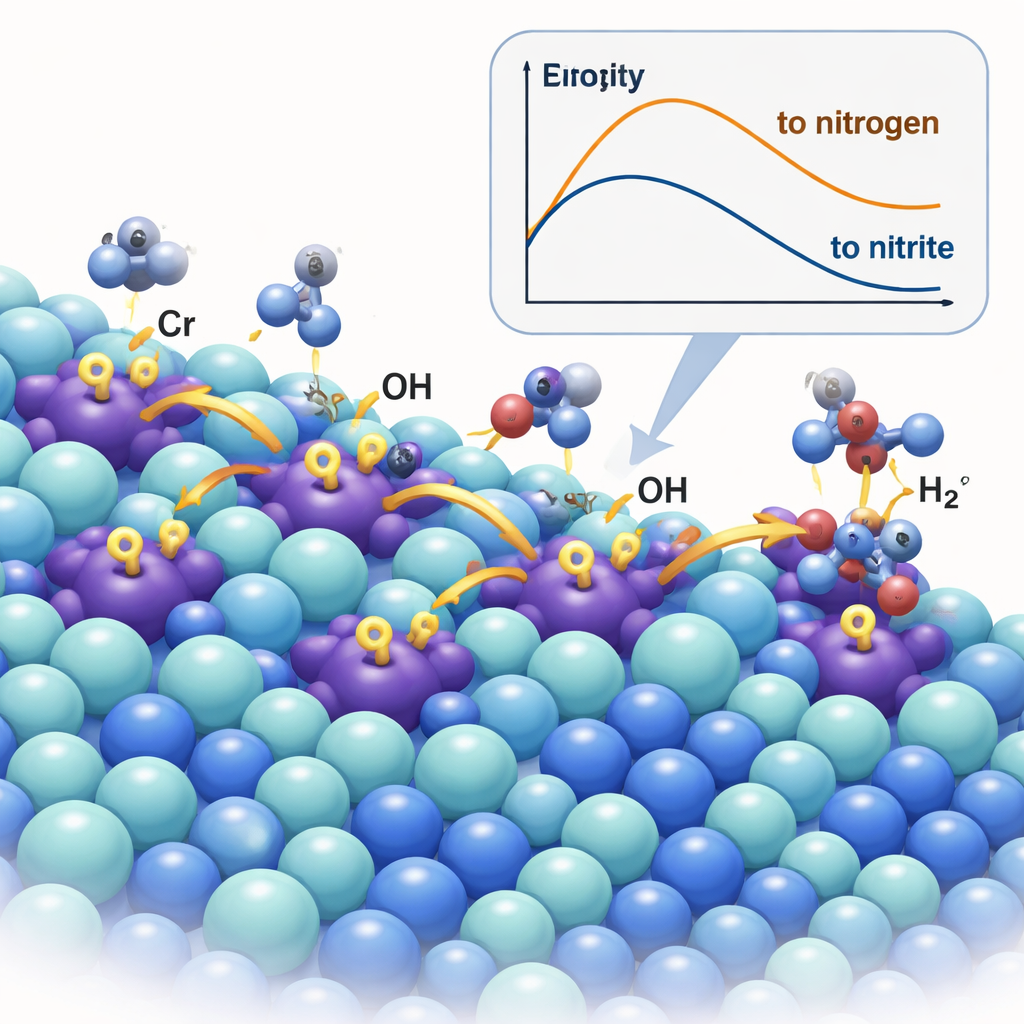
Ein Katalysator, der reaktive Spezies pumpt
Das Team entwickelte ein neues Material, indem es Nickelsulfid (Ni₃S₂) mit einer kleinen Menge Chrom dotierte und so Cr–Ni₃S₂ bildete. Chromionen fungieren als sogenannte Lewis‑Säure‑Stellen — elektronenarme Zentren, die Hydroxidionen stark anziehen. Mittels hochauflösender Mikroskopie, Röntgentechniken und Spektroskopie bestätigten die Forschenden, dass die Chromatome im Nickelsulfidgitter sitzen und dieses leicht schrumpfen und verzerren, wodurch sich die Elektronenverteilung ändert. Unter Reaktionsbedingungen wirken die Chromstellen wie winzige Pumpen: Sie fangen OH⁻ ein und „spillovern“ es auf benachbarte Nickelstellen, wo die eigentliche Urea‑Oxidation stattfindet. In situ‑Raman‑ und Infrarotmessungen sowie Isotopenmarkierungs‑Experimente verfolgten dieses Hydroxyl‑Spillover direkt von Cr zu Ni und zeigten, dass es die Bildung aktiver Nickeloxyhydroxid‑(NiOOH)‑Stellen beschleunigt, die die gewünschte Chemie antreiben.
Hohe Ausbeuten, geringerer Energiebedarf und gute Stabilität
Da OH⁻ effizient an die richtigen Orte geliefert wird, wandelt der Cr–Ni₃S₂‑Katalysator Urea mit beeindruckender Selektivität in Nitrit um. Bei industrierelevanten Stromdichten erreicht er eine Nitritproduktion von etwa 121 Milligramm pro Stunde und Quadratzentimeter bei Faraday‑Wirkungsgraden für Nitrit über 80 %, während die konkurrierende Sauerstoffentwicklung unter 1,5 % bleibt. Der Katalysator ist über Hunderte Stunden kontinuierlichen Betriebs stabil, mit vernachlässigbarer Chromauslaugung. Dasselbe Material senkt auch deutlich die benötigte Spannung, wenn es mit einer wasserstofferzeugenden Kathode in einem Urea‑unterstützten Wasseraufspaltungsgerät kombiniert wird, und reduziert die Stromkosten der Wasserstofferzeugung auf rund 3,7 Kilowattstunden pro Kubikmeter H₂ — weniger als bei konventioneller alkalischer Elektrolyse. Techno‑ökonomische Analysen deuten darauf hin, dass bei 400 Milliampere pro Quadratzentimeter die Verarbeitung einer Tonne Urea in diesem System einen Nettowert in der Größenordnung von etwa 1.200 US‑Dollar liefern könnte, wenn sowohl Nitrit als auch Wasserstoff mitgerechnet werden.
Von der Laborzelle zu praktischen Energiesystemen
Um das reale Potenzial zu demonstrieren, bauten die Autoren eine Durchflusszelle für kontinuierliche Urea‑unterstützte Wasserspaltung und eine Zn–Urea–Luft‑Batterie. In der Batterie führte der Ersatz der üblichen Sauerstoffentwicklungsreaktion beim Laden durch die Urea‑Oxidation zu einer Reduktion der Ladespannung um fast 0,3 Volt bei gleichzeitig stabiler Leistung über mehr als 100 Stunden. Das bedeutet, dass das Gerät sowohl Urea‑haltige Ströme reinigen als auch eine effizientere Stromspeicherung liefern kann. Die gleiche Lewis‑Säure‑Designstrategie funktionierte auch mit anderen Metallen wie Zinn und Titan oder einem anderen Wirtsmaterial wie Kupfersulfid, was darauf hindeutet, dass der Ansatz breit anwendbar ist.
Eine einfache Idee hinter einer komplexen Reaktion
Für Nicht‑Fachleute besteht die Kernidee darin, dass die Forschenden gelernt haben, wo und wie ein verbreiteter reaktiver Baustein — Hydroxid — auf einer Katalysatoroberfläche landet und sich bewegt. Durch das Einbringen von Chromstellen, die als starke Anziehungspunkte und Relais für OH⁻ wirken, erleichtern sie es, Urea‑Moleküle in Nitrit zu zerschneiden, statt sie vollständig zu N₂ zu verbrennen. Gleichzeitig erfordert dieser Weg weniger elektrische Energie und erzeugt von Natur aus Wasserstoff. Im Kern zeigt die Arbeit, dass eine sorgfältige atomare Gestaltung von Katalysator‑„Verkehrsführungen“ Abwasser in eine Quelle für sowohl Chemikalien als auch saubere Energie verwandeln kann.
Zitation: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Schlüsselwörter: Urea‑Oxidation, Nitrit‑Produktion, Wasserstofferzeugung, Elektrokatalyse, Abwasser‑Veredelung