Clear Sky Science · de
Mischprotokolle bestimmen die Dynamik der Flüssig‑Flüssig‑Phasentrennung bei polyelektrolytischen Komplex‑Coacervaten
Warum es wichtig ist, wie wir mischen
Viele der wichtigsten Tröpfchen in der Natur bestehen nicht aus Öl und Wasser, sondern aus geladenen Polymeren, die in Wasser gelöst sind. Diese flüssigen „Coacervate“ helfen Zellen, ihre Inhalte zu organisieren, und ermöglichen es Meerestieren wie Muscheln und Sandcastle‑Würmern, sich an nassen Felsen festzukleben. Die Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wenn man mit denselben Zutaten startet, sie aber auf unterschiedliche Weise mischt, wie sehr verändert das die Geschwindigkeit und das gleichmäßige Entstehen dieser Tröpfchen?
Tröpfchen, geboren aus geladenen Polymeren
Die Arbeit konzentriert sich auf Coacervate, die entstehen, wenn positiv und negativ geladene Polymerketten in Wasser aufeinandertreffen. Wie Magneten ziehen sich entgegengesetzte Ladungen an und ziehen die Ketten in eine dichte Flüssigphase, während die umgebende Lösung verdünnter bleibt. Diese Flüssig‑Flüssig‑Trennung ähnelt dem Zusammenziehen von Öl in Wasser, hier ist jedoch alles wasserbasiert und stark geladen. Solche polymerreichen Tröpfchen werden als Grundlage für „membranfreiere Organellen“ in Zellen und für schnell aushärtende Unterwasser‑Klebstoffe von Meeresorganismen angesehen. Während der Endzustand dieser Tröpfchen bereits ausführlich untersucht wurde, sind die Schritt‑für‑Schritt‑Abläufe — die Dynamik ihres Entstehens und Wachstums — weit weniger klar geblieben.
Drei Startarten, drei sehr unterschiedliche Wege
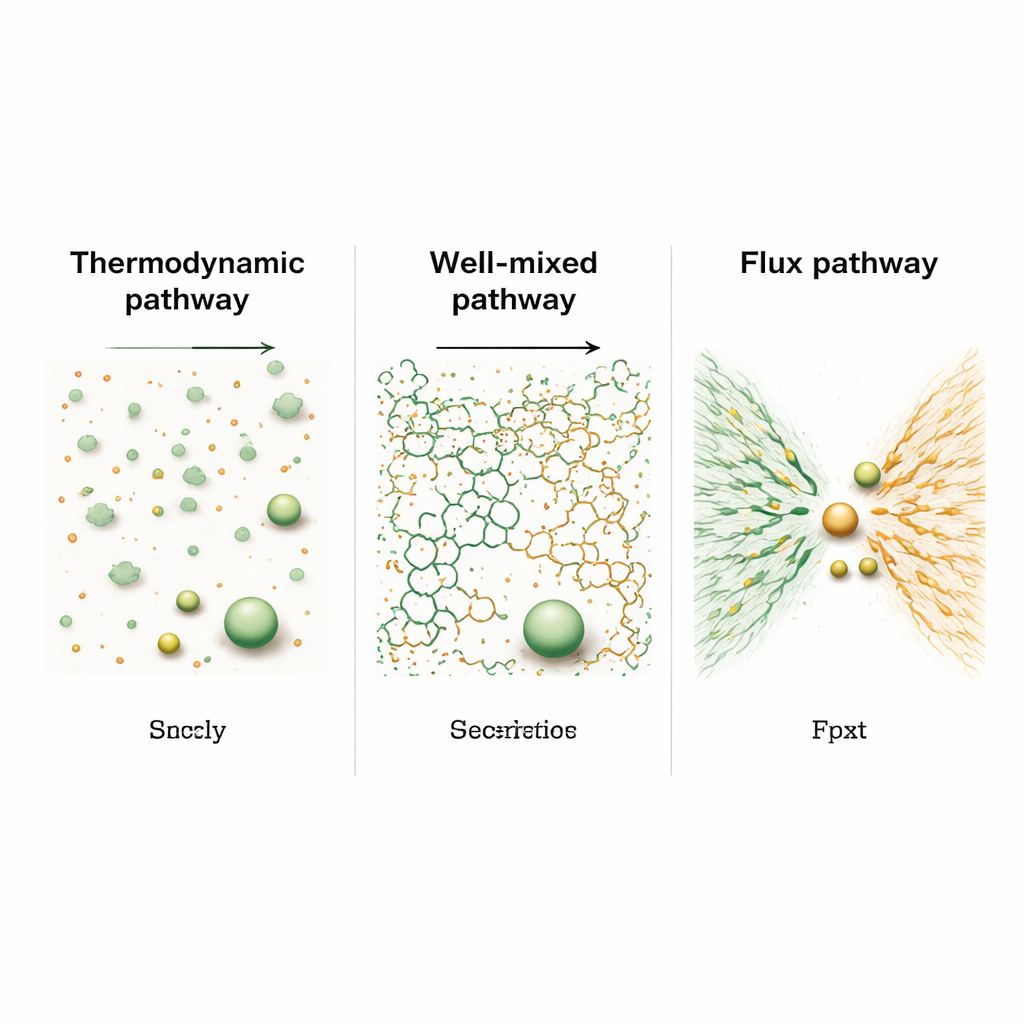
Mithilfe großmaßstäblicher molekularer Simulationen, die sowohl elektrische Kräfte als auch Fluidströmungen berücksichtigen, verglichen die Autorinnen und Autoren drei idealisierte Startwege des Systems. Im „thermodynamischen“ Pfad beginnen die Polymerketten als viele kleine, bereits gepaarte Cluster, die im gesamten Medium verteilt sind. Diese Cluster verschmelzen langsam wie zusammenlaufende Regentropfen, und die durchschnittliche Tröpfchengröße wächst mit der Zeit nach einem klassischen, relativ langsamen Gesetz (proportional zur Zeit hoch ein Drittel). Wenn hingegen die Polymere zu Beginn homogen bei hoher Konzentration verrührt sind — der „gut gemischte“ Pfad — bilden sie zuerst ein schwammartiges Netzwerk, das das System überspannt, bevor es in größere Tröpfchen kollabiert. Ein dritter,„Fluss“‑Pfad ahmt das Verhalten von Muscheln und Sandcastle‑Würmern nach: positiv und negativ geladene Polymere starten in getrennten Bereichen und werden dann so in eine gemeinsame Zone getrieben, wo Tröpfchen nahezu explosionsartig erscheinen.
Netzwerke, Strömungen und ultraschnelles Wachstum
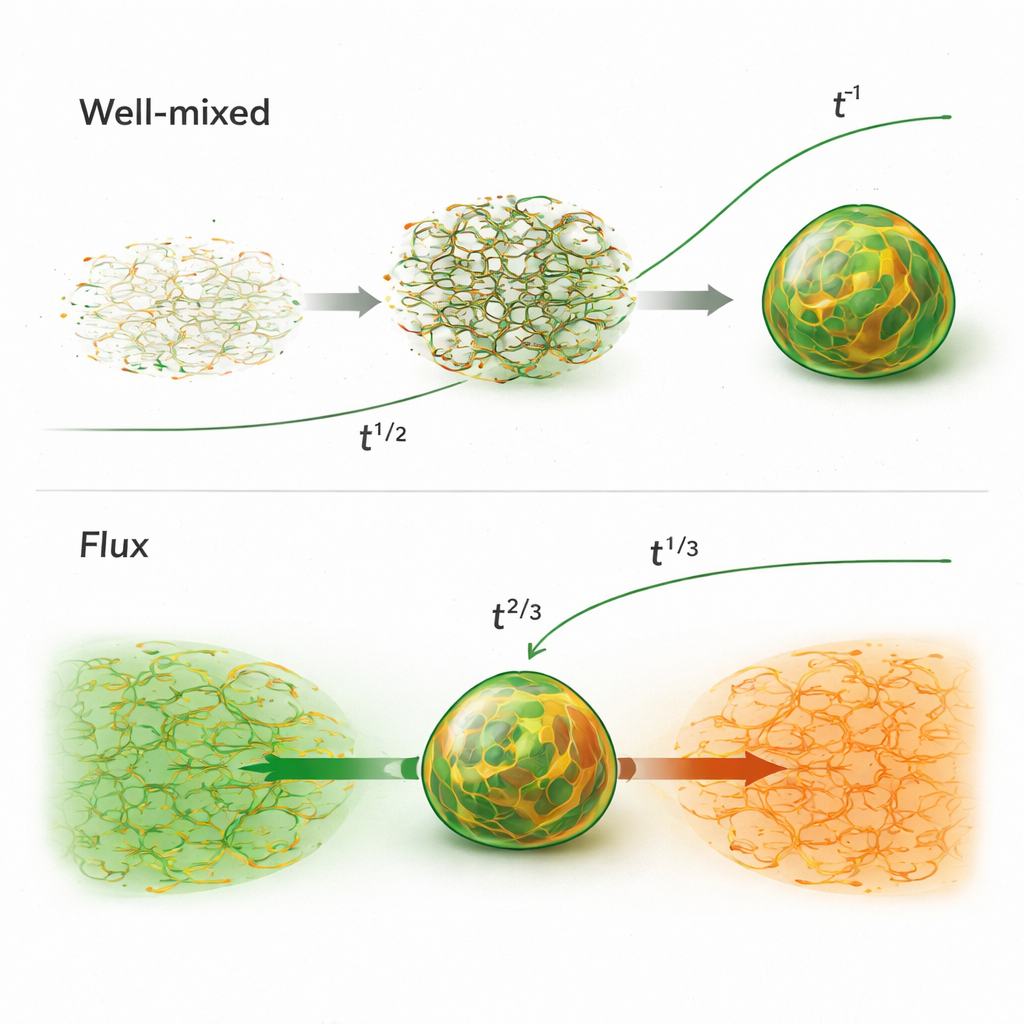
Diese Anfangsbedingungen führen zu auffallend unterschiedlichen Wachstumsgeschwindigkeiten. Im gut gemischten Fall erlaubt das frühe schwammartige Netzwerk einen effizienten Materialtransport über verbundene Pfade, sodass die Tröpfchen etwa so schnell wachsen wie die Quadratwurzel der Zeit — merklich schneller als der klassische Verschmelzungsweg. Je nachdem, wie gleichmäßig die Ladungen anfangs verteilt sind, bricht dieses Netzwerk später entweder in viele Tröpfchen auseinander, die dann auf die übliche langsame Weise zusammenschrumpfen, oder es bleibt verbunden und pumpt Fluid so effektiv, dass die Tröpfchengröße nahezu linear mit der Zeit anwächst. Im Fluss‑Pfad, wo zwei geladene Polymerdomänen aufeinanderrasen, ist das frühe Wachstum noch schneller und folgt einer Zeitpotenz von zwei Dritteln. Dieser Wachstums‑Schub wird durch ein starkes elektrisches und Konzentrationsungleichgewicht angetrieben, das Material zur Grenzfläche zieht, ähnlich wie Wasser, das talwärts unter Schwerkraft fließt.
Was das Tempolimit bestimmt
Die Simulationen zeigen, dass sowohl die Gesamt‑Konzentration als auch das lokale Ladungs‑Gleichgewicht wie Einstellknöpfe wirken, die den Pfad der Phasentrennung steuern. Bei hohen Polymerkonzentrationen bildet sich ein transientes Netzwerk, das das frühe Wachstum beschleunigt; bei geringeren Konzentrationen bilden die Polymere hingegen verstreute Tröpfchen und das Wachstum verlangsamt sich. Wenn positive und negative Ladungen in jeder lokalen Region gut ausbalanciert sind, bleiben die verbundenen Strukturen intakt und können Strömungen lenken, die das Zusammenwachsen dramatisch beschleunigen. Bei unausgewogener Ladungsverteilung fragmentiert das Netzwerk und das System kehrt zu langsamerem, tröpfchenweiser Wachstum zurück. In allen Fällen erreicht das System bei genügend langer Zeit einen ähnlichen Endzustand: ein großer, weicher Coacervat‑Tröpfchen, umgeben von einer verdünnten Phase.
Folgen von der Zelle bis zum Unterwasserkleber
Für Nicht‑Fachleute lautet die zentrale Botschaft: „Wie man startet“ kann die Frage „Wie schnell man ankommt“ um mehrere Größenordnungen verändern — selbst wenn das Endmaterial gleich aussieht. Unter biologisch inspirierter Mischführung können Tröpfchen, deren Assemblierung über den langsamen klassischen Weg Jahrzehnte dauern würde, stattdessen in Sekunden entstehen. Das hilft zu erklären, wie Zellen interne Tröpfchen schnell aufbauen und umgestalten und wie Meeresorganismen auf Abruf starke Unterwasserklebstoffe erzeugen. Es legt auch praktische Gestaltungsprinzipien für Technologien nahe: Durch die Wahl des richtigen Mischprotokolls könnten Ingenieurinnen und Ingenieure intelligente Materialien, Wirkstoff‑Freisetzungssysteme oder bioinspirierte Klebstoffe so entwickeln, dass sie schnell und zuverlässig anspringen — allein durch die Kontrolle, wie und wo die geladenen Polymerbestandteile zuerst aufeinandertreffen.
Zitation: Wu, Z., Wang, ZG. & Chen, S. Mixing protocols determine liquid–liquid phase separation dynamics in polyelectrolyte complex coacervation. Nat Commun 17, 1580 (2026). https://doi.org/10.1038/s41467-026-68296-5
Schlüsselwörter: polyelektrolytische Coacervate, Flüssig‑Flüssig‑Phasentrennung, biomolekulare Kondensate, Unterwasser‑Klebstoffe, Mischdynamik