Clear Sky Science · de
Stressvesikel verbinden epidermale Mechanotransduktion mit der Differenzierung von Stammzellen
Warum die verborgene Stressantwort der Haut wichtig ist
Jedes Mal, wenn Sie in Ihren Arm kneifen, sich beim Sport dehnen oder sogar auf einem zerknitterten Kissen schlafen, nimmt Ihre Haut diese mechanische Belastung stillschweigend auf. Meistens federt sie ohne Spuren zurück. Diese Studie legt ein überraschendes, verborgenes System offen, das den epidermalen Stammzellen hilft, diese physikalischen Kräfte wahrzunehmen und zu entscheiden, ob sie als Stammzellen bleiben oder zu ausgereiften Hautzellen werden. Das Verständnis dieses Systems könnte erklären, wie Haut zugleich robust und flexibel bleibt und warum bestimmte Krankheiten oder Fragilitätszustände der Haut entstehen.
Kleine Bläschen in belasteten Hautzellen
Mithilfe fortschrittlicher Live-Bildgebung bei Mäusen drückten, zogen oder saugten die Forscher an der Haut und beobachteten einzelne Zellen in Echtzeit. Sie fanden heraus, dass bei kurzzeitiger Krafteinwirkung Stammzellen im tiefsten Bereich der Epidermis schnell große innere Bläschen bildeten, die die Autor:innen „Stressvesikel“ nennen. Diese Vesikel füllten sich mit Flüssigkeit von außerhalb der Zelle und wuchsen über Sekunden bis Minuten, drückten gegen den Zellkern und verformten ihn, ohne die Zelle zum Platzen zu bringen. Wenn die Kraft entfernt wurde, schrumpften die meisten Vesikel und verschwanden innerhalb weniger Stunden, und die Kerne nahmen wieder ihre runde Form an. Das zeigt, dass es sich um eine reversible Reaktion und nicht um einen offensichtlichen Schaden handelt. 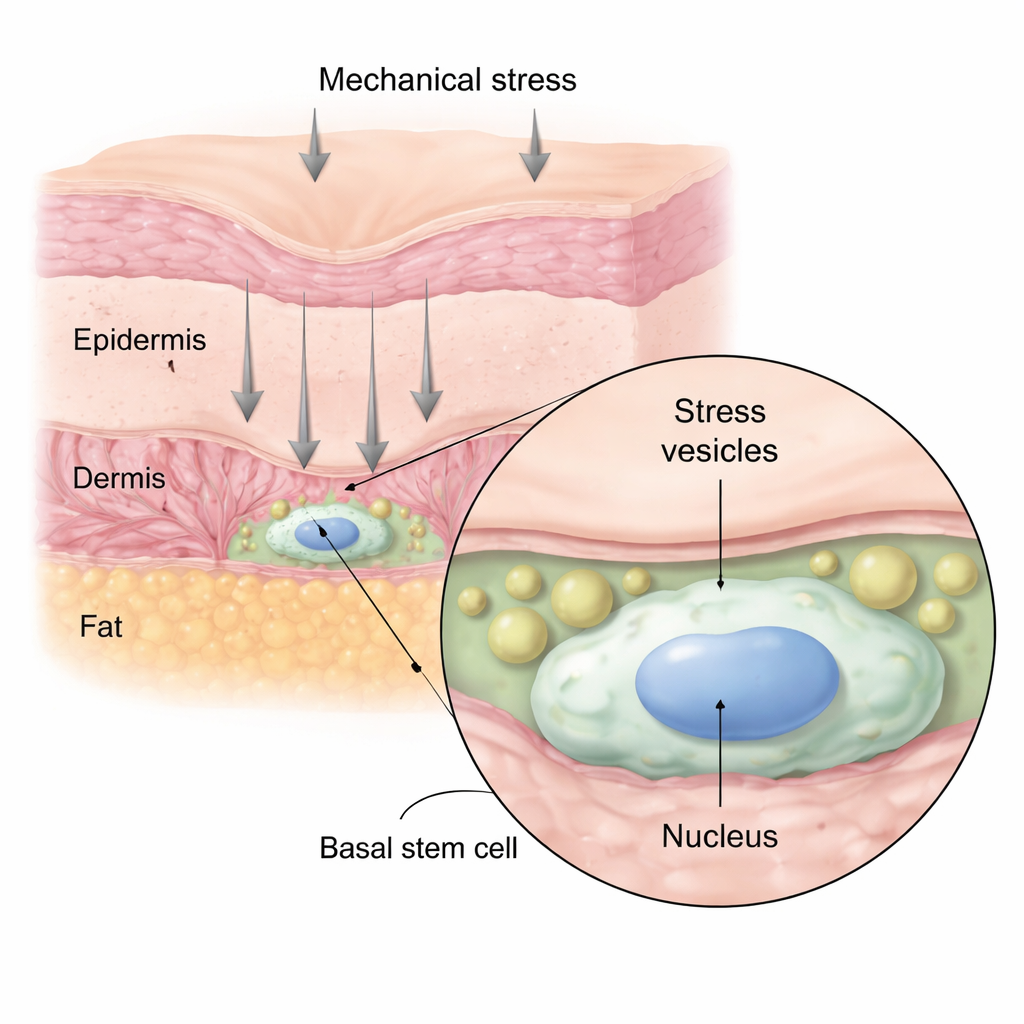
Vom mechanischen Druck zur Entscheidung über das Zellschicksal
Die Gruppe fragte dann, ob diese Stressvesikel nur eine strukturelle Besonderheit sind oder tatsächlich beeinflussen, was epidermale Stammzellen als Nächstes tun. Durch Markieren und Verfolgen einzelner Basalzellen über die Zeit zeigten sie, dass Zellen, deren Kerne stark durch Stressvesikel verformt wurden, eher dazu neigten, die Stammzellschicht zu verlassen und nach oben zu wandern, um zu reifen, nicht mehr teilenden Hautzellen zu werden. Zellen, die wenige oder keine Vesikel bildeten und deren Kerne kugelig blieben, blieben eher an Ort und Stelle, behielten Stammzell-Eigenschaften oder teilten sich. Interessanterweise traten Vesikel am häufigsten in Zellen auf, die bereits begonnen hatten, sich in Richtung Differenzierung zu bewegen, was darauf hindeutet, dass mechanischer Stress „schwankende“ Zellen weiter auf dem Weg zur vollständigen Reifung der Epidermiszellen vorantreiben kann.
Calcium-Signale und ein kraftsensitiver Kanal
Mechanische Kraft veränderte nicht nur die Gestalt der Zellen, sondern auch ihre Chemie. Mit einem fluoreszenten Calcium-Reporter beobachteten die Forscher unmittelbar nach Kompression eine Welle erhöhter Calciumwerte innerhalb der Epidermiszellen. In vielen Zellen war dieser Anstieg nur kurz, in anderen blieb Calcium länger erhöht — und genau diese Zellen hielten auch die Stressvesikel aufrecht. Das deutet auf eine enge Verbindung zwischen anhaltender Calcium-Erhöhung, Stabilität der Vesikel und einer Verschiebung in Richtung Differenzierung hin. Die Studie konzentrierte sich dann auf Piezo1, einen bekannten kraftempfindlichen Kanal in der Zellmembran, der auf Dehnung öffnet. Wurde Piezo1 gezielt aus Basalepidermiszellen entfernt, führte mechanischer Stress zu vermehrter Vesikelbildung, anormal hohen Calciumwerten und dazu, dass mehr Zellen nach oben wanderten und differenzierten. Die Aktivierung von Piezo1 mit einem kleinen Molekül hingegen förderte den kontrollierten Calciumeinstrom und verringerte tatsächlich die Vesikelbildung.
Eine konservierte Hautstrategie über Arten hinweg
Um zu prüfen, ob dieses Phänomen einzigartig für Maus-Haut ist, bauten die Forschenden menschliche Haut im Labor, verpflanzten sie auf Mäuse und verwendeten dieselbe Live-Bildgebung und mechanische Belastungsanordnung. Menschliche KERATINOZYTEN in diesen Transplantaten bildeten Stressvesikel, die den in Maus-Zellen beobachteten Vesikeln sehr ähnlich waren, einschließlich der damit verbundenen Kernverformung. Das legt nahe, dass Stressvesikel ein gemeinsames Merkmal der Säugetierhaut und kein Laborartefakt sind. Zusätzliche genetische und mikroskopische Analysen zeigten, dass bei fehlendem Piezo1 Gene, die an der Barrierefunktion und Zelladhäsion der Haut beteiligt sind, verändert waren und die Haut bei Belastung anfälliger für Blasenbildung wurde — ein Hinweis auf die schützende Rolle dieses Mechanosensormechanismus.
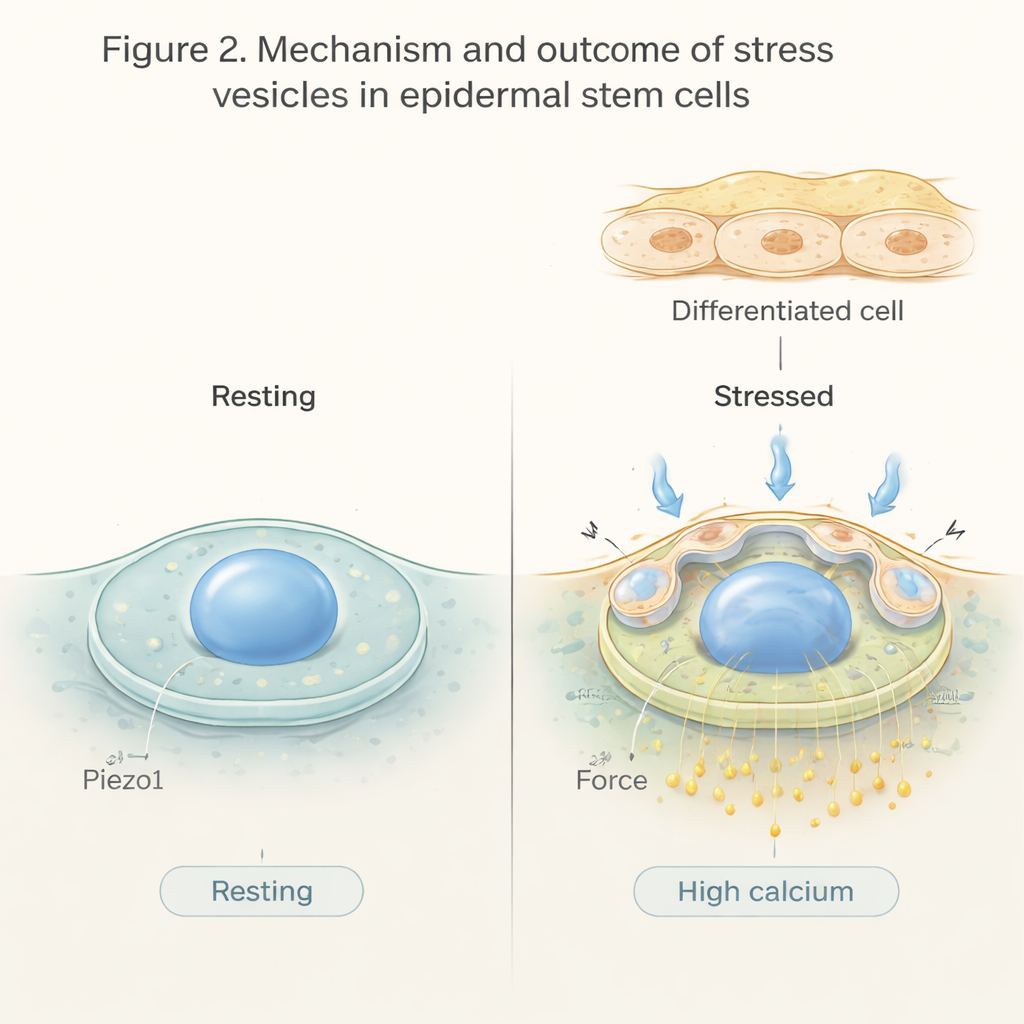
Was das für die alltägliche Hautgesundheit bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass epidermale Stammzellen Dehnung, Druck und Zug nicht bloß passiv ertragen — sie lesen diese Kräfte ab und reagieren, indem sie Flüssigkeit in Stressvesikel aufnehmen, ihre Kerne biegen, Calciumwerte ändern und in vielen Fällen die Entscheidung treffen, zu reifen und nach oben zu wandern. Der Piezo1-Kanal wirkt wie ein Sicherheitsventil, das bestimmt, wie stark und wie lange diese Calcium-Signale andauern, und übermäßige Vesikelbildung begrenzt. Zusammen helfen diese Mechanismen der Epidermis, sich kontrolliert zu erneuern und gleichzeitig unter mechanischer Belastung strukturell intakt zu bleiben. Künftig könnte das Ansteuern dieses Systems neue Wege eröffnen, um fragile Haut zu behandeln, die Wundheilung zu verbessern oder widerstandsfähigere Hautgewebe zu entwickeln.
Zitation: Huang, S., Kuri, P., Zou, J. et al. Stress vesicles link epidermal mechanotransduction to stem cell differentiation. Nat Commun 17, 1578 (2026). https://doi.org/10.1038/s41467-026-68294-7
Schlüsselwörter: Hautmechanik, epidermale Stammzellen, Calcium-Signalgebung, Piezo1-Kanal, Zelldifferenzierung