Clear Sky Science · de
Integriertes Multi-Omics-Atlas enthüllt die Hierarchie räumlich-zeitlicher Regulationsnetzwerke der Maus-Gastrulation
Wie ein Embryo seinen Körperplan aufbaut
Jeder Säuger, einschließlich des Menschen, beginnt das Leben als winzige Zellkugel, die sich rasch zu einem komplexen Körper mit Kopf, Schwanz, Rücken, Bauch und inneren Organen organisieren muss. Diese dramatische Umgestaltung findet in einem kurzen Zeitfenster statt, der Gastrulation genannt wird. Die hier zusammengefasste Studie erstellt eine detaillierte, mehrschichtige Karte dieses Prozesses in Maus-Embryonen und zeigt, wie Gene, DNA‑Schalter und chemische Signale räumlich und zeitlich zusammenwirken, um Zellen zu ihren künftigen Schicksalen zu führen.
Tausende von Zellen bei ihrer Entscheidungsfindung beobachten
Um die Gastrulation in Aktion zu verfolgen, analysierten die Forschenden über 35.000 einzelne Zellen aus Maus-Embryonen über fünf eng beieinanderliegende Stadien von früher bis später Gastrulation. Für jede Zelle maßen sie nicht nur, welche Gene aktiviert waren, sondern auch, welche DNA‑Regionen offen und zugänglich waren — ein Hinweis darauf, dass sie als regulatorische Schalter fungieren können. Anhand dieser Daten identifizierten sie 31 unterschiedliche Zelltypen und zeichneten nach, wie frühe, flexible Zellen sich schrittweise in die drei Keimblätter — Ektoderm, Mesoderm und Endoderm — verzweigen, die schließlich alle Gewebe und Organe bilden. Sie entwickelten außerdem eine neue rechnerische Methode, BioCRE, um Gene präziser mit den sie kontrollierenden DNA‑Elementen zu verbinden, und zeigten, dass viele wichtige Schalter weit von den Genen liegen, die sie regulieren.
Aufbau eines 3D‑molekularen Atlas im realen Embryoraum
Die meisten Einzelzellmethoden verlieren die ursprüngliche Position jeder Zelle im Embryo, doch der Ort ist entscheidend zum Verständnis der Musterbildung. Das Team umging dieses Problem, indem es seine Einzelzelldaten auf eine bereits bestehende dreidimensionale Karte der Genaktivität in Maus‑Embryonen ausrichtete. Das Ergebnis ist ST‑MAGIC, ein „digitaler Embryo“, in dem jeder winzige Ort mit den wahrscheinlichen Zelltypen, den von ihnen exprimierten Genen und der Zugänglichkeit der umliegenden DNA annotiert ist. Dieser Atlas zeigt zum Beispiel, wie verschiedene Mesoderm‑Subtypen — die künftiges Herz, Muskulatur und Stützgewebe bilden — in unterschiedlichen Regionen entstehen und wie weit verbreitet exprimierte Gene wie Otx2 auf der äußeren (Epiblast) und inneren (viszerales Endoderm) Embryonoberfläche unterschiedliche regulatorische Elemente nutzen.
Wenn Symmetrie bricht und links sich von rechts unterscheidet
Ein markantes Merkmal von Körperplänen ist, dass linke und rechte Seite nicht identisch sind — denken Sie an das leicht links sitzende Herz. Die Autorinnen und Autoren nutzten ihren spatialen Atlas, um in das laterale Mesoderm hineinzuzoomen, wo Links‑Rechts‑Unterschiede zuerst auftreten. Sie fanden subtile, aber konsistente Asymmetrien darin, welche Zelltypen auf jeder Seite angereichert sind und welche DNA‑Regionen stärker geöffnet sind. Auf der rechten Seite waren Regionen, die mit einem Wachstums‑Signalweg namens BMP verbunden sind, zugänglicher; auf der linken Seite dominierten Regionen, die mit Genen für Segmentbildung und Herzstrukturen assoziiert sind. Einige dieser DNA‑Elemente, einschließlich neu entdeckter Elemente, die das Gen Lefty2 steuern, öffnen sich bevor sichtbare Unterschiede in der Genexpression auftreten, was darauf hindeutet, dass eine frühe „Priming“ der Chromatinlandschaft jede Seite des Embryos darauf vorbereitet, Signale unterschiedlich zu interpretieren.
Eine Staffel von Faktoren führt die Mittellinie des Körpers
Die Studie konzentriert sich anschließend auf das axiale Mesendoderm, eine Zellpopulation, die die Chorda dorsalis (Notochord) bilden wird — eine stabförmige Struktur entlang der Mittellinie, die bei der Organisation der Wirbelsäule und des Nervensystems hilft. Mit ihren kombinierten Werkzeugen (ST‑MAGIC und einer erweiterten Version ST‑MAGIC (+)) verfolgten die Autorinnen und Autoren, wie diese Zellen aus dem anterioren primitiven Streifen entstehen und sich in zwei Zweige aufspalten: Knoten‑Zellen, die eine mit Zilien besetzte Struktur aufbauen, die für die Links‑Rechts‑Wahrnehmung wichtig ist, und anteriores Mesendoderm, das zu Mittellinien‑Geweben beiträgt. Sie entdeckten eine hierarchische Staffel von Transkriptionsfaktoren — Proteinen, die die Genaktivität steuern. Frühe Faktoren wie EOMES und intermediäre Faktoren einschließlich FOXA2 und LHX1 öffnen zunächst Schlüsselsektoren der DNA und etablieren die Antwortbereitschaft auf wichtige Signale wie WNT und NODAL. Später schalten „terminale“ Faktoren wie NOTO, SOX9 und ein neu implizierter Faktor POU6F1 spezialisierte Genprogramme an, zum Beispiel solche, die für Zilien oder die extrazelluläre Matrix benötigt werden.
Signale, Chromatin und spät wirkende Spezialisten
Durch die Integration öffentlicher Datensätze darüber, wo Effektoren der WNT‑ und NODAL‑Signalwege an die DNA binden, zeigten die Autorinnen und Autoren, dass die Reaktionsfähigkeit des Embryos auf diese Signale sich räumlich verschiebt, bevor sich die eigentlichen Signalquellen bewegen. In der Region, die zum axialen Mesendoderm bestimmt ist, öffnen sich DNA‑Stellen, die auf NODAL und WNT ansprechen, früh, und viele tragen Motive für FOXA2, Zfp281 und andere Regulatoren, was auf kooperative Kontrolle hindeutet. Experimentelle Deletionen der spät wirkenden Faktoren NOTO und POU6F1 in Mäusen störten die Expression knoten‑spezifischer und zilienbezogener Gene und verkürzten die Knoten‑Zilien, während die zugrundeliegende offene DNA‑Landschaft größtenteils intakt blieb. Das deutet darauf hin, dass frühere Faktoren das epigenetische Fundament legen, während späte Faktoren vor allem die Genexpression verfeinern, ohne das Chromatin grundlegend umzubauen.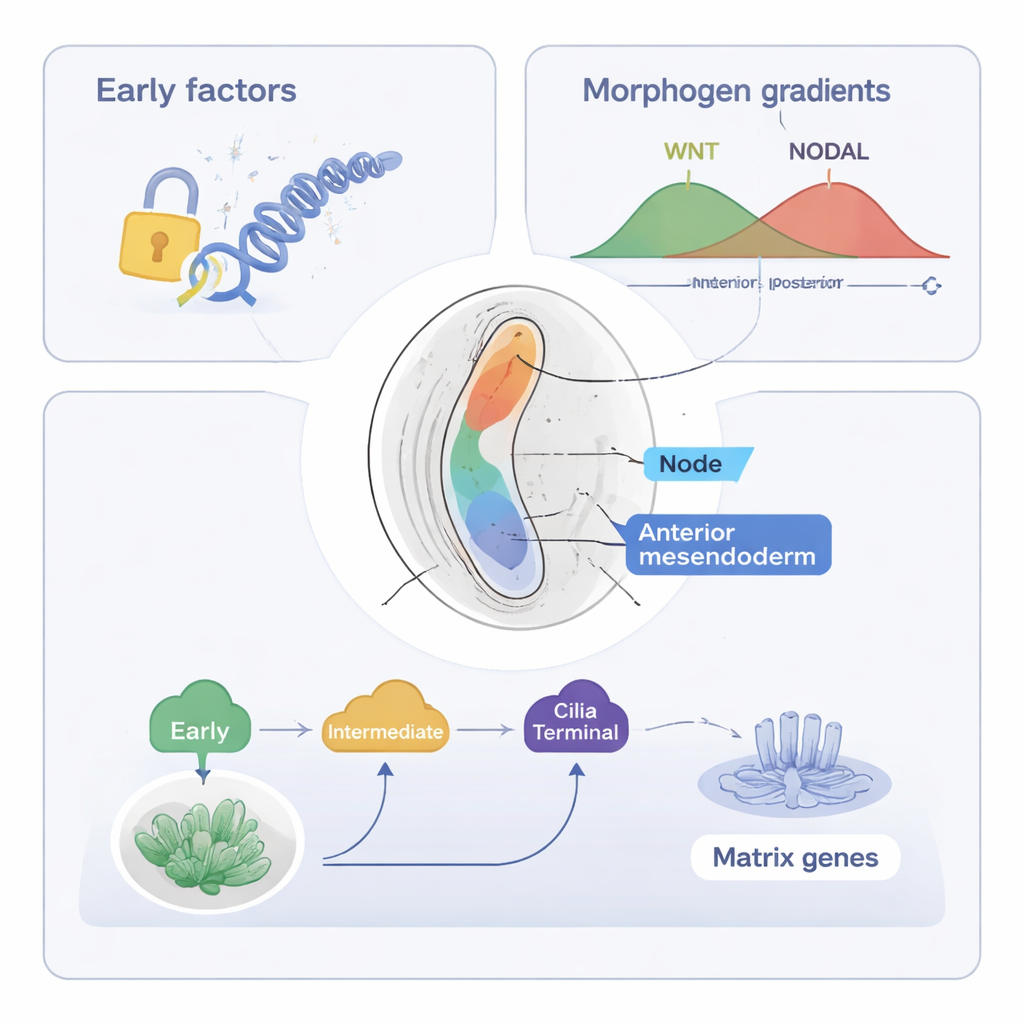
Warum das für das Verständnis der Entwicklung wichtig ist
Für Nichtfachleute lässt sich diese Arbeit als der Aufbau eines hochauflösenden „Schaltplans“ betrachten, wie ein Embryo seinen Körperplan anlegt. Die Autorinnen und Autoren zeigen, dass Zell‑Schicksalsentscheidungen während der Gastrulation nicht nur von den vorhandenen Signalen abhängen, sondern auch davon, wann und wo DNA‑Schalter geöffnet werden und welche Transkriptionsfaktoren in welcher Reihenfolge wirken. Ihre ST‑MAGIC und ST‑MAGIC (+) Atlanten bieten eine Ressource, um diese Beziehungen über Raum und Zeit zu erkunden, und liefern einen Rahmen, der Studien zu Geburtsfehlern, stammzellbasierten Embryomodellen und schließlich Aspekten der menschlichen Entwicklung informieren könnte.
Zitation: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Schlüsselwörter: Gastrulation, Genregulatorische Netzwerke, Einzelzell-Multi-Omics, Embryomusterung, Mausentwicklung