Clear Sky Science · de
HEXIM1-Intermonomer-Autoinhibition steuert die 7SK-RNA-Bindungsspezifität und die Inaktivierung von P-TEFb
Warum diese winzige RNA für die Genkontrolle wichtig ist
Jede Zelle muss entscheiden, wann Gene ein- oder ausgeschaltet werden, und sie tut dies, indem sie ein Enzym, das die RNA-Produktion antreibt, sorgfältig kontrolliert. Diese Arbeit zeigt, wie ein kleines Protein namens HEXIM1 gemeinsam mit einer nicht-kodierenden RNA namens 7SK wie eine Sicherung für dieses Enzym wirkt. Das Verständnis dieses molekularen Sicherheitssystems hilft zu erklären, wie Zellen übermäßige Genaktivität verhindern, und beleuchtet zugleich, wie Viren wie HIV dieselbe Maschinerie kapern.
Eine molekulare Bremse der Genexpression
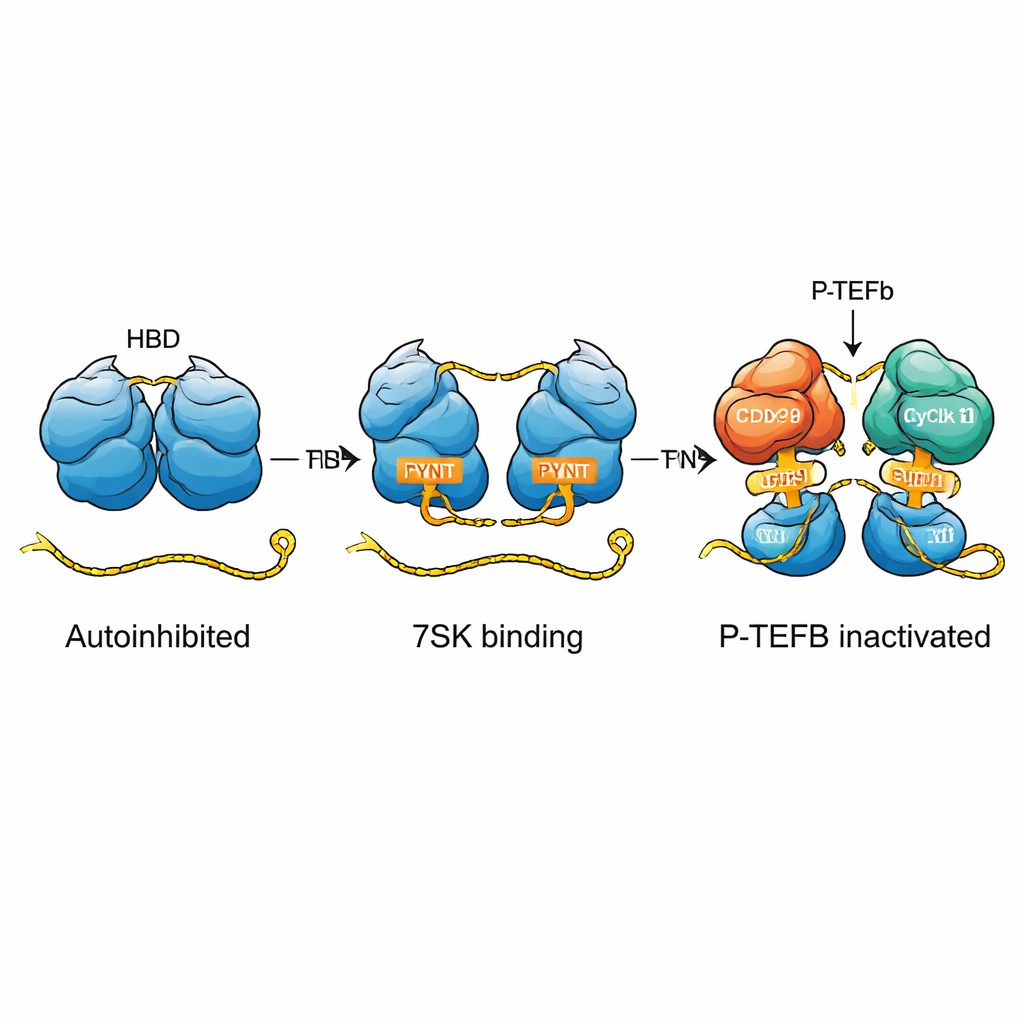
In menschlichen Zellen wird ein zentraler Schritt der Genexpression durch einen Faktor namens P-TEFb gesteuert, der der RNA-Polymerase II hilft, vom pausierten Zustand in die volle Transkription überzugehen. HEXIM-Proteine, insbesondere HEXIM1, spielen eine Schlüsselrolle dabei, P-TEFb in Schach zu halten. Sie tun dies innerhalb eines großen Komplexes, des 7SK-RNP, das um die 7SK-RNA aufgebaut ist. Wenn HEXIM1 und 7SK zusammenwirken, sperren sie P-TEFb so weg, dass es keine Transkription antreiben kann. Bisher fehlte jedoch die Erklärung, wie HEXIM1 selbst verhindert, P-TEFb zu früh zu binden, und wie die 7SK-RNA HEXIM1 zur aktiven Hemmung umschaltet.
Ein sich selbst umschlingendes Protein unter Kontrolle
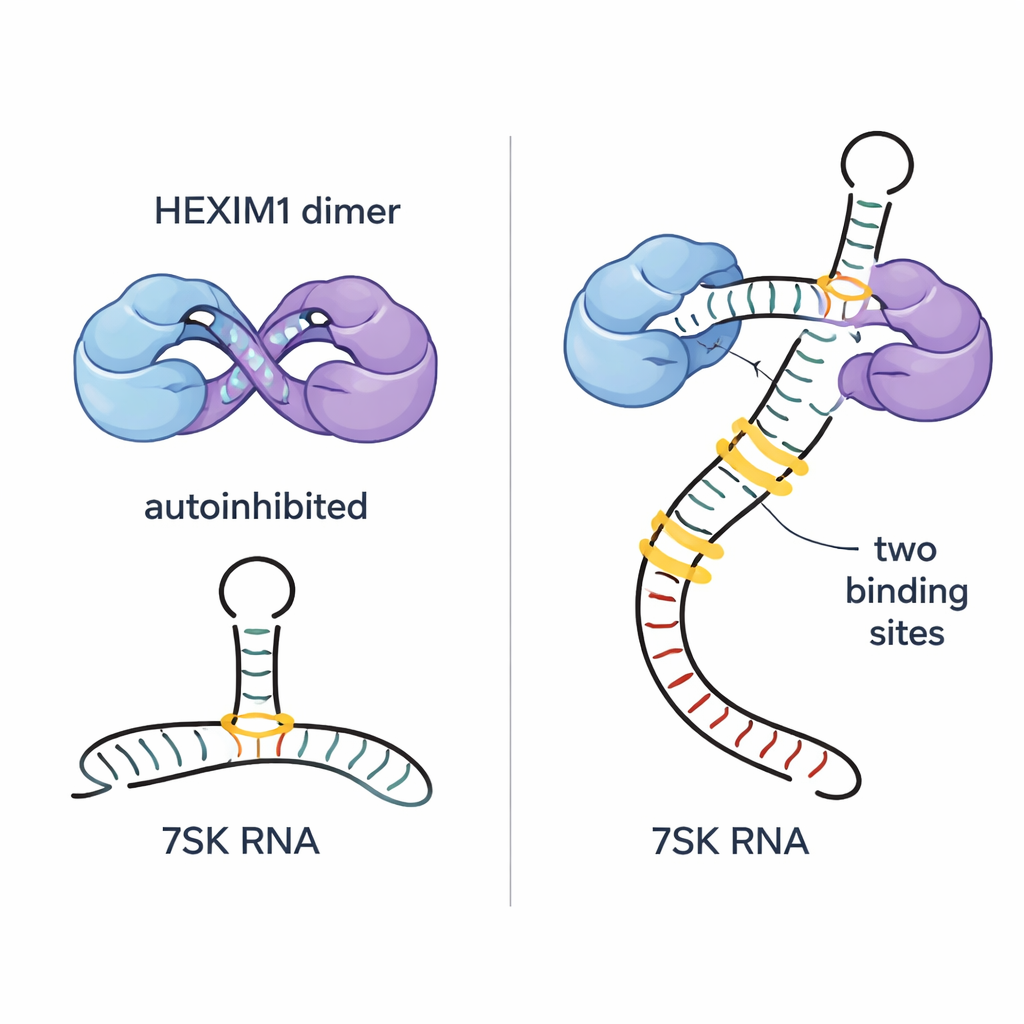
Die Autoren zeigen, dass HEXIM1 natürlicherweise ein Dimer bildet—zwei identische Proteinketten paaren sich—und dass die flexiblen zentralen Abschnitte jeder Kette einander in einer „Selbstumarmung“-Anordnung umschlingen. In diesem Zustand ist ein wichtiges kurzes Segment, das PYNT-Motiv, das normalerweise die P-TEFb-Kinase bindet und hemmt, an der Schnittstelle der beiden Ketten verborgen. Mithilfe empfindlicher NMR- und biophysikalischer Methoden kartierten die Forscher, wie basische (positiv geladene) und saure (negativ geladene) Regionen der beiden Monomere interagieren, um dieses autoinhibierte Dimer zu erzeugen. Diese eingebaute Zurückhaltung verhindert, dass HEXIM1 zufällig an P-TEFb klammert, wenn 7SK-RNA nicht vorhanden ist.
Wie 7SK-RNA HEXIM1 entriegelt
Die 7SK-RNA enthält mehrere strukturelle Merkmale, darunter eine lange Stamm-Schleifen-Region namens SL1. Durch Zerlegung dieser RNA in kleinere Fragmente und Verfolgen subtiler Änderungen in NMR-Signalen identifizierten die Forscher fünf mögliche HEXIM1-Bindungsstellen entlang von SL1. Zwei dieser Stellen heben sich als hochaffine Andockpunkte hervor; beide teilen einen A–U-reichen Doppelhelix-Abschnitt und eine nahegelegene U-reiche Ausbuchtung, die spezielle Dreibasenzuordnungen ausbilden kann. Das Team fand heraus, dass jede Hälfte des HEXIM1-Dimers an eine dieser beiden starken Stellen auf linearer 7SK-RNA bindet. Wenn beide Stellen besetzt sind, reorganisiert sich der zentrale Bereich von HEXIM1, die Selbstumarmungskontakte werden gelöst und die verborgenen PYNT-Motive freigelegt, wodurch das Protein bereit ist, P-TEFb zu erfassen.
Die richtige RNA-Form wählen — und die falschen vermeiden
7SK-RNA existiert nicht nur in einer Form; sie kann zwischen einer linearen Form, die beide Hochaffinitätsstellen präsentiert, und einer kreisähnlichen Form mit nur einer geeigneten Stelle wechseln. Die Autoren zeigen, dass HEXIM1 durch seine Autoinhibition überraschend wählerisch ist: Das Dimer bindet einzeln stehende Stellen nur schwach, aber deutlich stärker und kooperativ an das vollständige lineare SL1-Segment, das beide starken Stellen bietet. Diese Zwei-Stellen-Anforderung verhindert, dass HEXIM1 an beliebige RNAs im Zellinneren hängen bleibt, und macht seine Bindung sehr spezifisch für die lineare 7SK-Konformation, die den aktiven Repressionskomplex zusammenstellt. Sie zeigen außerdem, dass das Hinzufügen zusätzlicher negativer Ladungen in der Nähe der RNA-Bindungsregion (das eine Phosphorylierung an einer Schlüsselserin nachahmt) die RNABindung abschwächt, ohne die Autoinhibition vollständig zu zerstören — ein möglicher Mechanismus, mit dem Zellen P-TEFb bei Bedarf freisetzen können.
Vom molekularen Schalter zur zellulären Auswirkung
Insgesamt zeigt die Studie, dass HEXIM1 ein feinabgestimmter molekularer Schalter ist. In seinem ruhenden, selbstumarmenden Zustand hält es die P-TEFb-blockierenden PYNT-Segmente verborgen. Erst wenn es auf lineare 7SK-RNA mit zwei korrekt angeordneten Bindungsstellen trifft, klappt das Protein in einen „Ein“-Zustand auf, legt diese Segmente frei und kann so P-TEFb erfassen und inaktivieren—oft zwei Kopien gleichzeitig. Dieser Mechanismus erklärt, wie Zellen eine kleine RNA und ein flexibles Protein nutzen, um präzise Kontrolle über die Transkription auszuüben, und er bietet einen klareren Rahmen zum Verständnis, wie zelluläre Signale, chemische Modifikationen oder virale Proteine wie HIV Tat das Gleichgewicht zwischen pausierter und aktiver Genexpression verschieben können.
Zitation: Yang, Y., Murrali, M.G., Galvan, S. et al. HEXIM1 inter-monomer autoinhibition governs 7SK RNA binding specificity and P-TEFb inactivation. Nat Commun 17, 1570 (2026). https://doi.org/10.1038/s41467-026-68285-8
Schlüsselwörter: Transkriptionsregulation, 7SK-RNA, HEXIM1, P-TEFb, HIV Tat