Clear Sky Science · de
Viskoelastisches Hydrogel zur Aktivierung von CAR‑Makrophagen für die Behandlung der Lungenfibrose
Die Hausmeister des Körpers in präzise Reparaturteams verwandeln
Lungenfibrose ist eine verheerende Lungenerkrankung, bei der normales, elastisches Lungengewebe allmählich durch steife Narben ersetzt wird. Betroffene kämpfen ums Atmen, und die heutigen Medikamente verlangsamen meist nur den Krankheitsverlauf. Diese Studie untersucht eine neue Idee: die körpereigenen Aufräumzellen, Makrophagen, in gekapselte „intelligente Hausmeister“ umzuwandeln und ihre Wirksamkeit mit einem speziell entwickelten weichen Gel zu verstärken. Zusammen helfen diese Ansätze den Zellen, die Narbenbildner aufzuspüren und sogar das versteifte Gewebe in geschädigten Lungen aufzulockern.
Wenn Heilung schadet
In gesunden Lungen helfen Fibroblasten, das feine Netzwerk aus Kollagen zu erhalten, das die Lungenbläschen stützt. Bei Lungenfibrose werden diese Zellen überaktiv und legen dicke Kollagenfäden ab, die die Luftsäcke verengen. vorhandene Medikamente können diese Prozesse dämpfen, kehren sie aber selten um. Die Autoren konzentrieren sich auf ein Oberflächenmerkmal: das fibroblast‑aktivierende Protein (FAP), das auf überaktiven Fibroblasten reichlich vorkommt, in normalem Gewebe jedoch selten ist. Könnten Immunzellen darauf trainiert werden, FAP zu erkennen, könnten sie gezielt die „enthemmten“ Fibroblasten entfernen, die die Narbenbildung vorantreiben, und dabei gesunde Nachbarzellen verschonen.
Makrophagen umprogrammieren, damit sie Narbenbauer anvisieren
Makrophagen sind wandernde Immunzellen, die normalerweise tote Zellen, Mikroben und Zelltrümmer aufnehmen. Das Team stattete sie mit einem chimären Antigenrezeptor (CAR) aus, der FAP erkennt, und schuf so CAR‑Makrophagen (CAR‑Ms). Im Reagenzglas verschlangen diese CAR‑Ms effizient FAP‑reiche Fibroblasten und töteten sie, während sie Zellen mit reduziertem FAP weitgehend ignorierten. Sie bauten außerdem kollagenreiche Gele energischer ab als unveränderte Makrophagen, was einen doppelten Vorteil andeutet: die Eliminierung der Zellen, die Narben erzeugen, und der direkte Abbau der Narbenmatrix selbst. Diese Effekte zeigten sich sowohl in etablierten Zelllinien als auch in primären Mausmakrophagen, die der Situation im Gewebe näher kommen. 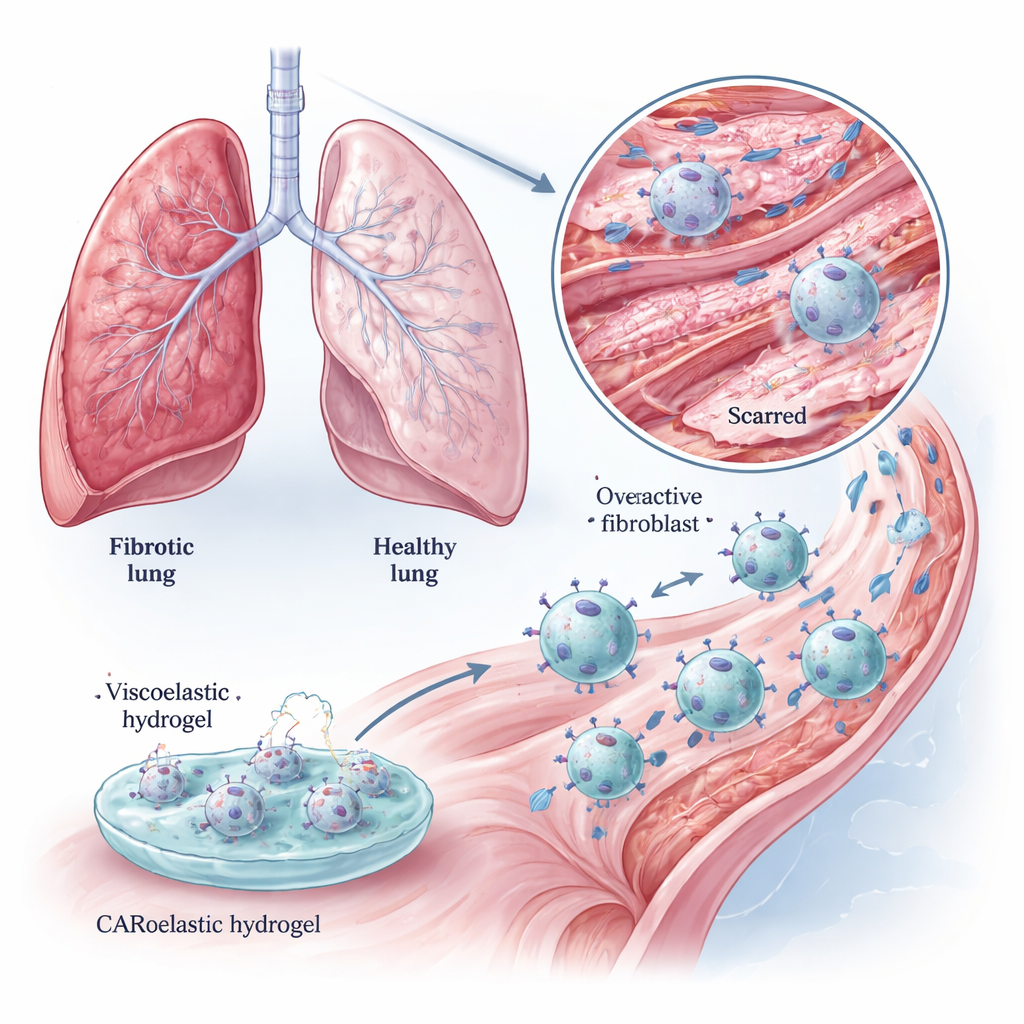
Immunzellen mit einem weichen, viskoelastischen Gel vorbehandeln
Genetische Modifikation von Zellen ist mächtig, aber komplex. Die Forscher fragten daher, ob ein rein physikalischer Reiz — ein weiches, viskoelastisches Hydrogel — das Verhalten der CAR‑Ms zusätzlich modulieren könnte. Sie entwickelten ein Gel aus Gelatine und Alginat, dessen „loss modulus“, ein Maß dafür, wie es unter Belastung langsam entspannt, fein einstellbar war, ohne die Gesamtsteifigkeit zu verändern. Wurden CAR‑Ms kurz auf Gelen mit der richtigen Viskoelastizität kultiviert, stieg ihre Fähigkeit, Ziel‑Fibroblasten zu töten, stärker als nach gängigen chemischen Stimuli, und der Effekt hielt mindestens zwei Tage an. Diese „Gel‑CAR‑Ms“ schalteten außerdem Gene ein, die mit Immunaktivierung und Gewebeumgestaltung verknüpft sind, während Gene, die mit Fibrose assoziiert sind, herunterreguliert wurden — ein Hinweis darauf, dass die Gel‑Erfahrung den Zellen eine stärker narbenbekämpfende Identität verlieh.
Wie eine weichere Oberfläche das Zellverhalten umprogrammiert
Um zu verstehen, warum das Gel wichtig war, untersuchten die Forscher den physikalischen Zustand der CAR‑Rezeptoren auf der Zelloberfläche. Eine fluoreszente Sonde zeigte, dass hydrogel‑vorbehandelte CAR‑Ms eine geringere Membranspannung hatten — die äußere „Haut“ der Zelle war entspannter. Unter diesen Bedingungen lösten sich CAR‑Moleküle aus engen Clustern und verteilten sich eher als einzelne Einheiten oder Paare. Biochemische Tests zeigten, dass diese dispergierten Rezeptoren Formen annahmen, die leichter interne Signale auslösten, insbesondere über Wege wie ERK, die Aktivierung und Abtötungskapazität steuern. Das Nachahmen des Spannungsabfalls mit einem kleinen Molekül reproduzierte dieselbe Rezeptoraufweitung und verbesserte das Töten von Zielzellen, was die Idee stützt, dass mechanische Entspannung der Membran ausreicht, die Zellen schon vor ihrem Zusammentreffen mit den Zielen „vorzubereiten“.
Verwundene Lungen bei Mäusen reparieren
Der ultimative Test war ein Mausmodell der medikamenteninduzierten Lungenfibrose. Die Tiere erhielten entweder unveränderte Makrophagen, Standard‑CAR‑Ms oder hydrogel‑vorbereitete Gel‑CAR‑Ms. Alle behandelten Mäuse verbesserten sich im Vergleich zu unbehandelten Kontrollen, doch die Gel‑CAR‑Ms schnitten am besten ab: Ihre Lungen enthielten weniger Kollagen, mehr normale Luftsäcke und weniger FAP‑positive Fibroblasten. Genexpressionsanalysen aus Lungengewebe zeigten, dass Gel‑CAR‑Ms Entzündungssignale beruhigten und die Expression narbenbezogener Gene wirksamer reduzierten als Standard‑CAR‑Ms. Nachverfolgte Zellen verblieben mindestens eine Woche in der Lunge, und verlängerte Sicherheitsprüfungen über 12 Wochen ergaben keine größeren Organschäden, Blutstörungen oder Anzeichen von Autoimmunität.
Eine neue Richtung für zellbasierte Anti‑Fibrose‑Therapien
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die Kombination aus gezielter Zelltechnik und intelligenten Materialien kann angeborene Immunzellen in hocheffektive, dabei nicht übermäßig genetisch komplizierte Narbenbekämpfer verwandeln. Indem man gentechnisch veränderte Makrophagen kurz auf einem sorgfältig abgestimmten weichen Gel ruhen lässt, „stellt“ man mechanisch ihre Oberflächenrezeptoren in einen reaktionsfreudigeren Modus. In Mäusen mit Lungenfibrose führte dies zu besserer Entfernung schädlicher Fibroblasten, Abbau von überschüssigem Kollagen und teilweiser Wiederherstellung normaler Lungenstruktur — ohne erkennbare Sicherheitsprobleme. Zwar bleibt viel Arbeit vor humanen Studien, doch zeigt diese Strategie, dass das Feintuning der physischen Umgebung therapeutischer Zellen eines Tages Behandlungen fibrotischer Lungenerkrankungen wirksamer und präziser machen könnte.
Zitation: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Schlüsselwörter: Lungenfibrose, CAR‑Makrophagen‑Therapie, viskoelastisches Hydrogel, fibroblasten‑aktivierendes Protein, Zell‑Mechanobiologie