Clear Sky Science · de
Molekulare Grundlage der Hemmung der de novo-DNA-Methylierung durch TCL1A
Wie Zellen entscheiden, was sie behalten
Jede Zelle in Ihrem Körper trägt im Wesentlichen dieselbe DNA, doch Nervenzellen, Blutzellen und Hautzellen verhalten sich sehr unterschiedlich. Eine Möglichkeit, wie Zellen ihre Identität „behalten“, sind chemische Markierungen, die an die DNA angefügt werden — ein Prozess namens DNA-Methylierung. Diese Studie enthüllt auf atomarer Ebene, wie ein kleines Protein namens TCL1A die Enzyme abschalten kann, die diese Methylmarken setzen. Da sowohl DNA-Methylierung als auch TCL1A mit Krebs und Fortpflanzungsstörungen in Verbindung stehen, könnte das Verständnis dieses molekularen Tauziehens letztlich neue Therapien inspirieren.
Die DNA-Markierungsmaschinerie der Zelle
DNA-Methylierung funktioniert wie ein Bleistiftstrich am Rand des Genoms und hilft, bestimmte Gene stummzuschalten und das Genom während der Entwicklung zu stabilisieren. Zwei Enzyme, DNMT3A und DNMT3B, sind die hauptsächlichen „Schreiber“, die neue Methylmarken während der frühen Entwicklung und bei der Spezialisierung von Stammzellen anbringen. Wenn diese Enzyme mutiert oder fehlreguliert sind, kann das Muster der DNAMarken durcheinandergeraten und zu Entwicklungsstörungen und Blutkrebserkrankungen beitragen. TCL1A ist ein Protein, das vor allem für seine Rolle bei Krebserkrankungen von Immunzellen bekannt ist, wo es häufig überproduziert wird. Frühere Arbeiten deuteten an, dass TCL1A an DNMT3A und DNMT3B binden und deren Aktivität dämpfen kann, doch war bislang unklar, wie genau dieser Block zustande kommt.
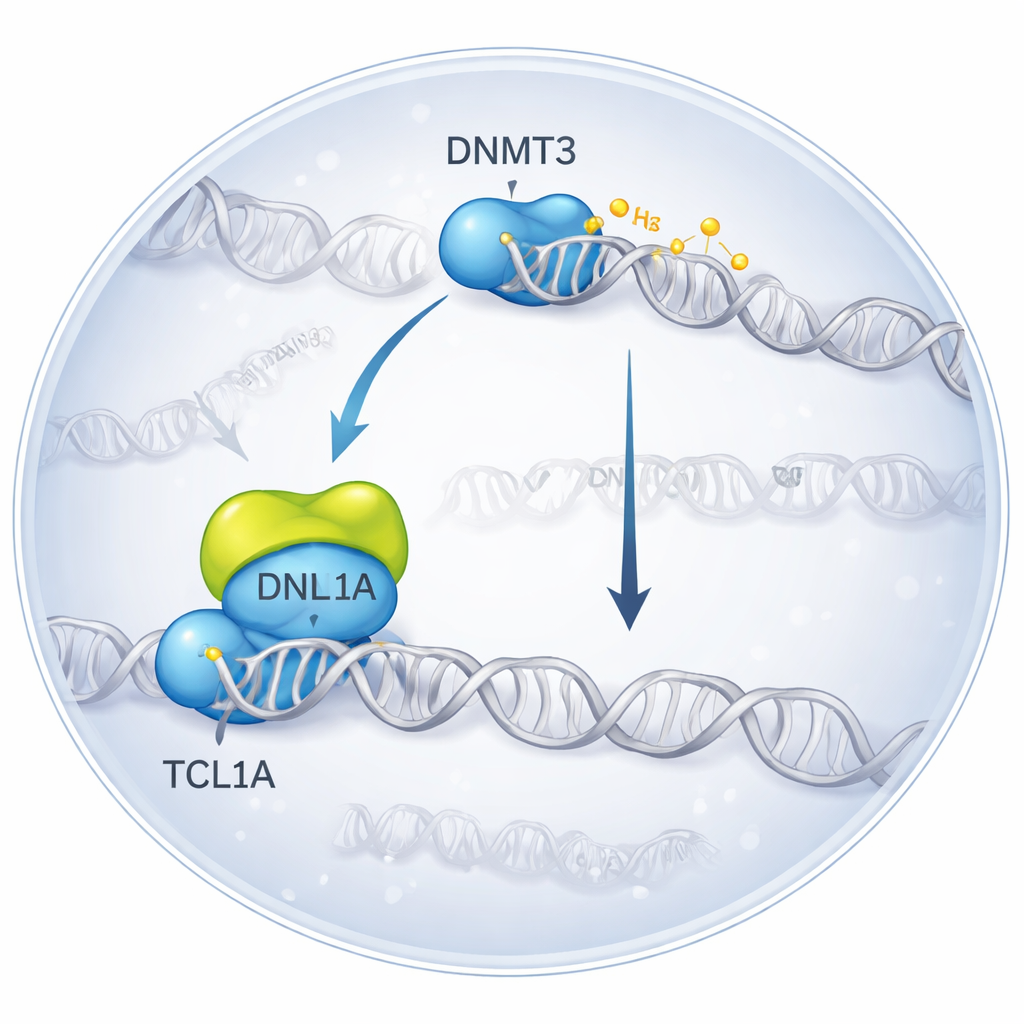
Eine molekulare Begegnung in 3D einfrieren
Die Forschenden nutzten Kryo-Elektronenmikroskopie, eine Technik, die blitzgefrorene Moleküle abbildet, um den Komplex zu visualisieren, der entsteht, wenn DNMT3A an TCL1A bindet. Sie fanden heraus, dass sich zwei DNMT3A-Moleküle paaren und dass auf jeder Seite ein TCL1A-Dimer an den katalytischen Teil von DNMT3A andockt — genau an die Region, die normalerweise mit Helferproteinen und DNA interagiert. Diese Bindungsoberfläche überschneidet sich mit der Stelle, an der ein anderer Partner, DNMT3L, üblicherweise ansetzt, um die Aktivität von DNMT3A zu steigern. In biochemischen Tests reduzierte die Zugabe von TCL1A die Fähigkeit sowohl von DNMT3A als auch DNMT3B, DNA zu methylieren, deutlich, selbst in Gegenwart von DNMT3L, was bestätigt, dass der strukturmechanisch beschriebene Komplex einem stark gehemmt Zustand entspricht.
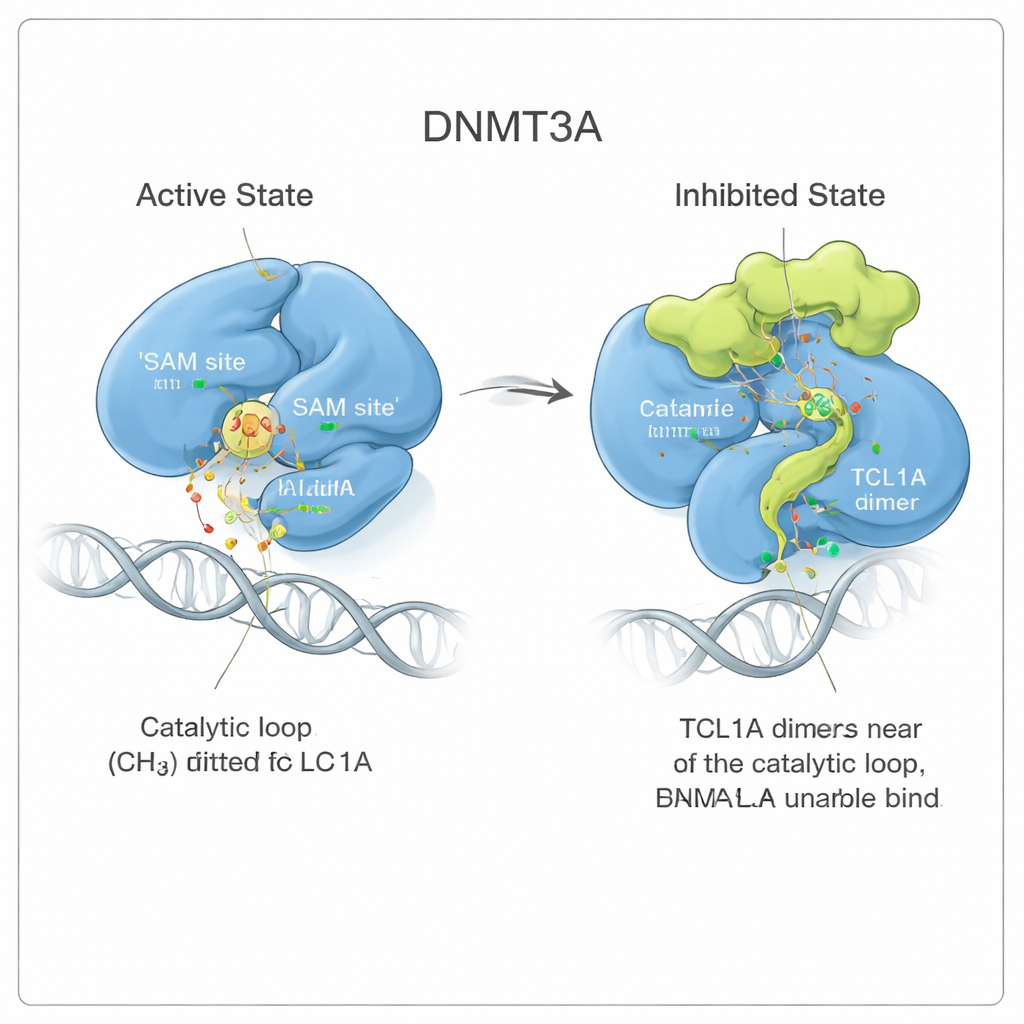
Eine Formänderung, die das Enzym blockiert
Bei genauerer Betrachtung zeigte das Team, dass die Bindung von TCL1A nicht einfach wie ein Deckel auf dem aktiven Zentrum sitzt. Stattdessen löst sie eine subtile, aber weitreichende Formänderung in DNMT3A aus. Zwei flexible Regionen des Enzyms, bekannt als die Ziel-Erkennungs-Schleife und die katalytische Schleife, schwenken von den Positionen weg, die sie einnehmen, wenn DNMT3A an DNA gebunden ist. In der aktiven Form schmiegen sich diese Schleifen an die DNA und bilden eine Tasche für ein kleines Molekül-Brennstoffmolekül namens SAM, das die Methylgruppe spendet. Mit gebundenem TCL1A faltet sich die katalytische Schleife stattdessen in die SAM-Tasche und verstopft sie, wodurch es außerdem für die DNA schwieriger wird, das Enzym zu erreichen. Bindungsmessungen bestätigten, dass DNMT3A, das mit TCL1A assoziiert ist, nachweislich weder DNA noch SAM binden kann.
Beobachtung einer dynamischen Blockade in Bewegung
Um zu verstehen, wie stabil diese inhibierte Konformation ist, führten die Autoren lange Molekulardynamik-Simulationen durch — im Wesentlichen physikbasierte Filme der Moleküle in Lösung. Wenn DNMT3A an seinen Aktivator DNMT3L gebunden war, blieb die katalytische Schleife in ihrer aktiven Position sitzen. In Anwesenheit von TCL1A wurde diese Schleife deutlich beweglicher, schlug umher, besetzte aber wiederholt die SAM-Tasche wie Tang, der wirbelt und dennoch den Abfluss verstopft. Diese konstante Bewegung verringerte den verfügbaren Raum für SAM um mehr als das Zehnfache und stützt ein Modell, in dem TCL1A die natürliche Flexibilität von DNMT3A ausnutzt, um eine dynamische statt einer starren Hemmungsform zu erzwingen.
Folgen für sich entwickelnde Zellen und Krankheit
Das Team untersuchte danach, was diese molekulare Blockade in echten Zellen bedeutet. Sie veränderten Maus-embryonale Stammzellen so, dass diese menschliches TCL1A in einer Phase produzierten, in der Zellen normalerweise eine erhöhte DNA-Methylierung aufbauen, wenn sie zu differenzieren beginnen. Genomeweite Methylierungskarten zeigten, dass Zellen mit überexprimiertem TCL1A das übliche hohe Niveau der DNA-Methylierung nicht erreichten und stark den Zellen ähnelten, bei denen sowohl Dnmt3a als auch Dnmt3b ausgeschaltet waren. Eine mutierte Version von TCL1A, die schlecht an DNMT3-Enzyme bindet, hatte kaum Effekt, was unterstreicht, dass die physische Interaktion entscheidend ist. Diese Ergebnisse verknüpfen den strukturellen Mechanismus mit weitreichenden epigenetischen Veränderungen im gesamten Genom.
Was das für die Gesundheit bedeutet
Zusammengefasst zeigt die Arbeit, wie TCL1A als kraftvolle Bremse auf die Enzyme wirken kann, die neue DNA-Methylierungsmarken setzen. Indem es an einer kritischen Schnittstelle andockt, verändert TCL1A die Position flexibler Schleifen in DNMT3A und DNMT3B so, dass sie ihre DNA-Vorlage oder ihren chemischen Brennstoff nicht mehr binden können, was zu einem globalen Verlust von Methylmarken in Zellen führt. In der normalen Entwicklung kann diese fein abgestimmte Kontrolle helfen zu bestimmen, wann und wo Methylierung hinzugefügt wird. Wird TCL1A fehlplatziert oder überproduziert, wie bei bestimmten Blutkrebserkrankungen und seltenen Fortpflanzungsstörungen, kann derselbe Mechanismus das epigenetische Programm der Zelle entgleisen lassen. Das Verständnis dieser Interaktion auf atomarer Auflösung eröffnet die Möglichkeit, Moleküle zu entwerfen, die TCL1As Wirkung nachahmen oder ihr entgegenwirken und damit potenziell gesunde DNA-Methylierungsmuster wiederherstellen.
Zitation: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Schlüsselwörter: DNA-Methylierung, DNMT3A, TCL1A, Epigenetik, Krebs