Clear Sky Science · de
Beispielhafte Probenabgabemethoden für die Proteinkristallographie mit besonderem Fokus auf den Probenverbrauch
Moleküle in Aktion beobachten
Die Röntgenkristallographie erlaubt es Wissenschaftlern, die Anordnung der Atome in Proteinen zu sehen – den winzigen Maschinen, die das Leben antreiben. Ein neuerer Ansatz, die serielle Kristallographie, geht noch einen Schritt weiter: Sie kann «molekulare Filme» von Proteinen in Aktion aufzeichnen, beispielsweise Enzyme, die ein Arzneimittel verarbeiten, oder photosynthetische Proteine, die Wasser spalten. Doch es gibt einen Haken. Viele wichtige Proteine sind schwer herzustellen und zu kristallisieren, und aktuelle Experimente können Milligramm bis Gramm an kostbarem Material verbrauchen. Dieser Übersichtsartikel stellt eine auf den ersten Blick einfache Frage: Wie können wir Kristalle in starke Röntgenstrahlen einbringen, während wir so wenig Probe wie möglich vergeuden?
Warum die serielle Kristallographie bessere Abgabemethoden braucht
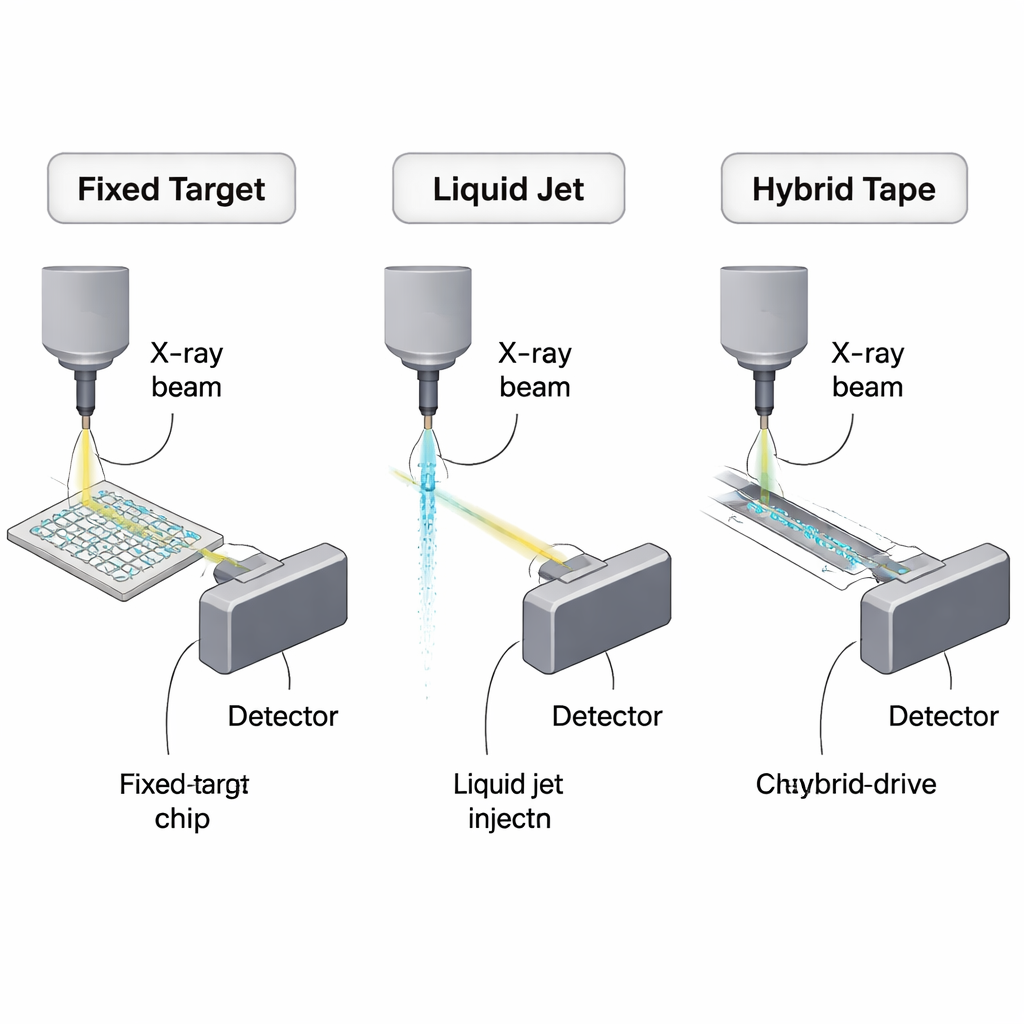
Die traditionelle Kristallographie beruhte auf einem einzelnen großen Kristall, der in einem Röntgenstrahl rotiert wurde. Die serielle Kristallographie dreht das Szenario um: Statt eines großen Kristalls werden Tausende Mikrokristalle, von denen jedes nur einmal genutzt wird, durch ultrastarke Röntgenpulse aus Synchrotronen oder Röntgen-Freie-Elektronen-Lasern (XFELs) geschossen oder gescannt. Das ermöglicht Messungen bei Raumtemperatur und schnelle «Schnappschüsse» chemischer Reaktionen, bedeutet aber auch, dass Kristalle mit Raten ersetzt werden müssen, die zu den Pulsezügen der Röntgenquelle passen und bis zu Millionen Pulse pro Sekunde erreichen können. Ein Großteil der Kristallsuspension trifft nie auf den Strahl und wird verworfen, weshalb die Reduktion des Probenverbrauchs zu einer zentralen technischen und ökonomischen Herausforderung für das Feld geworden ist.
Feststehende Ziele: winzige Chips, die jeden Tropfen strecken
Eine wichtige Strategie besteht darin, Mikrokristalle auf kleinen festen Trägern, sogenannten Fixed Targets, zu immobilisieren. Statt Kristalle am Strahl vorbeizusprühen, ordnen Forscher sie in Arrays auf Silizium- oder Polymerchips an und bewegen den Chip so, dass jeder Kristall einmal in den Röntgenfokus gebracht wird. Im Gedankenexperiment könnte ein idealer Fall etwa 10.000 Mikrokristalle eines Modellproteins theoretisch zu einem vollständigen Datensatz führen und dabei nur rund 450 Nanogramm Protein verbrauchen. Reale Geräte sind noch nicht so sparsam, reduzieren den Bedarf aber bereits auf einige zehn Mikrogramm bis wenige Zehntel Milligramm – Größenordnungen besser als frühe serielle Experimente. Die Übersicht vergleicht Siliziummaschen, ultradünne Polymerfilme und mehrlagige Plastikchips und wägt deren Stärken (geringe Hintergrundstreuung, Kristallwachstum auf dem Chip, Kompatibilität mit Raumtemperaturstudien) gegen praktische Probleme wie Dehydratation, streuende Beiträge des Chipmaterials und zusätzliches «totes Volumen», das durch manuelles Pipettieren entsteht, ab.
Flüssigkeitsjets und viskose Ströme: schnell, aber gefräßig
Eine andere Gruppe von Methoden hält Kristalle in einer Flüssigkeit suspendiert und liefert sie kontinuierlich durch den Strahl. Gasdynamische virtuelle Düsen erzeugen haarfeine Jets, die mit schnellen XFEL-Pulszügen Schritt halten können und deshalb ein Arbeitspferd für zeitaufgelöste Studien und Mix-and-Inject-Experimente sind, bei denen Reaktionen kurz vor der Belichtung durch schnelles Mischen ausgelöst werden. Da Jets jedoch kontinuierlich betrieben werden, trifft der Großteil des Strahls nie auf einen X‑Ray‑Pulse. Selbst mit sorgfältiger Abstimmung verbrauchen praktische Experimente weit mehr Protein als das theoretische Minimum – typischerweise einige zehn bis hunderte Mikroliter konzentrierter Kristallslurries. Um den Verbrauch zu senken, wurden effizientere Designs entwickelt, etwa Doppelstromdüsen, die den Kristallstrom mit einer opferbaren Flüssigkeit umgeben, elektrospinnende «MESH»-Injektoren, die bei niedrigeren Flussraten arbeiten, und hochviskose Extruder, die Kristalle in Gelen oder lipidischen kubischen Phasen mit Mikrolitern pro Minute oder langsamer transportieren. Diese viskosen Methoden sind besonders wertvoll für empfindliche Membranproteine und für Raumtemperaturstudien an Synchrotronen, aber ihre dickeren Ströme erhöhen die Hintergrundstreuung und eignen sich weniger für die schnellsten Röntgenquellen.
Tropfen, Bänder und Hybride: Puls für Puls abstimmen
Eine dritte, zunehmend kreative Klasse von «Hybrid»-Ansätzen kombiniert feste Träger mit kontrollierter Flüssigkeits- oder Tropfenabgabe. Tape‑Drive-Systeme zum Beispiel deponieren Tropfen oder dünne Flüssigkeitsstreifen auf einer sich bewegenden Polymerfolie, die durch den Strahl läuft; durch das Timing der Bewegung lassen sich Reaktionsschritte oder Gasexpositionen in definierten Verzögerungen untersuchen. Drop‑on‑Demand‑Systeme gehen weiter und verwenden akustische oder piezoelektrische Geräte, um Nanoliter- oder sogar Pikoliter-Tropfen nur dann auszuwerfen, wenn ein Röntgenpuls erwartet wird, wodurch der Abfall drastisch reduziert wird. Einige Designs mischen einen Ligandentropfen in einen vorab platzierten, Kristall‑enthaltenden Tropfen auf dem Band, kurz bevor dieser den Strahl erreicht, und ermöglichen so zeitaufgelöste Enzymologie mit sorgfältig rationierten Reagenzien. Andere Hybride, wie die LAMA‑On‑Chip‑Methode, geben winzige Tröpfchen Substrat direkt auf bereits auf Fixed‑Target‑Chips montierte Kristalle. Über diese Designs hinweg reicht der berichtete Proteinverbrauch über eine große Spanne – von nahezu Milligramm‑Niveau bis zu einigen Milligramm für vollständige zeitaufgelöste Reihen – und zeigt sowohl das Potenzial als auch die derzeitigen ingenieurtechnischen Herausforderungen bei der Synchronisierung von Tropfen, Kristallen und Röntgenpulsen.
Wie nah sind wir am theoretischen Minimum?
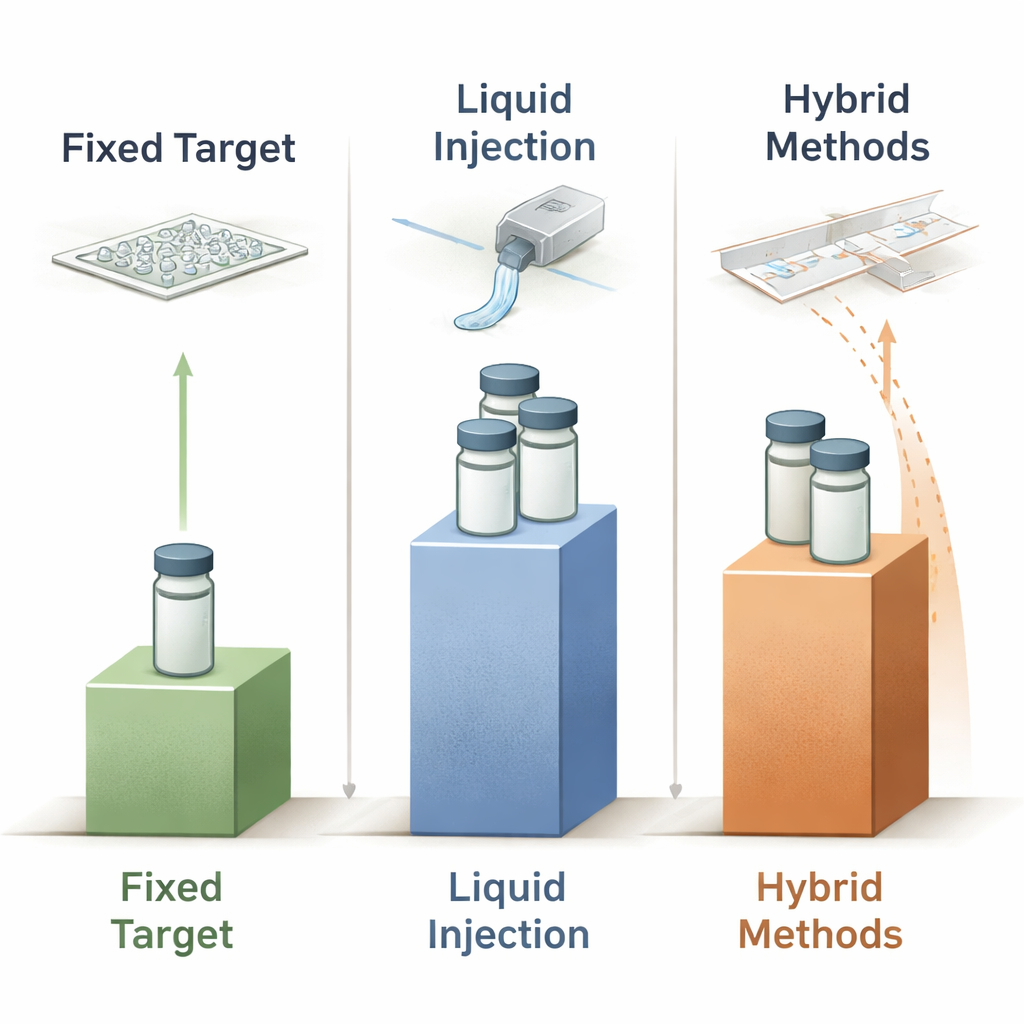
Durch den Vergleich dutzender veröffentlichter Experimente zu Fixed Targets, flüssigen Injektoren und Hybridsystemen zeigen die Autoren, dass keine der existierenden Methoden dem idealen 450‑Nanogramm‑Benchmark nahekommt; selbst die besten Geräte liegen noch grob zwei Größenordnungen darüber. Dennoch zeichnen sich klare Trends ab. Fixed Targets benötigen typischerweise am wenigsten Protein und sind attraktiv, sofern zeitaufgelöstes Mischen nicht erforderlich ist oder on‑chip realisiert werden kann. Flüssigkeitsjets dominieren nach wie vor die anspruchsvollsten zeitaufgelösten XFEL‑Studien, sind aber sehr probeintensiv, insbesondere wenn viele Zeitpunkte erforderlich sind. Hybride Tropfen‑und‑Band‑Schemen bieten einige der größten relativen Einsparungen, vor allem wenn die Tropfenzeit präzise mit der Röntgenquelle synchronisiert ist. Ein Blick nach vorn: Der Artikel argumentiert, dass weitere Fortschritte durch bessere mikrofluidische Kontrolle, Automatisierung zur Beseitigung verschwenderischer Handhabungsschritte und den Einsatz kompakter Röntgenquellen sowie datengestützter Optimierung zu erwarten sind, um Experimente und Abgabesysteme gemeinsam zu entwerfen und den Proteingebrauch immer näher an das theoretische Limit zu bringen.
Zitation: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Schlüsselwörter: serielle Kristallographie, Proteinkristallographie, Probenabgabe, Röntgen-Freie-Elektronen-Laser, Mikrofluidik