Clear Sky Science · de
Das Nervenzentrum der Organ‑Technik
Warum die Verkabelung von Organen wichtig ist
Wissenschaftler kommen dem Ziel näher, Ersatzorgane im Labor zu züchten, um den dramatischen Mangel an Spenderherzen, -lebern, -nier en und mehr zu bekämpfen. Die meisten künstlichen Organe konzentrieren sich jedoch auf Blutgefäße und vernachlässigen eine weitere entscheidende Zutat: Nerven. Dieser Übersichtsartikel erklärt, warum die elektrische Verkabelung des Körpers wesentlich für Organwachstum, Alltagfunktion und Heilung ist und wie Forschende lernen, Nervennetze in im Labor gezüchtete Organe einzubauen.
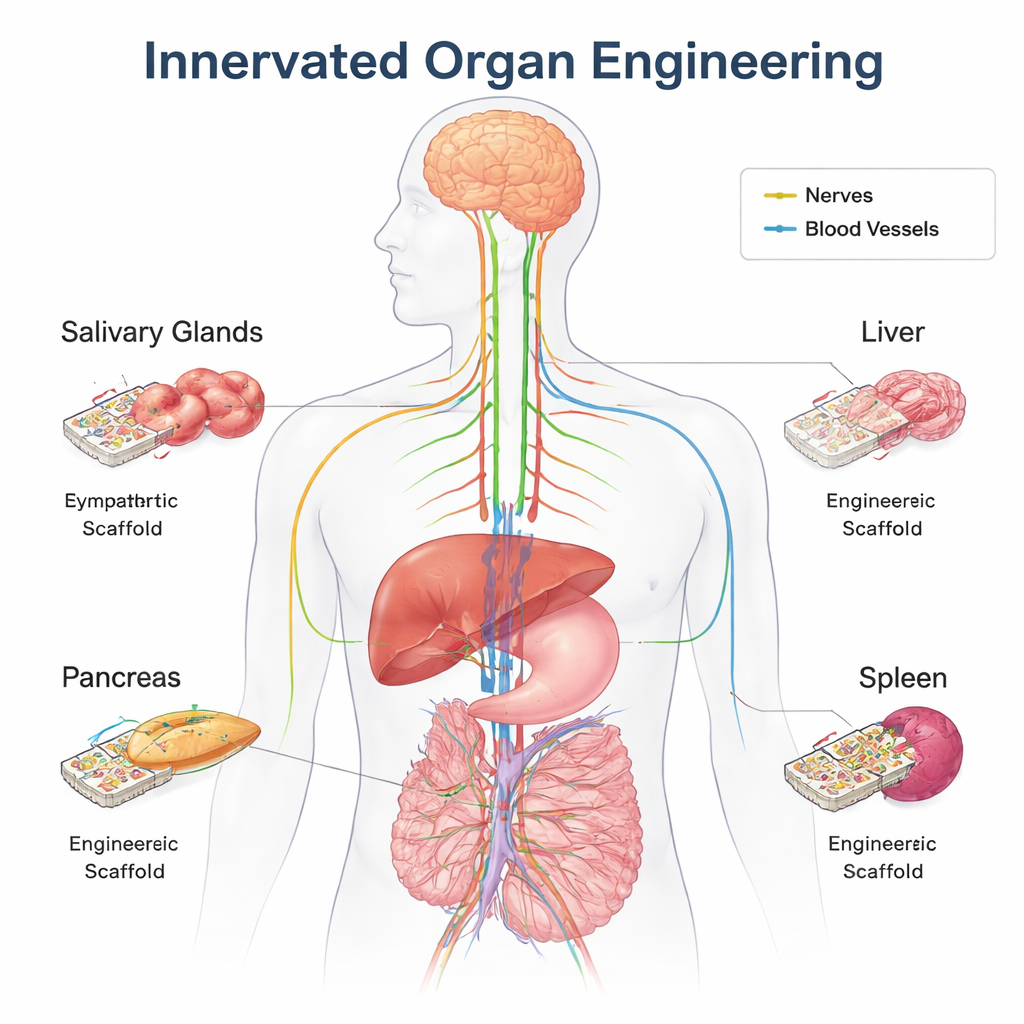
Das verborgene Steuerungsnetz des Körpers
Jedes größere Organ ist von Nervenfasern durchzogen, die ständig mit Gehirn und Rückenmark kommunizieren. Über das autonome Nervensystem — die „Kampf‑oder‑Flucht“‑ und die „Ruhe‑und‑Verdauung“‑Zweigstellen — regulieren diese Nerven unauffällig Blutzucker, Verdauung, Immunantworten, Durchblutung und mehr. Sie tun dies durch das Senden chemischer Botenstoffe wie Acetylcholin und Noradrenalin und durch das Wahrnehmen von Veränderungen wie Dehnung, Temperatur oder Nährstoffständen. Über die tägliche Steuerung hinaus helfen Nerven auch bei der Formung von Organen vor der Geburt, leiten die Wundheilung und unterstützen Stammzellen, die Gewebe reparieren. An vielen Stellen wachsen Nerven entlang von Blutgefäßen und nutzen ähnliche Wegweiser, sodass Verkabelung und „Sanitäranlagen“ gemeinsam entstehen.
Warum Transplantate ohne Nerven zurechtkommen — aber Labororgane nicht
Konventionelle Organtransplantate werden in der Regel ohne ihre ursprünglichen Nerven eingesetzt. Eine transplantierte Leber oder Niere kann weiterhin funktionieren, weil sie Hormone und andere Signale über den Blutkreislauf empfängt, und im Laufe der Zeit können neue Nervenfasern vom Empfänger einwachsen. Diese „Schonfrist“ existiert nicht für von Grund auf neu konstruierte Organe. Solche Konstrukte fehlen typischerweise die vollständige Mischung reifer Zelltypen und die komplexe Stützmatrix eines natürlichen Organs. Präzise Nervenverbindungen sind besonders wichtig, um die vielen spezialisierten Zellen in Organen wie Bauchspeicheldrüse, Leber, Speicheldrüsen und Milz zu koordinieren. Die Autoren argumentieren, dass bei der Bottom‑up‑Organ‑Technik — bei der Organe aus kleinen Bausteinen zusammengesetzt werden — vorgeplante Innervation als Konstruktionsanforderung und nicht als optionales Extra betrachtet werden sollte.
Wie Nerven vier Schlüsselorgane formen
Die Übersichtsarbeit untersucht ausführlich, wie Nerven vier beispielhafte Organe beeinflussen. In der Bauchspeicheldrüse helfen sympathische und parasympathische Fasern während der Entwicklung, die Architektur der insulinproduzierenden Langerhans‑Inseln zu formen, und feinjustieren später die Freisetzung von Insulin und Glukagon, wenn der Blutzucker steigt oder fällt. In den Speicheldrüsen erhält frühe parasympathische Einwirkung epitheliale Stammzellen am Leben und lenkt die verzweigende Struktur der Ausführungsgänge, die schließlich Speichel absondern; das Durchtrennen dieser Nerven zum falschen Zeitpunkt stört die normale Drüsenbildung. Die Nerven der Leber registrieren Salz, Wasser, Zucker und Fett im Blut und passen Stoffwechsel, Blutdruck und Regeneration nach Verletzung an. In der Milz kommunizieren sympathische Fasern direkt mit Immunzellen, dämpfen oder verstärken Entzündungen und helfen dem Körper, auf Infektionen und Stress zu reagieren. In all diesen Organen ist der Verlust oder die Fehlverkabelung von Nerven mit Diabetes, Verdauungsstörungen, Lebererkrankungen und geschwächter Immunfunktion verknüpft.
Organe mit eingebauter Verkabelung bauen
Um Innervation in bioengineerte Organe zu bringen, kombinieren Forschende fortschrittliches 3D‑Drucken, ausgeklügeltes Scaffold‑Design und aus Stammzellen abgeleitete Nervenzellen. Extrusions‑ und lichtbasierte Bioprinting‑Verfahren können verschiedene Zelltypen und Materialien in präzisen Mustern platzieren, während spezialisierte Hydrogele und Polymere so abgestimmt sind, dass sie lange, verzweigende Nervenfasern unterstützen. Studien haben bereits gedruckte neuronale Netzwerke, Nerven‑Muskel‑Einheiten und kleine gehirnähnliche Gewebe geschaffen, die realistische elektrische Aktivität zeigen. Die Autoren skizzieren praktische Pläne für innervierte Versionen von Bauchspeicheldrüse, Speicheldrüse, Leber und Milz: die relevanten Organzellen isolieren oder ableiten, sie mit autonomen Neuronen (sympathisch und parasympathisch) in kompatiblen Bioinks mischen, in organförmige Strukturen drucken und in Bioreaktoren reifen lassen, damit Nerven vor der Implantation ins Gewebe ausstrecken können.
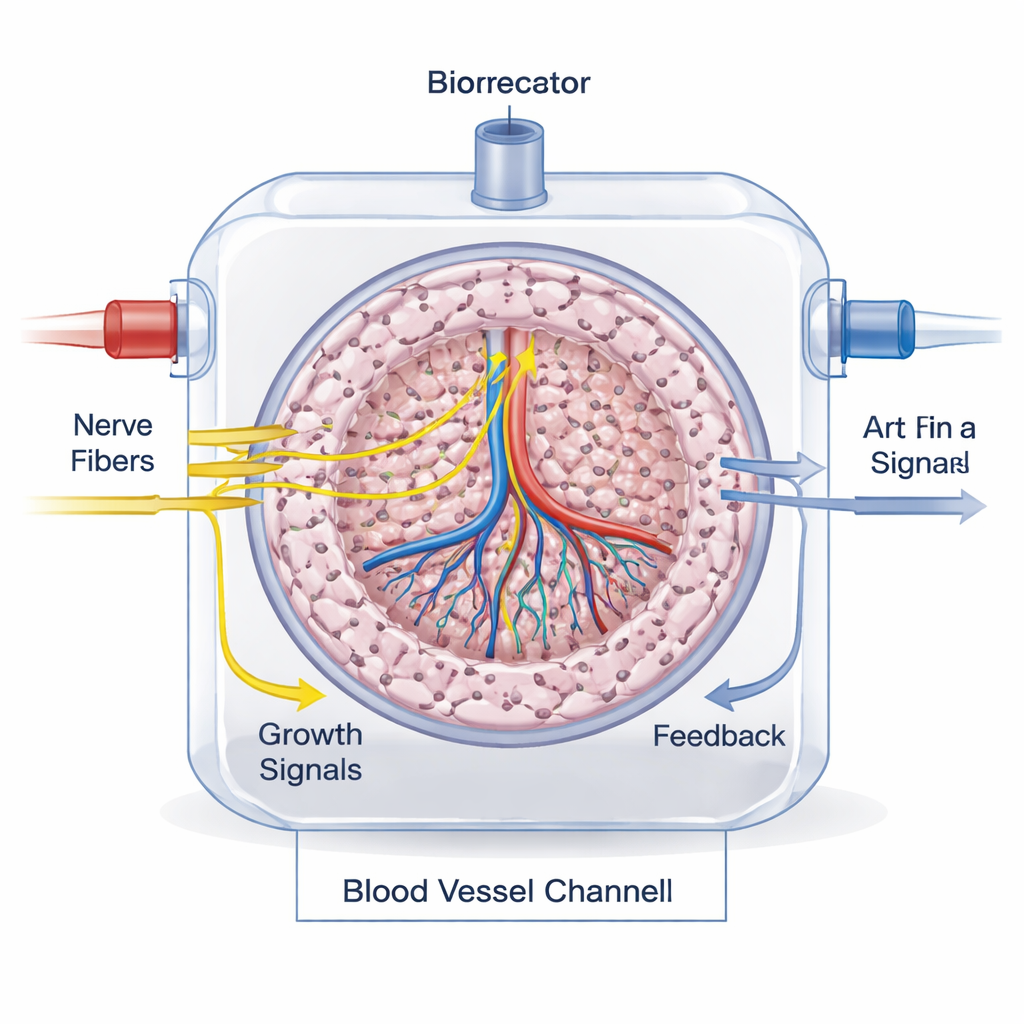
Messen, ob die Verkabelung funktioniert
Nachzuprüfen, ob Nerven wirklich integriert und funktional sind, ist eine große Herausforderung. Im Labor färben Forschende nach nervenspezifischen Proteinen, messen Neurotransmitter mit biochemischen Tests und verwenden Live‑Imaging, um das Wachstum von Axonen und die Reaktion von Zellen zu beobachten. Mikrof luidische „Organ‑on‑a‑Chip“‑Plattformen helfen, realistische Blutströmungen und Nerven‑Organ‑Signalübertragung zu modellieren. In Tierversuchen und schließlich bei Patienten kann die Innervation verfolgt werden, indem Gewebefärbungen, Nerventracer und moderne Bildgebungsverfahren wie MRT, CT und PET kombiniert werden, wobei spezielle radioaktive Verbindungen sympathische oder parasympathische Fasern hervorheben.
Von der Idee zur Therapie
Der Artikel schließt mit der Feststellung, dass Nerven kein Luxusmerkmal, sondern eine Kernanforderung für wirklich funktionale künstliche Organe sind. Um von vielversprechenden Labordemos zu echten Therapien zu gelangen, muss künftige Arbeit großmaßstäbliches Bioprinten komplexer Nervennetze verbessern, Zellquellen verfeinern (insbesondere aus menschlichen Stammzellen abgeleitete autonome Neuronen) und praktikable klinische Bildgebungswerkzeuge entwickeln, um die neuronale Integration nach der Implantation zu überwachen. Werden diese Hürden überwunden, könnten nächste‑Generation‑konstr uierte Organe nicht nur verlorenes Gewebe ersetzen, sondern sich nahtlos in die körpereigenen Steuerkreise einfügen und verlässlichere, lebensnähere Behandlungen für Diabetes, Leberversagen, Xerostomie‑Erkrankungen, Immundefizite und darüber hinaus bieten.
Zitation: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Schlüsselwörter: Organtechnik, Innervation, Biofabrikation, 3D‑Bioprinting, autonomes Nervensystem