Clear Sky Science · de
Optische Superauflösungshistologie von formalinfixierten, paraffineingebetteten Gewebeproben: Herausforderungen und Chancen
Mehr sehen in aufbewahrten Gewebeproben
Krankenhäuser auf der ganzen Welt bewahren winzige Schnitte von Patientenorganen in Paraffinblöcken auf, damit Erkrankungen wie Krebs oder Nierenschäden über Jahre hinweg untersucht werden können. Dieser Übersichtsartikel erklärt, wie neue Arten von Lichtmikroskopen diese routinemäßigen Proben in leistungsfähige Fenster auf Krankheiten verwandeln und Details sichtbar machen, die für normale Krankenhausmikroskope zu klein sind. Diese Fortschritte könnten Ärzten helfen, Erkrankungen früher zu erkennen, ihren Verlauf besser zu verstehen und Behandlungen präziser zuzuschneiden.
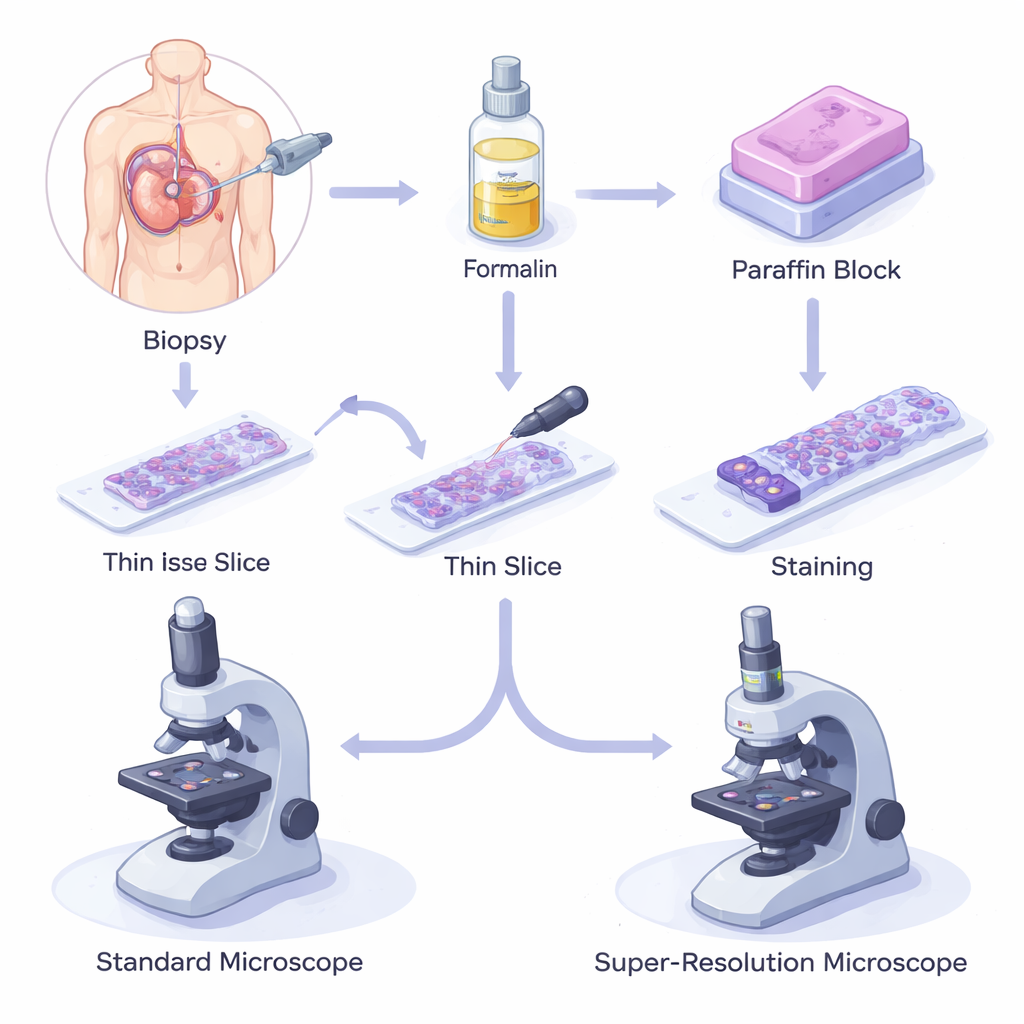
Wie wachserhaltende Gewebe die moderne Medizin antreiben
Bei einer Biopsie wird ein kleines Gewebestück entnommen, in einer Chemikalie namens Formalin fixiert, um Verfall zu stoppen, und dann in Paraffinwachs eingebettet. Der Block wird in haarfeine Schnitte zerteilt, auf Objektträger gelegt, gefärbt und unter einem Lichtmikroskop untersucht. Die Methode der formalinfixierten, paraffineingebetteten (FFPE) Proben ist kostengünstig, zuverlässig und kann Proben über Jahrzehnte bei Raumtemperatur konservieren. Infolgedessen werden Millionen von FFPE-Proben in Biobanken weltweit gelagert und unterstützen alles von Grundlagenforschung bis hin zu fortgeschrittenen genetischen und Proteinanalysen und bilden das Rückgrat moderner Diagnose und Prognose.
Warum gewöhnliche Mikroskope nicht mehr ausreichen
Konventionelle optische Mikroskope sind durch die Physik des Lichts begrenzt: Details kleiner als etwa 250 Nanometer verschwimmen. Viele krankheitsrelevante Strukturen – wie die feinen Filter in den Nieren, die Verbindungen zwischen Nervenzellen oder kleine Architekturveränderungen in der DNA im Zellkern – liegen unterhalb dieser Grenze. Der heutige Arbeitsablauf kombiniert oft die Standardlichtmikroskopie für einen groben Überblick mit der Elektronenmikroskopie für Nanometerdetails, doch dieser Ansatz ist langsam, teuer und erfordert völlig andere Probenvorbereitungen. Kliniker und Forscher suchen daher nach einem einzigen, flexiblen System, das große Flächen schnell scannen und gleichzeitig in denselben FFPE-Schnitten nanoskalige Merkmale sichtbar machen kann.
Neue Wege, das Bild zu schärfen
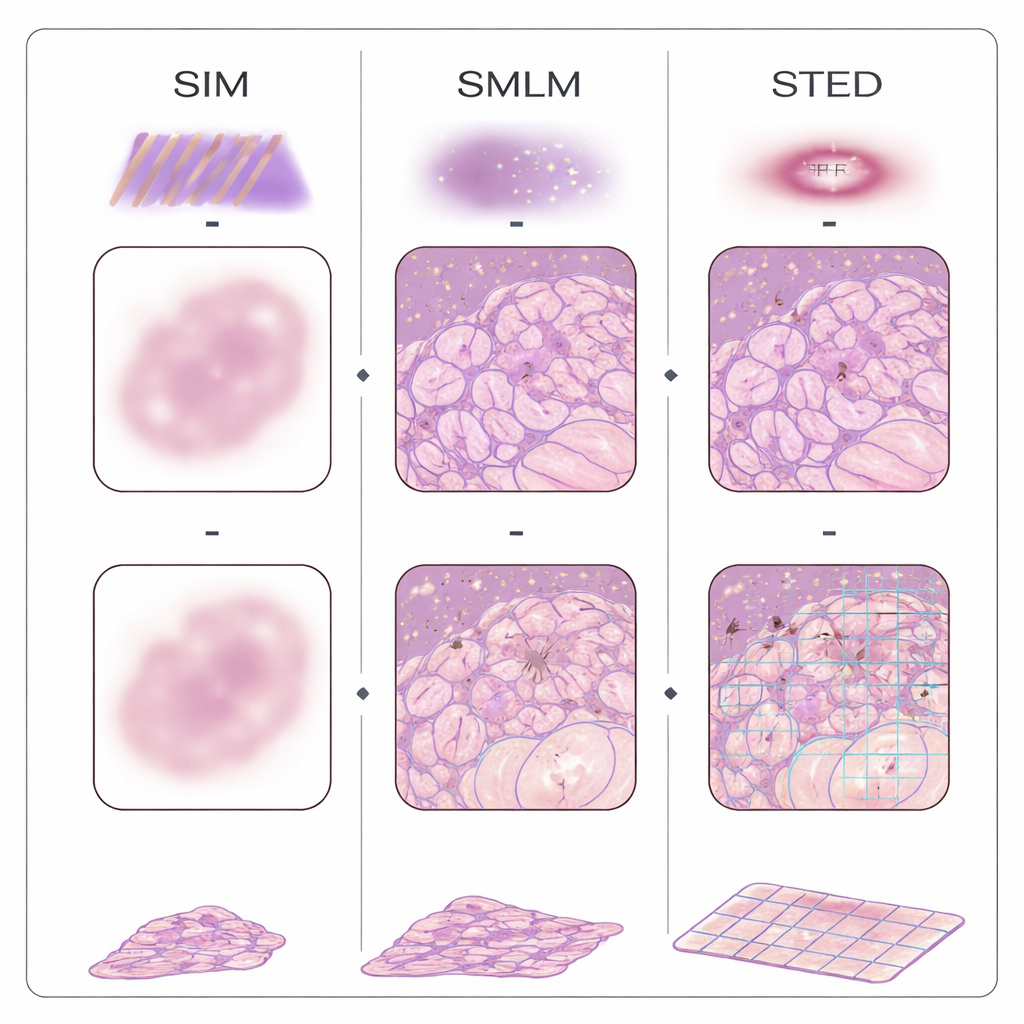
In den vergangenen zwei Jahrzehnten haben mehrere Familien von „Super‑Auflösungs“-Mikroskopen die traditionelle Auflösungsgrenze durch den Einsatz fluoreszierender Marker und raffinierter Optik durchbrochen. Single‑Molecule-Localization-Methoden schalten Moleküle ein und aus und bestimmen ihre Positionen einzeln; Structured Illumination projiziert gestreifte Lichtmuster auf das Gewebe und verwendet Rechenverfahren, um feinere Details zurückzugewinnen; Stimulated Emission Depletion schafft mit einem donutförmigen Strahl einen winzigen leuchtenden Punkt; und fluktuationsbasierte Ansätze analysieren subtile Flimmern im Bild, um Struktur zu erschließen. Eine andere Strategie, die Expansion-Mikroskopie, umgeht komplexe Optik, indem das Gewebe in ein Gel physikalisch aufgeschwemmt wird, sodass gewöhnliche Mikroskope zuvor unsichtbare Details sehen können. Diese Methoden wurden bereits auf FFPE-Proben von Brust, Dickdarm, Pankreas, Niere, Gehirn, Haut, Plazenta und anderen Organen angewendet und zeigten beispielsweise, wie Mitochondrien in Tumoren verändert sind, wie Nierenfilter versagen und wie sich Proteinaggregate bei Alzheimer bilden.
Hürden auf dem Weg zum Alltag
Trotz ihres Potenzials sind diese Techniken noch nicht bereit, in den meisten Pathologielabors routinemäßig eingesetzt zu werden. Viele Super‑Auflösungs‑Systeme sind langsam, decken nur winzige Sichtfelder ab oder benötigen zehntausende Bilder, um ein einziges hochdetailliertes Bild zu erstellen, was unpraktisch ist, wenn ein Pathologe große Gewebeareale beurteilen muss. FFPE-Gewebe selbst sind optisch anspruchsvoll: Sie streuen Licht, zeigen Eigenfluoreszenz und können die Moleküle verbergen, die markiert werden sollen, was zu unscharfen Bildern oder falschen Strukturen führen kann. Manche Methoden erfordern spezielle Farbstoffe, kundenspezifische Puffer oder mehrstufige chemische Behandlungen, die sich nur schwer in standardisierte histologische Arbeitsabläufe einfügen. Darüber hinaus sind kommerzielle Instrumente teuer und komplex in der Bedienung, und die resultierenden Daten verlangen intensive rechnerische Verarbeitung und Speicherressourcen.
Intelligente Optik und intelligente Software zusammenbringen
Um diese Hindernisse zu überwinden, kombinieren Forscher verbesserte Optik mit label‑freien Methoden und Künstlicher Intelligenz. Hochdurchsatzfähige, beugungsbegrenzte Methoden wie Fourier‑Ptychographie und nichtlineare optische Mikroskopie können große, sogar ungefärbte FFPE‑Schnitte schnell abtasten und quantitative Karten der Gewebestruktur liefern. Plattformen der digitalen Pathologie erfassen inzwischen ganze Objektträger in hoher Auflösung und nutzen maschinelles Lernen, um Tumore zu erkennen und Biomarker wie HER2, Ki‑67 und PD‑L1 zu bewerten. Deep‑Learning‑Modelle können sogar niederauflösende Bilder in superaufgelöste Ansichten umwandeln, was den Bedarf an spezialierter Hardware potenziell verringern und die Nutzung bestehender Biopsiearchive verbessern könnte.
Was das für zukünftige Patientinnen und Patienten bedeutet
Die Autoren kommen zu dem Schluss, dass eine echte „Super‑Auflösungshistologie“ von FFPE‑Proben – die Nanometerdetails, hohe Geschwindigkeit, vertretbare Kosten und Kompatibilität mit aktuellen Laborroutinen vereint – noch nicht vollständig verwirklicht ist, aber in Reichweite liegt. Sobald optische Methoden schneller und robuster werden und KI‑gestützte Analysen ausreifen, könnten diese Werkzeuge subtile, frühe Veränderungen im Gewebe sichtbar machen, die heute unbemerkt bleiben, die Genauigkeit von Diagnosen verbessern und präzisere Therapieentscheidungen anleiten. Langfristig könnte aus jedem archivierten Paraffinblock eine hochauflösende Karte der Krankheit werden, die Forschung und klinische Versorgung gleichermaßen transformiert.
Zitation: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Schlüsselwörter: Superauflösungsmikroskopie, FFPE-Gewebe, digitale Pathologie, optische Bildgebung, Krebsdiagnostik