Clear Sky Science · de
Nanozyme erweitern die Grenzen der Biokatalyse
Kleine Helfer, die Chemie beschleunigen
Vom Bierbrauen bis zur Verdauung verlassen wir uns auf unsichtbare Helfer, sogenannte Katalysatoren, die chemische Reaktionen beschleunigen. Mehr als ein Jahrhundert lang galten die biologischen Katalysatoren als empfindliche Proteine und später als katalytische RNA. Dieses Review stellt „Nanozyme“ vor – winzige, konstruierte Partikel, die sich wie Enzyme verhalten, aber aus robusten Materialien wie Metallen, Oxiden und Kohlenstoff aufgebaut sind. Sie überstehen Hitze, Kälte und raue Bedingungen und verändern zunehmend unser Verständnis von Chemie in lebenden Systemen, Krankheiten, der Industrie und sogar der Entstehung des Lebens.
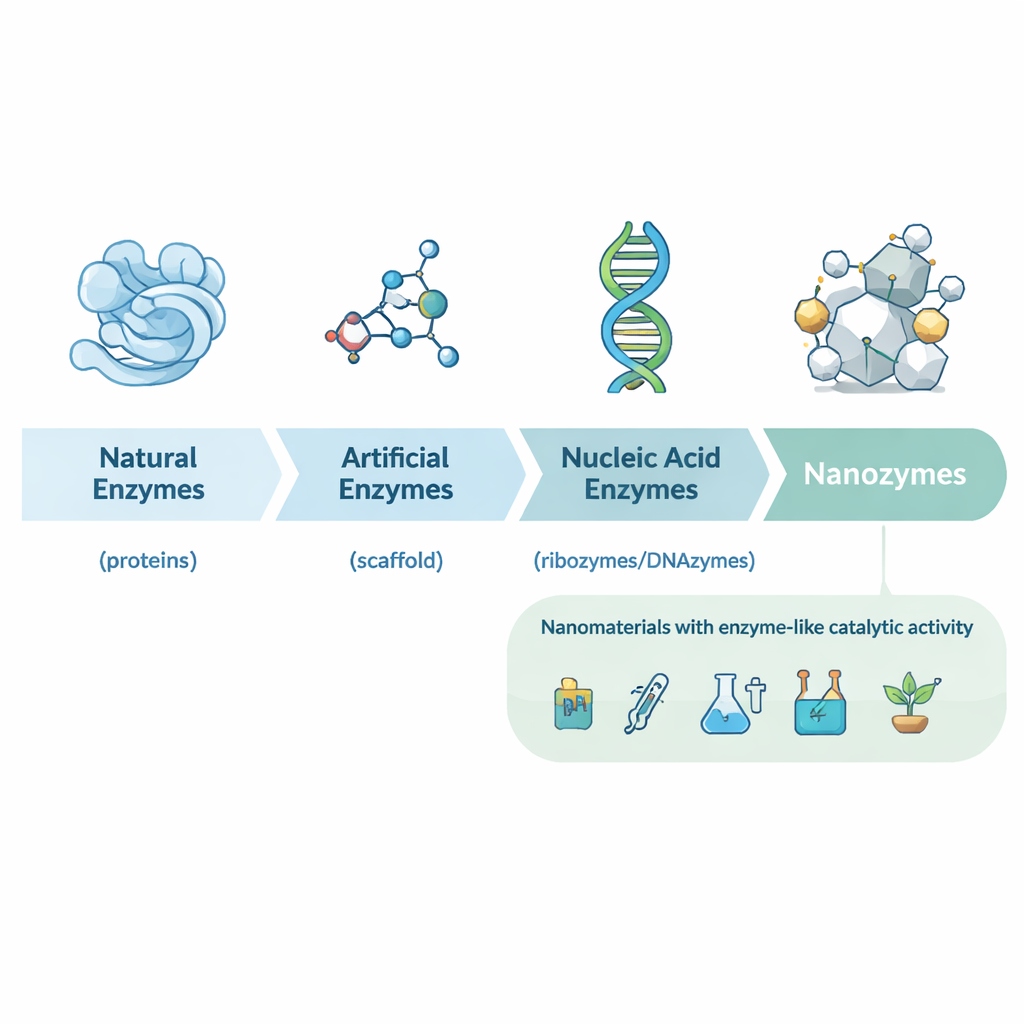
Von natürlichen Enzymen zu designer Nanokatalysatoren
Der Artikel skizziert zunächst die Geschichte der Biokatalyse, von den frühen Entdeckungen von Proteinenzymen in Hefe und Magensäften bis hin zu Ribozymen (katalytische RNA) und einer Vielzahl künstlicher Enzyme aus kleinen Molekülen und Antikörpern. Diese traditionellen Katalysatoren sind leistungsfähig, aber oft teuer, instabil und schwer in großen Mengen herzustellen. Anfang der 2000er Jahre entdeckten Forscher, dass einige Nanomaterialien – zum Beispiel Eisenoxid‑Nanopartikel – das Verhalten klassischer Enzyme wie Peroxidase aus Meerrettich nachahmen können. Daraus entstand das Konzept der Nanozyme: nanometergroße Partikel, deren eigene Struktur ihnen enzymähnliche Aktivität verleiht, statt daran gebundene Proteine oder kleinmolekulare Katalysatoren.
Was Nanozyme unterscheidet
Im Gegensatz zu Enzymen, die eine einzelne, präzise geformte aktive Tasche besitzen, zeigen Nanozyme zahlreiche aktive Stellen über ihre Oberflächen. Diese Stellen können an Kristallkanten, Defekten oder Grenzflächen zwischen zwei Materialien liegen und gemeinsam viele Moleküle gleichzeitig umsetzen. Eine einzelne aktive Stelle eines Nanozyms ist in der Regel weniger effizient als die eines Enzyms, doch ein Nanopartikel kann Tausende solcher Stellen beherbergen, sodass seine Gesamtkatalyseleistung mit oder über der natürlicher Enzyme liegen kann. Ihre Aktivität lässt sich außerdem durch Änderung von Größe, Form, chemischer Dotierung und Oberflächenbeschichtungen feinjustieren – ähnlich dem Umbau der Architektur und Verkabelung einer winzigen Maschine. Da sie aus robusten Festkörpern statt aus empfindlich gefalteten Proteinen bestehen, funktionieren Nanozyme bei hohen oder niedrigen Temperaturen oder in hohen Salzkonzentrationen weiter, die die meisten Enzyme schnell ausschalten würden.
Wie Nanozyme wirken und wie man sie misst
Die Autoren zeigen, dass Nanozyme oft denselben grundlegenden kinetischen Regeln folgen wie Enzyme, etwa dem Michaelis‑Menten‑Verhalten, bei dem die Reaktionsgeschwindigkeit davon abhängt, wie leicht ein Katalysator sein Substrat bindet und umsetzt. Es gibt jedoch wichtige Unterschiede. Ein Partikel kann mehrere Typen aktiver Stellen tragen, sodass ein einzelnes Nanozym verschiedene oder sogar widersprüchliche Reaktionen ausführen kann, etwa gleichzeitig reaktive Sauerstoffspezies erzeugen und abbauen. Das kann komplexe, „nicht‑lehrbuchmäßige“ kinetische Kurven erzeugen, die mehrere Prozesse unter einem glatten Verlauf verbergen. Das Review erklärt, wie Forscher diese Verhaltensweisen aufschlüsseln, abschätzen, wie viele aktive Stellen tatsächlich vorhanden sind, und die Gesamtaktivität verschiedener Nanozyme mit standardisierten Einheiten vergleichen – alles entscheidend, um ein interessantes Material in ein verlässliches Werkzeug zu verwandeln.
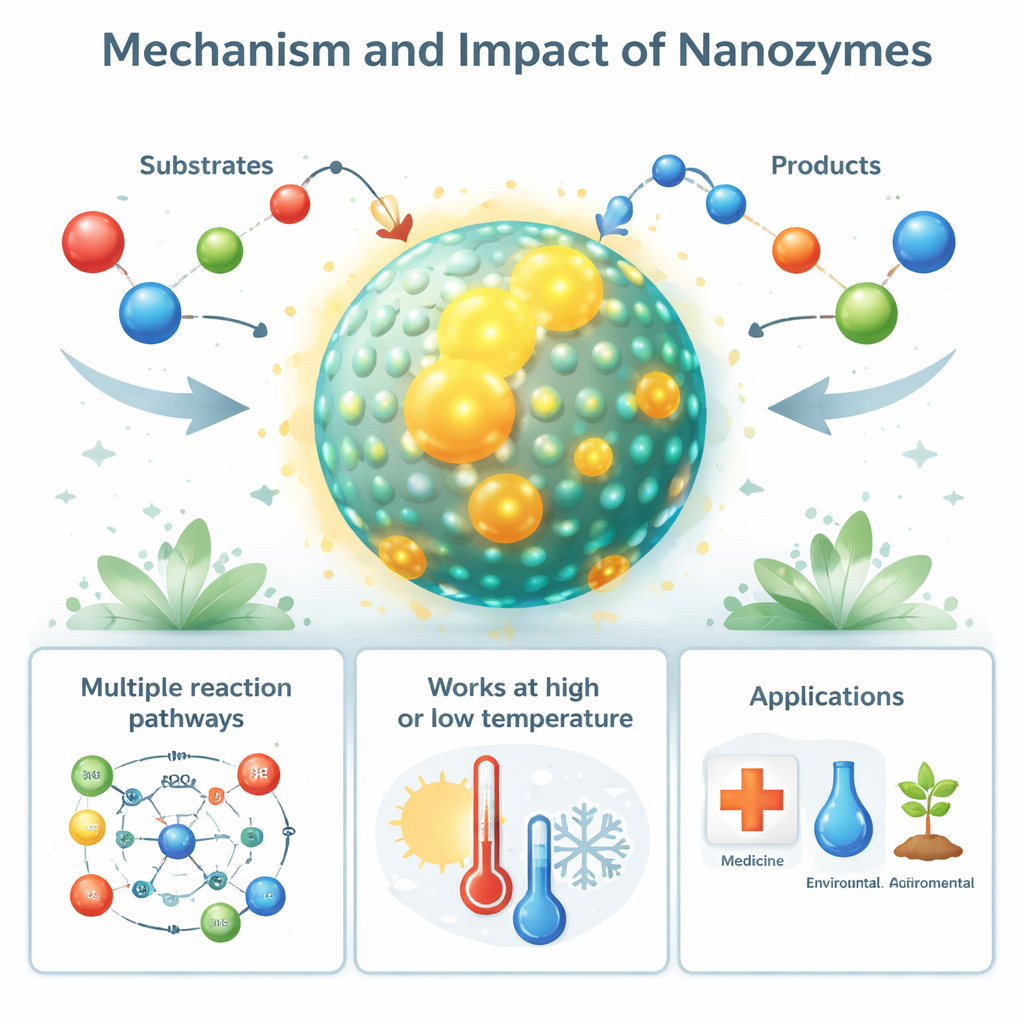
Von natürlichen Nanozymen zu Anwendungen in der Praxis
Bemerkenswerterweise beschränkt sich nanozymähnliches Verhalten nicht auf das Labor. Bestimmte biologische Nanostrukturen, wie eisengefüllte Proteinhüllen (Ferritin) und magnetische Partikel in Bakterien (Magnetosomen), wirken als natürliche Nanozyme und helfen, schädliche reaktive Sauerstoffspezies zu kontrollieren. Selbst krankheitsassoziierte Proteinfasern, etwa Amyloidablagerungen bei Alzheimer, können peroxidaseähnliche Aktivität annehmen, die umliegende Zellen schädigt. Auf der angewandten Seite werden synthetische Nanozyme als günstigere, robustere Ersatzstoffe für Enzyme in Diagnosetests, Biosensoren und industriellen Assays eingesetzt. Ihre Fähigkeit, reaktive Sauerstoffspezies zu erzeugen oder zu entfernen, wird genutzt, um Tumorzellen und Bakterien abzutöten, Gewebe vor oxidativem Stress zu schützen und Nutzpflanzen bei Dürre, Salzstress und Verschmutzung widerstandsfähiger zu machen.
Die nächste Generation intelligenter Katalysatoren entwerfen
Mit Blick nach vorn heben die Autoren zentrale Herausforderungen hervor: die genauen atomaren Strukturen zu identifizieren, die als aktive Stellen fungieren, die Reaktionsselektivität zu verbessern, sodass Nanozyme nur dort und dann wirken, wo sie gebraucht werden, und Sicherheit sowie Stabilität im Körper zu gewährleisten. Sie verweisen auf fortgeschrittene Bildgebung, quantenmechanische Simulationen und maschinelles Lernen als leistungsfähige Werkzeuge zur Vorhersage und Optimierung der Nanozyme‑Leistung. Da Nanozyme unter extremen Bedingungen arbeiten, auf Licht, Wärme, Schall oder Magnetfelder reagieren und manchmal mehrere Reaktionen nacheinander ausführen können, könnten sie neue Therapien, Umwelttechnologien und industrielle Prozesse ermöglichen. Das Review schließt mit der Feststellung, dass Nanozyme die Definition von Biokatalyse erweitern und möglicherweise sogar Hinweise darauf geben, wie primitive Katalysatoren einst die Chemie des frühen Lebens antrieben.
Zitation: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Schlüsselwörter: Nanozyme, Biokatalyse, Nanopartikel, Enzym‑Mimetika, reaktive Sauerstoffspezies