Clear Sky Science · de
Endogene Opioidrezeptoren und das Festmahl-oder-Hungern von maladaptivem Essverhalten
Warum unser Gehirn uns zum Überessen oder fast Nichtessen treiben kann
Die meisten Menschen haben sowohl starke Verlangen nach reichhaltigen Lebensmitteln als auch Phasen mit Appetitverlust unter Stress erlebt. Dieser Artikel erklärt, wie das körpereigene Opioidsystem — dieselbe Familie von Botenstoffen, die an Schmerzstillung und Drogenabhängigkeit beteiligt ist — Essgewohnheiten in gefährliche Extreme treiben kann. Anhand von Fettleibigkeit und Anorexia nervosa zeigen die Autoren, wie ähnliche Hirnschaltkreise und chemische Signale gegensätzliche Ergebnisse hervorbringen können: chronisches Überessen oder schwere Selbstverhungung.

Die Lust- und Schmerzchemie des Gehirns
Der Körper stellt natürlicherweise opioidähnliche Moleküle wie Endorphine, Enkephaline und Dynorphine her. Diese Stoffe wirken an Opioidrezeptoren, die im Gehirn weit verbreitet sind, insbesondere in Bereichen, die Belohnung, Motivation, Hunger und Schmerz steuern. Beim Essen, besonders von schmackhaften, kalorienreichen Nahrungsmitteln, reagieren diese Systeme mit Signalen, die Nahrung belohnend erscheinen lassen und Unbehagen lindern können. Unter normalen Bedingungen hilft das, genügend Nahrung zu suchen, ohne ins Extreme zu geraten. Werden diese Rezeptoren jedoch überaktiv, unteraktiv oder anders verschaltet, können sie verzerren, wie belohnend Nahrung wirkt, wie hungrig wir uns fühlen und wie viel Schmerz oder Stress wir wahrnehmen.
Wie natürliche Opioide Überessen und Fettleibigkeit antreiben können
Bei Fettleibigkeit scheinen sich die Belohnungsschaltkreise des Gehirns in einer Weise umzuformen, die Veränderungen ähnelt, wie sie durch suchterzeugende Drogen entstehen. Opioidrezeptoren in einem wichtigen Belohnungsknoten, dem Nucleus accumbens, fördern das Verlangen, schmackhafte, fettreiche und zuckerreiche Nahrungsmittel zu suchen und zu genießen. Genetische Studien deuten darauf hin, dass bestimmte Varianten des mu-Opioidrezeptor-Gens manche Menschen vor Gewichtszunahme schützen können, während andere Muster der Genregulation mit Fettleibigkeit verbunden sind. Experimente an Nagetieren zeigen, dass das Blockieren von Opioidrezeptoren die Attraktivität süßer, fettreicher Diäten verringert, während das Entfernen dieser Rezeptoren Tiere resistenter gegen diätinduzierte Fettleibigkeit machen kann. Gleichzeitig zeigen Menschen mit Fettleibigkeit oft eine geringere Verfügbarkeit von mu-Opioidrezeptoren im Belohnungssystem, aber höhere Werte in hypothalamischen Regionen, die Hunger und Sättigung messen — ein Hinweis auf eine langfristige Verschiebung darin, wie das Gehirn Nahrung bewertet und reguliert.
Wenn dasselbe System Selbstverhungern unterstützt
Anorexia nervosa, äußerlich das Gegenteil von Fettleibigkeit, beinhaltet ebenfalls veränderte Opioidsignale. Genetische Studien weisen wiederholt auf das delta-Opioidrezeptor-Gen als Risikofaktor hin, und bildgebende Verfahren zeigen insgesamt reduzierte Verfügbarkeit von Opioidrezeptoren in Regionen, die Belohnung, Angst und Abneigung verarbeiten. Eine langjährige Theorie besagt, dass Hungern bei anfälligen Personen einen sich selbst verstärkenden "Rausch" auslöst: Durch Diäten und intensives Training freigesetzte körpereigene Opioide dämpfen Stress und erzeugen emotionale Erleichterung, was weiteren Gewichtsverlust eher begünstigt als normales Wiederauffüllen. Tiermodelle, in denen Nahrungsbeschränkung mit freiwilligem Laufen kombiniert wird, zeigen ähnliche Muster — Hyperaktivität, Gewichtsverlust und Anzeichen dafür, dass das Opioidsystem auf einen so hohen Basisspiegel getrieben wurde, dass externe Opioide ihre Wirkung verlieren. Wichtig ist, dass das Blockieren von Opioidrezeptoren in einigen Studien Patienten mit Anorexie beim Zunehmen zu helfen scheint und Nagetiere dazu anregt, fettreichere Nahrung zu sich zu nehmen, was auf einen potenziellen Behandlungsansatz hinweist.
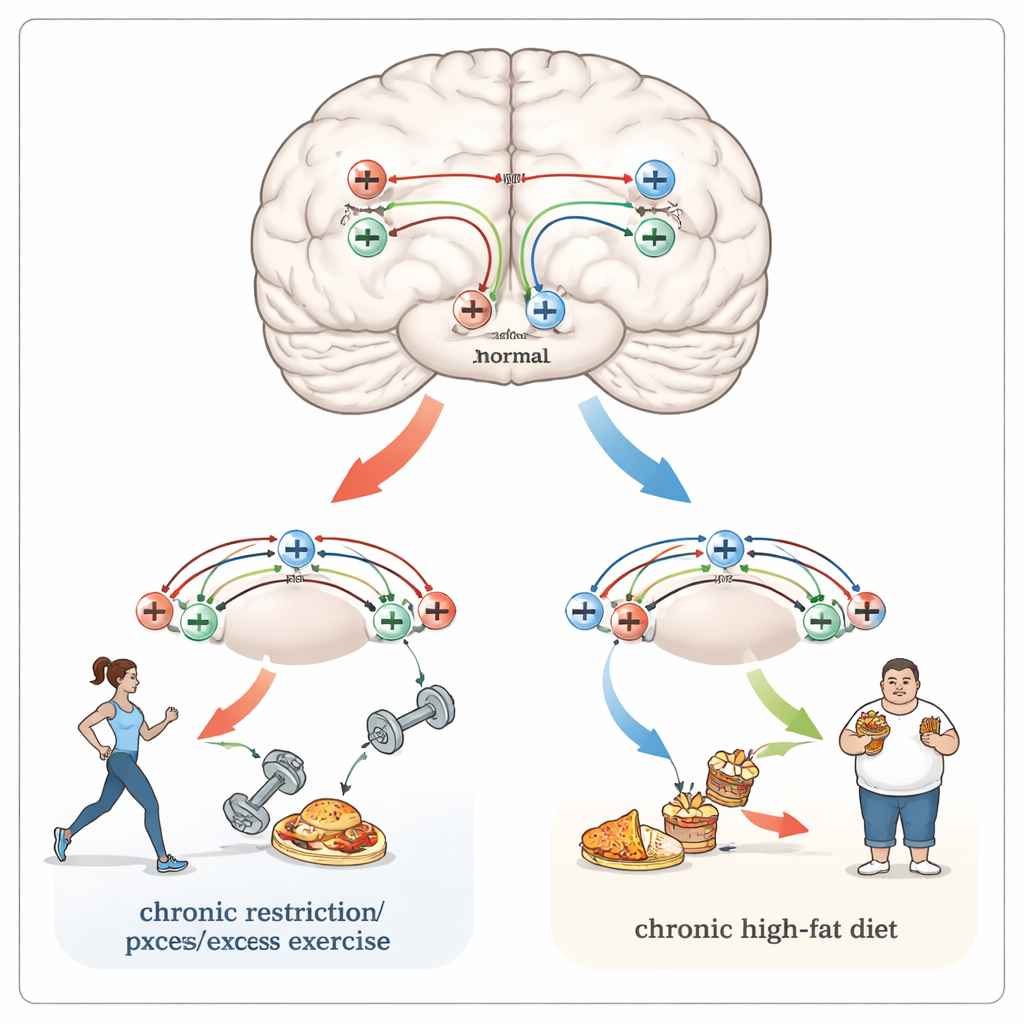
Geteilte Verbindungen zu Schmerz, Sucht und starren Gewohnheiten
Die gleichen Hirnregionen und Rezeptoren, die das Essen formen, verarbeiten auch Schmerz und Drogenbelohnung. Menschen mit Fettleibigkeit neigen dazu, mehr Schmerzen zu erleben, einschließlich Migräne, während Personen mit langjähriger Anorexie häufig eine abgeschwächte Reaktion auf schmerzhafte Reize zeigen. Natürliche Opioide können in Regionen wie Hypothalamus, Hirnstamm und Nucleus accumbens sowohl Schmerzen mildern als auch die Aufmerksamkeit auf dringende Bedürfnisse wie Hunger lenken. Diese Schaltkreise überschneiden sich mit Pfaden, die durch suchterzeugende Drogen umgestaltet werden, und chronische Nahrungsbeschränkung erhöht in Tierstudien die Empfindlichkeit gegenüber Substanzen wie Opioiden. Sowohl Fettleibigkeit als auch Anorexie sind außerdem mit verminderter kognitiver Flexibilität verbunden — der Fähigkeit, Gewohnheiten an neue Umstände anzupassen — was tiefere, langanhaltende Veränderungen an Verbindungen zwischen Nervenzellen widerspiegeln kann, die teilweise durch Opioidrezeptoren getrieben werden.
Was das für das Verständnis und die Behandlung extremes Essverhaltens bedeutet
Insgesamt legt die Evidenz nahe, dass das körpereigene Opioidsystem mitbestimmt, ob Änderungen im Essverhalten — etwa durch den Konsum reichhaltiger Lebensmittel oder Phasen des Diätens — vorübergehend und adaptiv bleiben oder sich zu langfristigen, schädlichen Mustern auswachsen. Bei Fettleibigkeit scheint wiederholtes Überessen Belohnungs- und Hungerschaltkreise so umzubauen, dass kalorienreiche Nahrungsmittel besonders anziehend werden. Bei Anorexie können Hunger und exzessives Training dieselben opioidgetriebenen Lernprozesse kapern, sodass Selbstverweigerung und Hyperaktivität trotz gefährlichem Gewichtsverlust als belohnend erlebt werden. Indem man genauer bestimmt, wo und wie sich diese Rezeptoren verändern, argumentieren die Autoren, könnte künftige Forschung präzisere Behandlungen leiten — etwa gezielte Rezeptorblocker, Hirnstimulation oder Medikamente, die synaptische Plastizität normalisieren — um die Festmahl-oder-Hungern-Schaltkreise des Gehirns wieder ins Gleichgewicht zu bringen.
Zitation: Sutton Hickey, A.K., Matikainen-Ankney, B.A. Endogenous opioid receptors and the feast or famine of maladaptive feeding. Nat Commun 16, 2270 (2025). https://doi.org/10.1038/s41467-025-57515-0
Schlüsselwörter: endogene Opioide, Essstörungen, Fettleibigkeit, Anorexia nervosa, Belohnungsschaltkreise im Gehirn