Clear Sky Science · de
Bio-inspirierte Elektronik: Weiche, biohybride und „lebende“ neuronale Schnittstellen
Sanfte Geräte für das Nervensystem
Von Gehirn‑Computer‑Schnittstellen, die Menschen erlauben, Roboterarme zu bewegen, bis zu Tiefenhirnstimulatoren, die Parkinson‑Symptome lindern: Elektronik, die mit unseren Nerven kommuniziert, wandelt sich schnell von Science‑Fiction zu medizinischer Realität. Dennoch sind heutige Geräte im Kern weiterhin Stücke aus Metall und Silizium, die in Gewebe eingebracht werden, das so weich wie Pudding ist. Diese Übersicht erläutert, wie Wissenschaftler diese Werkzeuge neu gestalten, damit sie dem Körper ähnlicher sind — weicher, biologisch aktiver und teils sogar lebendig — in der Hoffnung, neuronale Implantate sicherer, langlebiger zu machen und die Fähigkeit zu geben, Gehirn und Nerven bei der Heilung zu unterstützen.
Warum herkömmliche Implantate nicht ausreichen
Konventionelle neuronale Implantate, etwa Utah‑Arrays und Tiefenhirnstimulations‑Sonden, bestehen aus starren Metallen und Silizium. Diese Materialien sind millionenfach steifer als Hirngewebe, das eher wie Gelee als wie Glas reagiert. Dieser Unterschied macht es schwierig, dass sich Geräte an die feinen Bewegungen und Formen des Gehirns anpassen. Wenn das Gewebe sich bei jedem Herzschlag und Atemzug verschiebt, reiben und ziehen steife Elektroden und verursachen winzige Verletzungen. Der Körper erkennt diese Fremdkörper und reagiert mit einer Immunantwort, indem er sie in eine dichte Narbe aus Stützzellen einschließt. Im Laufe der Zeit erhöht diese Narbe den elektrischen Widerstand zwischen dem Gerät und den umliegenden Neuronen, verschlechtert die Signalqualität und begrenzt, wie lange ein Implantat zuverlässig funktionieren kann.
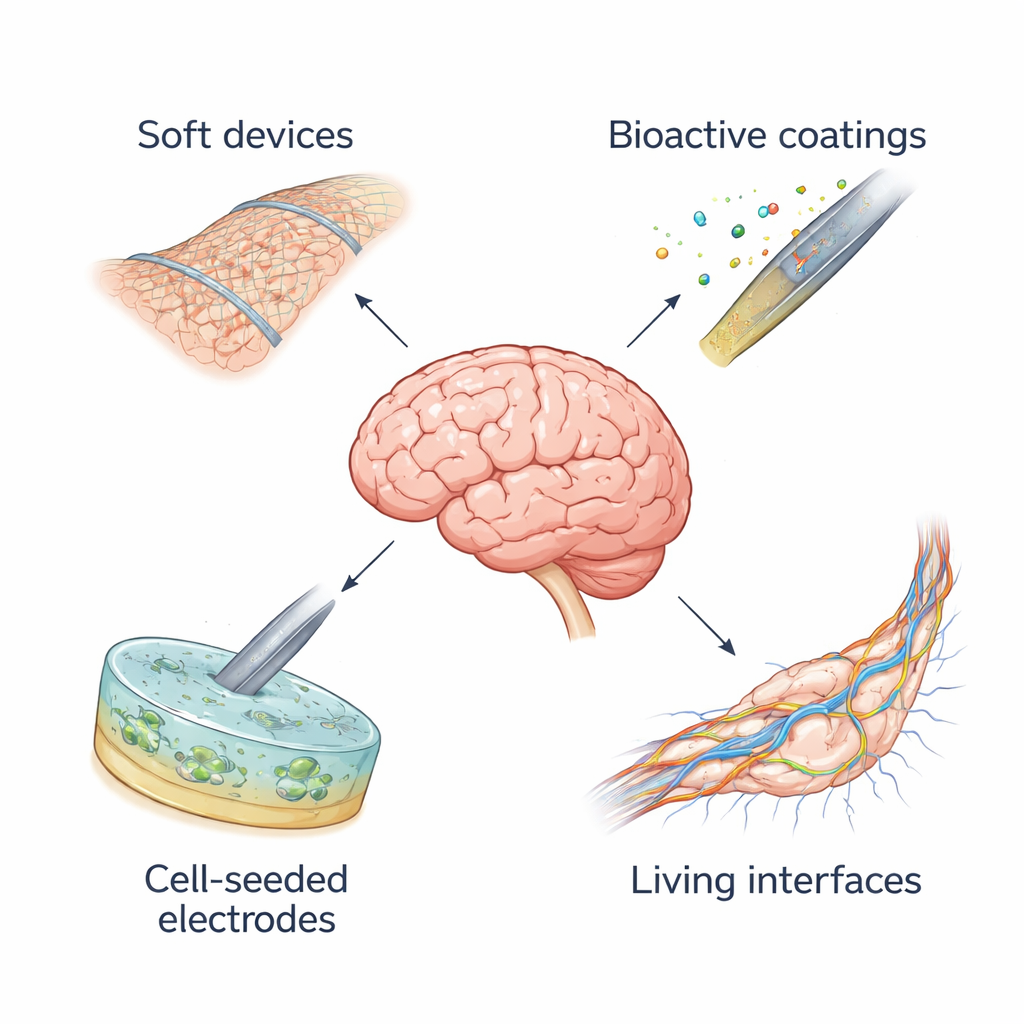
Weiche Geräte, die mit dem Gehirn mitbewegen
Um diesen Schaden zu verringern, bauen Forschende „biomimetische" Elektronik — Geräte, deren physikalische Eigenschaften den Gewebeeigenschaften nachempfunden sind. Statt dicker, starrer Schäfte fertigen Ingenieurinnen und Ingenieure heute ultradünne Filme, flexible Fasern und offene Netzstrukturen, die wie lebende Zellen biegen und sich rollen können. Weiche Polymere, dehnbare Kautschuke und wasserreiche Gele gleichen die Weichheit des Gehirns an und dämpfen die Kräfte, die Entzündungen auslösen. Einige dieser Geräte verweben leitfähige Kunststoffe oder Nanomaterialien wie Graphen in flexible Rückgrate, bewahren hochwertige elektrische Aufzeichnungen und senken gleichzeitig die Steifigkeit drastisch. Mehrere weiche Schnittstellen, darunter fadenförmige Gehirnimplantate und dünne Foliengitter, die auf der Hirnoberfläche liegen, gelangen bereits in klinische Studien am Menschen und zeigen, dass sanftere Mechanik mit fortschrittlicher Elektronik koexistieren kann.
Oberflächen, die Zellen einladen statt sie abzuweisen
Die Geräte weicher zu machen, ist nur ein Teil der Lösung. Auch die Zellen des Gehirns reagieren auf das chemische „Gefühl“ einer Implantatoberfläche. Bioaktive Elektronik nutzt dies, indem Elektroden mit biologischen Komponenten beschichtet werden, die das Nervensystem bereits kennt und vertraut, etwa Proteine aus der natürlichen Matrix, die Zellen umgibt, oder kurze Moleküle, die Nervenwachstum fördern. Diese Beschichtungen können Neuronen dazu anregen, näher an Elektroden heranzuwachsen, die Aktivität von Immunzellen dämpfen und die üblicherweise entstehende Narbe verringern. Manche Beschichtungen sind so gestaltet, dass sie Wirkstoffe wie Entzündungshemmer oder Wachstumsfaktoren langsam genau dort freisetzen, wo sie gebraucht werden, und so einen passiven Draht in eine intelligente, Arzneimittel‑freisetzende Schnittstelle verwandeln. Die Herausforderung besteht darin, diese empfindlichen Schichten jahrelang stabil und wirksam im Körper zu halten.
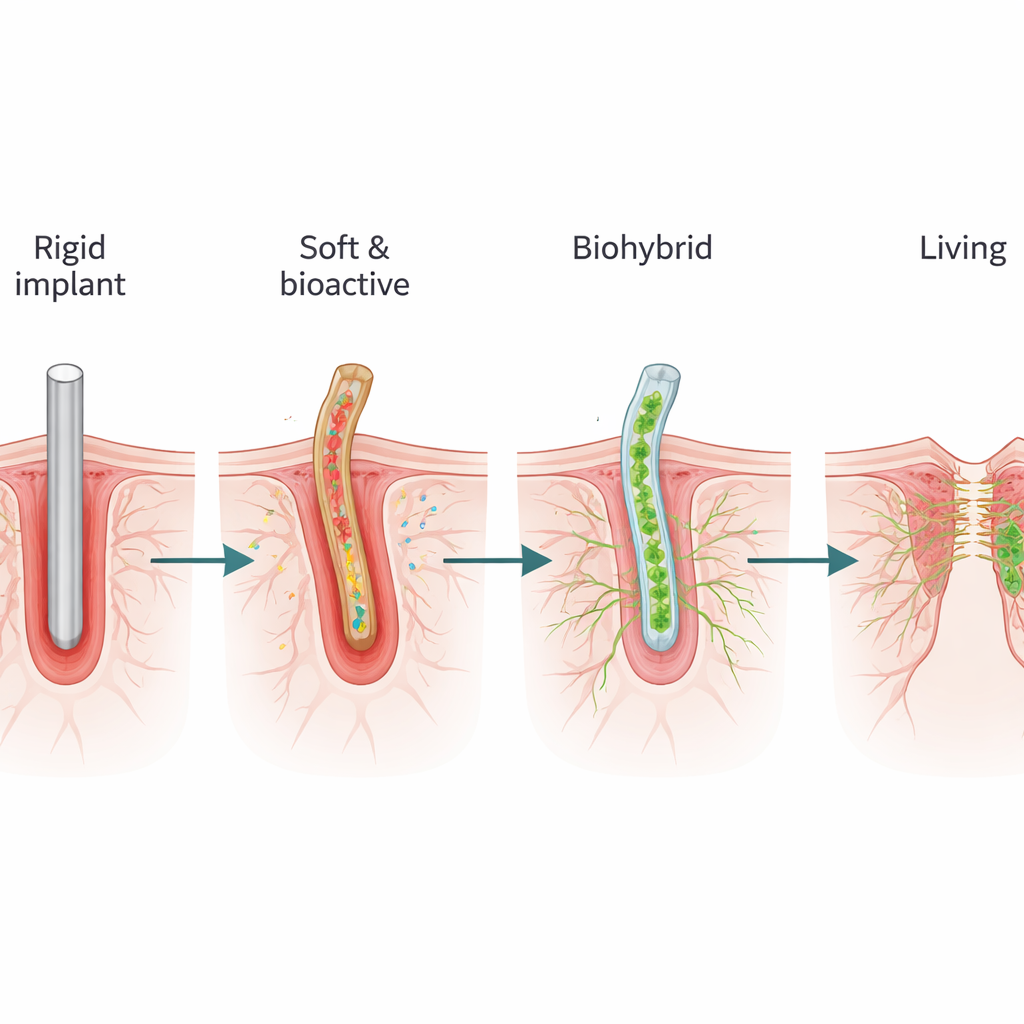
Lebende Zellen mit Schaltkreisen verschmelzen
Weiter entlang des Spektrums integrieren „biohybride" Geräte echte lebende Zellen in oder auf die Elektronik. Bei einer Strategie werden Zellen vor der Implantation auf Elektroden kultiviert, manchmal innerhalb eines weichen Hydrogels, das Hirngewebe nachahmt. Einmal im Körper, kann diese lebende Schicht hilfreiche Moleküle sezernieren, Nervenfasern anziehen und eine biologische Brücke zwischen starrer Hardware und Wirtsgewebe bilden. Frühe Versionen, wie konusförmige Elektroden, die Nervenfasern anlockten, lieferten in Menschen über ein Jahrzehnt stabile Aufzeichnungen. Neuere Ansätze besiedeln Elektroden mit Stammzellen, Nervenzellen oder Muskelzellen und zielen nicht nur darauf ab, Aktivität zu lesen oder zu stimulieren, sondern auch beschädigte Bahnen zu regenerieren und verlorene Funktionen wiederherzustellen, etwa Bewegung nach Nervenschäden. Diese Systeme müssen schwierige Probleme lösen: Zellen am Leben erhalten, ihr Wachstum lenken und verhindern, dass sie sich unerwünscht ausbreiten oder falsche Verbindungen bilden.
Vollständig lebende „Leitungen“ fürs Gehirn
Am ambitioniertesten sind „lebende Schnittstellen“, die vollständig aus biologischen Materialien und Zellen bestehen. Hier dienen im Labor herangezüchtete lange Bündel von Nervenfasern als lebende Kabel, die implantiert werden können, um Hirnregionen wieder zu verbinden oder Lücken in verletzten Nerven zu überbrücken. Statt Strom durch Metall zu leiten, nutzen diese Konstrukte natürliche Synapsen — die Kontaktstellen zwischen Neuronen — zur Signalübertragung. Im Gehirn wurden solche lebenden Bahnen so entwickelt, dass sie bestimmte chemische Nachrichten transportieren, etwa Dopamin, was Hoffnungen weckt, Erkrankungen wie Parkinson zu behandeln, indem verlorene Schaltkreise wiederaufgebaut werden, anstatt Symptome nur mit elektrischen Impulsen zu überdecken. Da diese Geräte vollständig biologisch sind, integrieren sie sich gut mit dem Wirtsgewebe, verlangen aber neue Wege zu ihrer Überwachung und Kontrolle, die oft auf lichtbasierte Bildgebung und Stimulation statt auf traditionelle Drähte bauen.
Was das für die künftige Gehirn‑ und Nervenversorgung bedeutet
Weiche, bioaktive, biohybride und vollständig lebende Schnittstellen skizzieren zusammen eine Roadmap hin zu neuronalen Technologien, die mit dem Körper kooperieren, statt ihm entgegenzuwirken. Sanftere Mechanik und freundlichere Oberflächen können Vernarbung reduzieren und die Lebensdauer von Geräten verlängern; lebende Zellen und schließlich ganze Gewebepfade könnten Implantate dazu befähigen, beschädigte Schaltkreise zu reparieren oder zu ersetzen, nicht nur von ihnen zu messen. Für zellhaltige und komplett lebende Systeme bleiben viele wissenschaftliche, fertigungstechnische und regulatorische Hürden. Doch die Richtung ist klar: Die Implantate von morgen werden weniger wie starre Gadgets aussehen und sich eher wie sorgfältig entworfene Stücke lebenden Gewebes verhalten.
Zitation: Boufidis, D., Garg, R., Angelopoulos, E. et al. Bio-inspired electronics: Soft, biohybrid, and “living” neural interfaces. Nat Commun 16, 1861 (2025). https://doi.org/10.1038/s41467-025-57016-0
Schlüsselwörter: neuronale Schnittstellen, biohybride Elektronik, weiche Implantate, Gehirn‑Computer‑Schnittstelle, Gewebeengineering