Clear Sky Science · de
Kategorisierung von 34 rechnerischen Methoden zur Erkennung räumlich variabler Gene aus räumlich aufgelösten Transkriptomikdaten
Warum der Ort für unsere Gene wichtig ist
Unser Körper besteht aus Zellen, die sich nicht nur in ihrer Funktion unterscheiden, sondern auch darin, wo sie in Geweben und Organen sitzen. Neue "räumliche Transkriptomik"-Technologien können nun ablesen, welche Gene aktiv sind, und gleichzeitig die Position jeder Zelle auf einer Gewebekarte festhalten. Dieser Übersichtsartikel erklärt, wie Forscher Gene erkennen, deren Aktivität sich von Ort zu Ort verändert — sogenannte räumlich variable Gene — und warum Einigkeit darüber, wie man sie findet, zentral dafür ist, Krebs, Gehirnfunktionen und viele andere Krankheiten besser zu verstehen.
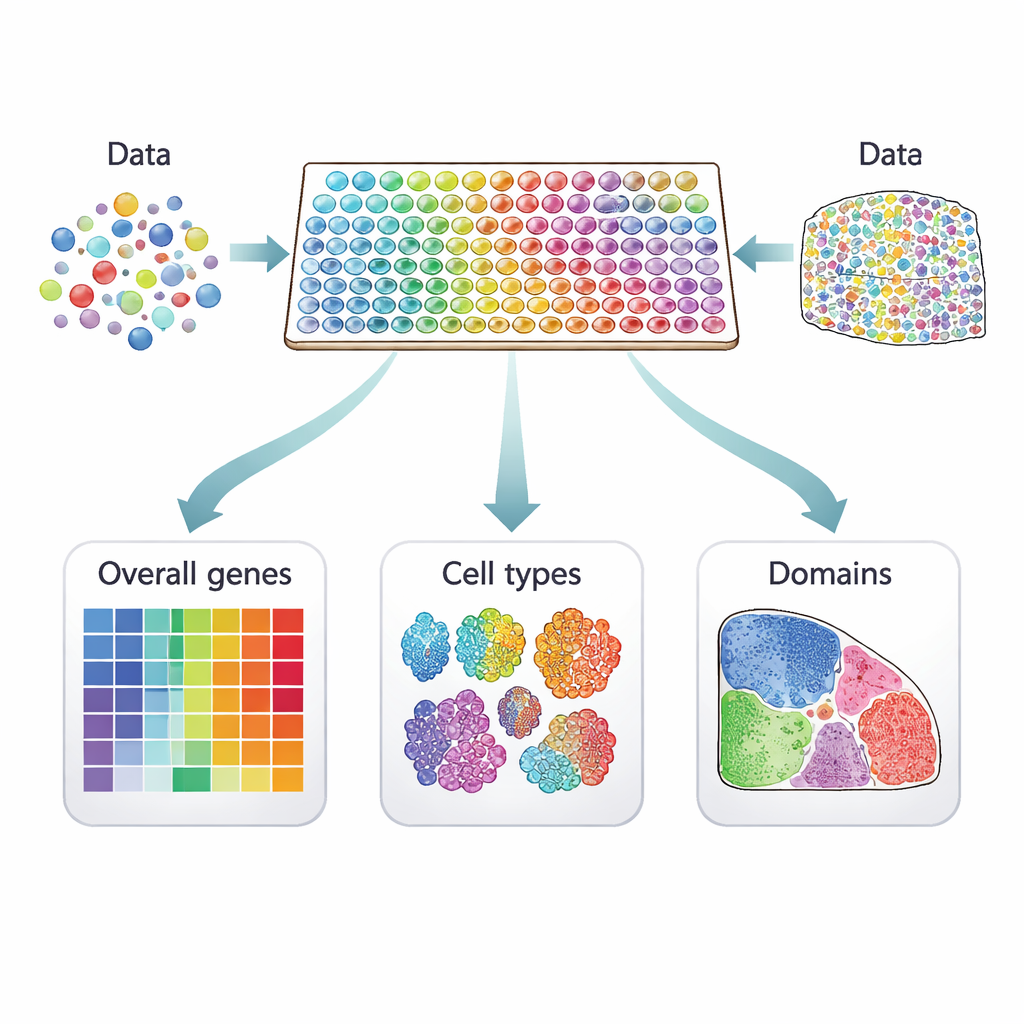
Von verstreuten Zellen zu lebendigen Karten
Traditionelle Einzelzellstudien messen die Genaktivität in Tausenden einzelner Zellen, verlieren dabei aber die Information, wo diese Zellen herkamen. Räumliche Transkriptomik schließt diese Lücke, indem sie Genaktivität direkt auf dünnen Gewebeschnitten misst. Jede Messung ist an einen "Punkt" auf dem Schnitt gebunden, der je nach Technologie eine oder mehrere Zellen enthalten kann. Bildgebende Verfahren lokalisieren einige hundert ausgewählte Gene mit sehr hoher räumlicher Auflösung, während sequenzbasierte Plattformen nahezu alle Gene mit geringerer Auflösung erfassen. Zusammen verwandeln diese Ansätze einen Gewebeschnitt in eine bunte Karte der Genaktivität, die verborgene Strukturen offenbaren kann, etwa Schichten im Gehirn oder Regionen innerhalb eines Tumors.
Drei Arten ortssensitiver Gene
Viele rechnerische Methoden wurden vorgeschlagen, um Gene herauszufiltern, die in diesen Gewebekarten sinnvolle Muster zeigen; sie suchen dabei jedoch nicht alle nach demselben Merkmal. Die Autoren ordnen 34 aktuelle Methoden in drei klare Kategorien ein. Die erste Gruppe sucht nach "übergreifenden" räumlich variablen Genen, deren Aktivität sich auf nicht‑zufällige Weise über das Gewebe verändert — etwa in Streifen, Clustern oder Gradienten. Die zweite Gruppe konzentriert sich auf "zelltyp‑spezifische" räumliche Gene, die innerhalb eines einzelnen Zelltyps variieren und etwa helfen, Subtypen von Neuronen oder unterschiedliche Zustände von Immunzellen zu unterscheiden. Die dritte Gruppe sucht nach "Domänenmarker"-Genen, die in bestimmten Regionen oder Schichten stark aktiviert sind und sich somit als Kennzeichen dieser Gewebeareale eignen.
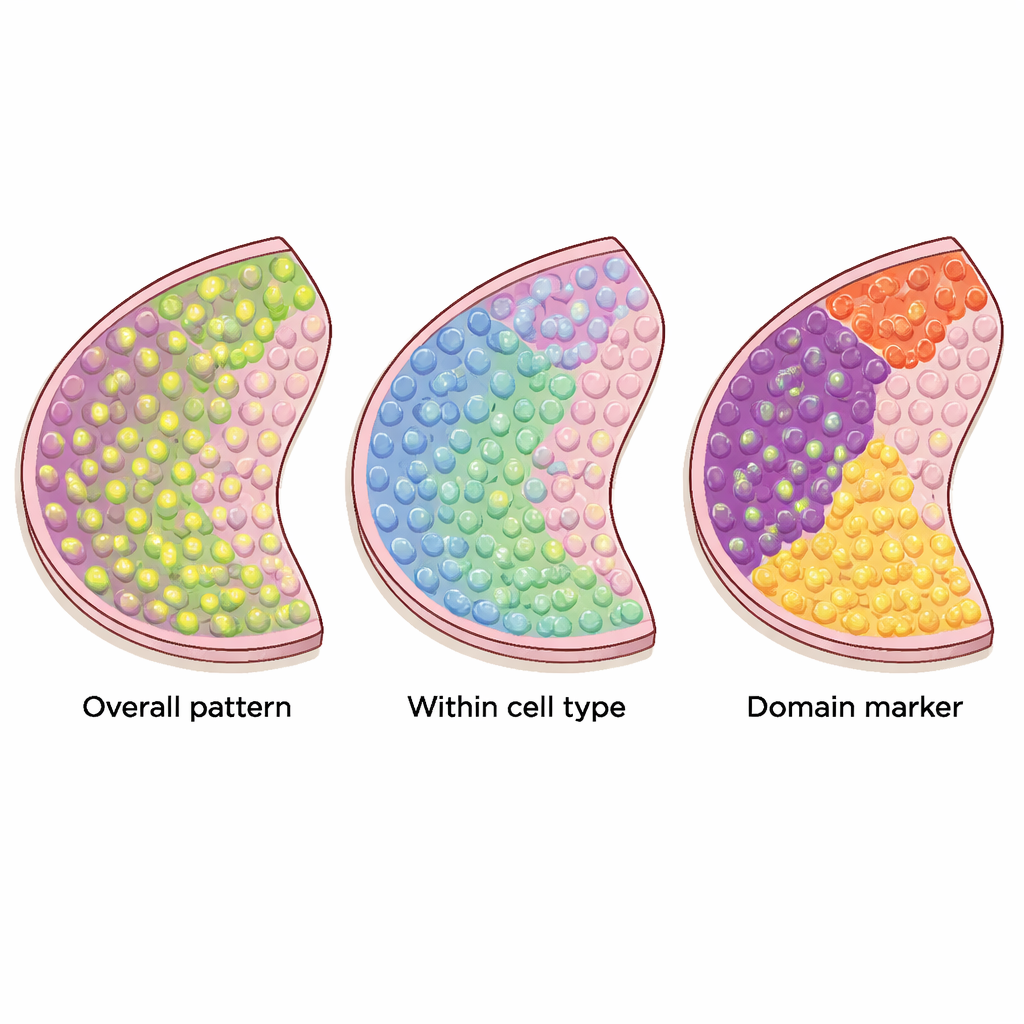
Verschiedene Werkzeuge für verschiedene Muster
Der Review erklärt, wie diese Methoden im Detail arbeiten. Einige behandeln den Gewebeschnitt als Punkte in regulärem zweidimensionalem Raum und verwenden mathematische "Kernel", um Muster wie Punkte oder Wellen zu erkennen. Andere verknüpfen zunächst benachbarte Orte zu einem Netzwerk oder Graphen und prüfen dann, ob hohe Expressionen entlang der Verbindungen dieses Graphen gehäuft auftreten. Bestimmte Werkzeuge stützen sich auf formale statistische Tests mit klar definierten Fehlerraten, während andere Gene vorwiegend danach ordnen, wie stark ihre Muster hervorstechen. Methoden, die sehr spezifische Muster anvisieren, können stark sein, wenn die Daten ihren Annahmen entsprechen, doch sie können unregelmäßigere oder komplexere Formen übersehen, wie sie etwa in vielen Tumoren vorkommen. Es gibt zudem einen Zielkonflikt zwischen Flexibilität und Geschwindigkeit: Manche Ansätze skalieren bis zu Hunderttausenden von Punkten, während andere mit sehr großen Datensätzen Schwierigkeiten haben.
Was diese Gene offenbaren können
Sind räumlich variable Gene einmal identifiziert, dienen sie als Ausgangsmaterial für tiefere biologische Entdeckungen. Übergreifende räumliche Gene werden häufig als erste Filter genutzt, um die Zahl der Gene zu reduzieren, bevor Punkte in "räumliche Domänen" gruppiert werden — Regionen, deren Zellen ähnliche Expressionsprofile teilen. Diese Domänen können mit bekannten Gewebestrukturen übereinstimmen, neue Unterregionen vorschlagen oder bestimmte Zellnachbarschaften hervorheben, etwa Invasionsfronten in Tumoren. Domänenmarker-Gene helfen dann zu erklären, was jede Region einzigartig macht, und lassen sich verwenden, um ähnliche Strukturen in anderen Proben zu kennzeichnen. Zelltyp‑spezifische räumliche Gene versprechen zudem eine feinere Sicht darauf, wie sich bestimmte Zelltypen über ein Gewebe verändern, was tumor‑immunologische Interaktionen oder spezialisierte Schaltkreise im Gehirn erhellen kann.
Herausforderungen und der weitere Weg
Die Autoren betonen, dass keine einzelne Methode für jede Aufgabe die beste ist und dass ein fairer Vergleich von Werkzeugen sorgfältiges Nachdenken darüber erfordert, nach welcher Art räumlicher Gene eine Methode tatsächlich sucht. Sie fordern bessere Benchmarks mit realistischen Datensätzen, klarere statistische Standards zur Vermeidung falscher Entdeckungen und neue Ansätze, die Unterschiede zwischen Technologien und Gewebearten berücksichtigen. Für Nicht‑Experten lautet die Hauptbotschaft: Räumlich variable Gene verwandeln flache Genlisten in lebendige Karten und verknüpfen molekulare Aktivität mit Gewebestruktur. Robuste Methoden, diese Gene zu erkennen und zu interpretieren, werden zentral sein, um die räumliche Transkriptomik in praxisrelevante Einsichten über Entwicklung, Gehirnfunktion und Krankheit zu überführen.
Zitation: Yan, G., Hua, S.H. & Li, J.J. Categorization of 34 computational methods to detect spatially variable genes from spatially resolved transcriptomics data. Nat Commun 16, 1141 (2025). https://doi.org/10.1038/s41467-025-56080-w
Schlüsselwörter: räumliche Transkriptomik, räumlich variable Gene, Expressionsmuster von Genen, Gewebemikroumgebungen, computationale Genomik