Clear Sky Science · de
Die Wirkung der N‑terminalen Acetylierung erhellen: vom Protein zur Physiologie
Wie winzige chemische Markierungen das Verhalten von Proteinen verändern können
Jede Zelle in Ihrem Körper ist voller Proteine, die korrekt falten, an den richtigen Ort gelangen, sich zu molekularen Maschinen zusammenlagern und bei Schädigung wieder entfernt werden müssen. Dieser Übersichtsartikel beleuchtet eine subtile, aber äußerst häufige chemische Veränderung an einem Ende vieler Proteine – die sogenannte N‑terminale Acetylierung – und zeigt, wie diese kleine „Kappe“ alles steuert, von Zellwachstum und Stressreaktionen bis hin zur Herzentwicklung und Gehirnfunktion.
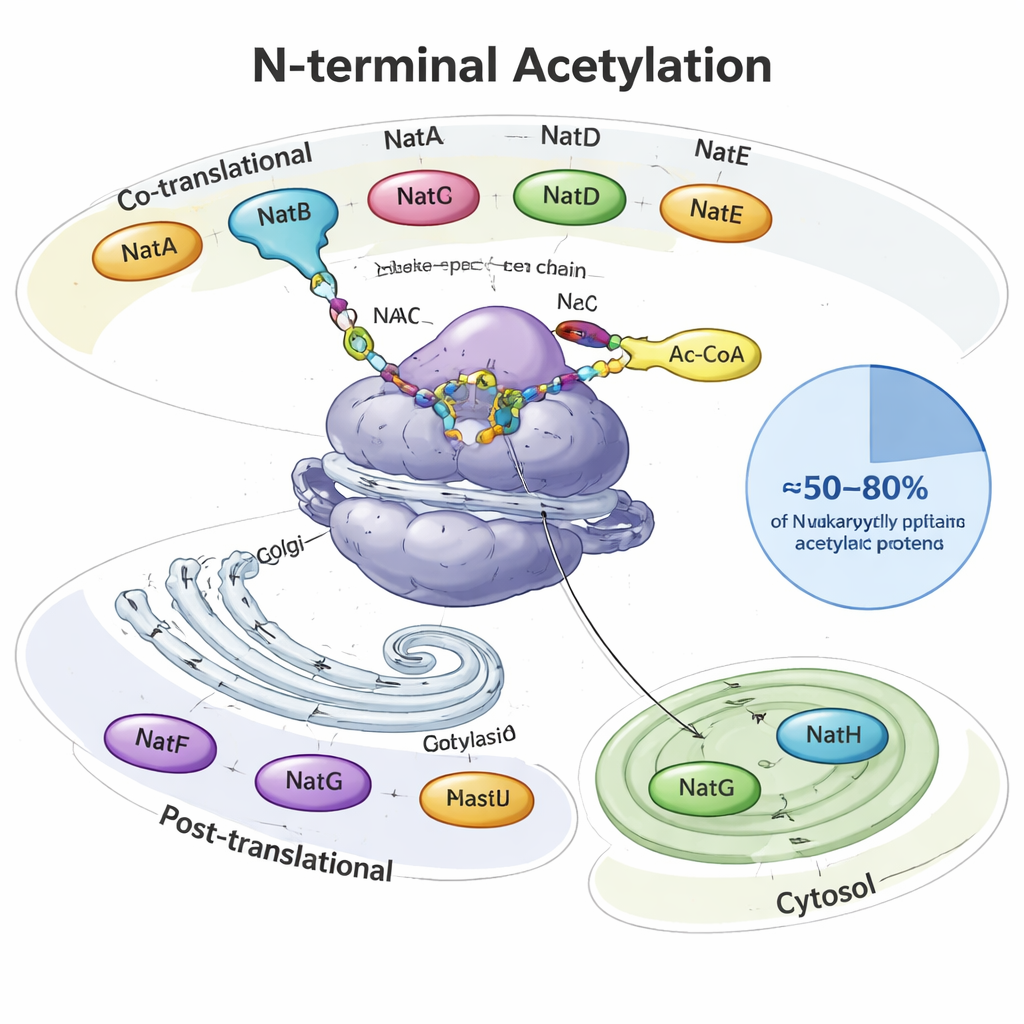
Die Proteinkappe, von der die meisten nie gehört haben
Wenn ein Protein hergestellt wird, tritt es aus der zellulären Proteinfabrik, dem Ribosom, wie ein wachsender Faden heraus. Ganz am Anfang – der N‑Terminustelle – erhalten viele eukaryotische Proteine eine Acetylgruppe, eine winzige Zweikohlenstoff‑Kappe. Spezialisierte Enzyme, die N‑terminale Acetyltransferasen (NATs) genannt werden, führen diese Reaktion aus und nutzen das verbreitete Stoffwechselmolekül Acetyl‑CoA als Donor. In Hefen, Pflanzen und Tieren teilen acht Haupttypen von NATs (NatA–NatH) die Arbeit untereinander auf. Einige wirken noch während der Proteinsynthese, andere arbeiten nachträglich und sind an bestimmten Orten stationiert, etwa am Golgi‑Apparat oder in Pflanzenplastiden. Zusammengenommen modifizieren sie etwa die Hälfte bis vier Fünftel aller zellulären Proteine, wobei jede NAT bevorzugte N‑Startsequenzen von zwei bis vier Aminosäuren erkennt.
Viele Enzyme, jeweils mit eigener Spezialität
NatA, NatB und NatC sind die Hauptakteure; sie wirken direkt am Ribosom und decken große Bereiche des „N‑terminalen Acetyloms“ ab. Allein NatA kann etwa 40 % der menschlichen Proteine modifizieren, meist solche, deren erste Methionin entfernt wurde. NatB und NatC wirken an Proteinen, die ihr initiales Methionin behalten, unterscheiden sich jedoch in den benachbarten bevorzugten Aminosäuren. Andere NATs sind selektiver: NatD konzentriert sich auf nur wenige Histonproteine, die die DNA verpacken; NatF zielt auf Transmembranproteine am Golgi; NatG arbeitet in Pflanzenplastiden; und NatH (NAA80) vollendet einen speziellen zweistufigen Reifungsprozess an Aktin, einem Hauptbestandteil des zellulären Zytoskeletts. Der Artikel fasst strukturelle und biochemische Studien zusammen, die zeigen, wie Hilfssubstanzen diese Enzyme am Ribosom oder an Membranen verankern und die Zielauswahl feinjustieren.
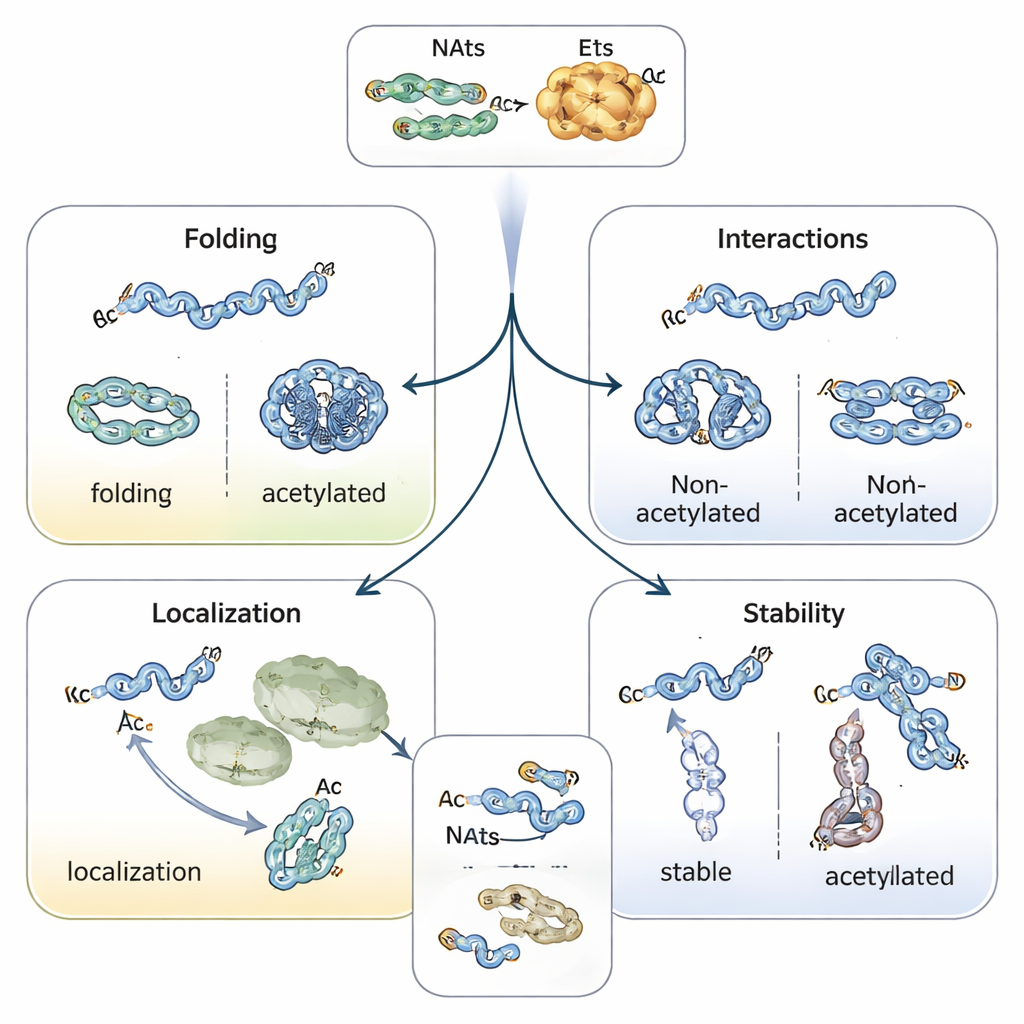
Protein‑Faltung, Lokalisation und Lebensdauer steuern
Das Anfügen einer Acetylkappe verändert die chemischen Eigenschaften des Proteinanfangs, stabilisiert häufig helikale Strukturen und beeinflusst die Faltung. Beispielsweise neigt das mit Parkinson assoziierte Protein Alpha‑Synuclein bei N‑terminaler Acetylierung weniger zum Verklumpen und nimmt eine stabilere Konformation ein. Tropomyosin, ein Partner von Aktin, bindet und reguliert Aktinfilamente deutlich besser, wenn es korrekt acetylieret ist. In Pflanzen und Tieren kann die N‑terminale Acetylierung als eine Art Adressetikett dienen, das Proteinen hilft, Chloroplasten, Lysosomen oder das Golgi zu finden. Am deutlichsten ist ihre Rolle bei der Bestimmung der Lebensdauer von Proteinen: Ein ungeschützter N‑Terminus kann von Ubiquitinierungsenzymen als „Abbausignal“ gelesen werden, während Acetylierung dieses Signal maskieren und das Protein stabilisieren kann – oder in einigen Fällen ein bedingtes Erkennungsmerkmal schafft, das nur sichtbar wird, wenn das Protein fehlgefaltet ist oder nicht im richtigen Komplex liegt.
Von der Zellphysiologie zu Entwicklung und Krankheit
Da die N‑terminale Acetylierung so viele Proteine betrifft, haben Störungen der NATs weitreichende Konsequenzen für ganze Organismen. Das Entfernen von NatA, NatB oder NatC in Modellorganismen führt oft zu schweren Entwicklungsdefekten, veränderten Stressreaktionen oder sogar zum Tod, während spezialisiertere Enzyme wie NatF und NatH engere Probleme verursachen, etwa Hirnverkalkungen oder Hörverlust. Beim Menschen liegen vererbte Mutationen in mehreren NAT‑Genen seltenen neuro‑entwicklungsbedingten Syndromen mit geistiger Behinderung, Herzfehlern oder Muskelschwäche zugrunde. Dieselben Maschinen sind in Krebs häufig überaktiv; erhöhte NAT‑Spiegel korrelieren mit schlechter Prognose und können Tumorwachstum, Metastasierung und Therapieresistenz fördern. Veränderungen der N‑terminalen Acetylierung beeinflussen auch aggregationsempfindliche Proteine wie Alpha‑Synuclein und Huntingtin und verknüpfen diese Modifikation mit Mechanismen neurodegenerativer Erkrankungen.
Zukünftige Richtungen und therapeutisches Potenzial
Die Autoren schließen, dass wir zwar die meisten Kernenzyme kennen, die diese N‑terminalen Kappen anbringen, aber noch immer nur einen Bruchteil der spezifischen Proteinziele und Regulationsregeln verstehen. Ein zentrales Thema ist, dass Acetylierung am Proteinanfang oft vor vorzeitigem Abbau schützt, zugleich aber kontextabhängige Signale für die Qualitätskontrolle erzeugen kann. Zu klären, welche Ubiquitinligasen welche N‑terminalen Muster lesen, und ob es Enzyme gibt, die diese Kappen wieder entfernen können, sind wichtige offene Fragen. Da NATs an der Schnittstelle von Proteinstabilität, Genregulation und zellulären Stressreaktionen sitzen, gelten selektive NAT‑Inhibitoren – und möglicherweise künftige Werkzeuge, die die N‑terminale Acetylierung bestimmter krankheitsrelevanter Proteine gezielt verändern – als vielversprechende Ansätze für neue Therapien bei Krebs, Herzkrankheiten und Neurodegeneration.
Zitation: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Schlüsselwörter: Proteinmodifikation, N‑terminale Acetylierung, Protein‑Qualitätskontrolle, neurodegenerative Erkrankung, Krebsbiologie