Clear Sky Science · de
m6A-RNA-Methylierung moduliert die antivirale Antwort bei Zöliakie
Wenn ein Virus und Gluten zusammenwirken
Zöliakie wird häufig als ein einfaches Ernährungsproblem angesehen: Gluten essen und der Darm wird geschädigt. Diese Studie offenbart jedoch eine tiefere Geschichte, in der ein verbreiteter Darvirus und ein winziges chemisches Markierungszeichen auf unseren RNA-Molekülen zusammenarbeiten, um das Immunsystem in Richtung dauerhafter Schädigung zu treiben. Das Verständnis dieser verborgenen Kontrollschicht kann erklären, warum nur manche Menschen Zöliakie entwickeln, und auf neue Behandlungsansätze jenseits der glutenfreien Ernährung hinweisen. 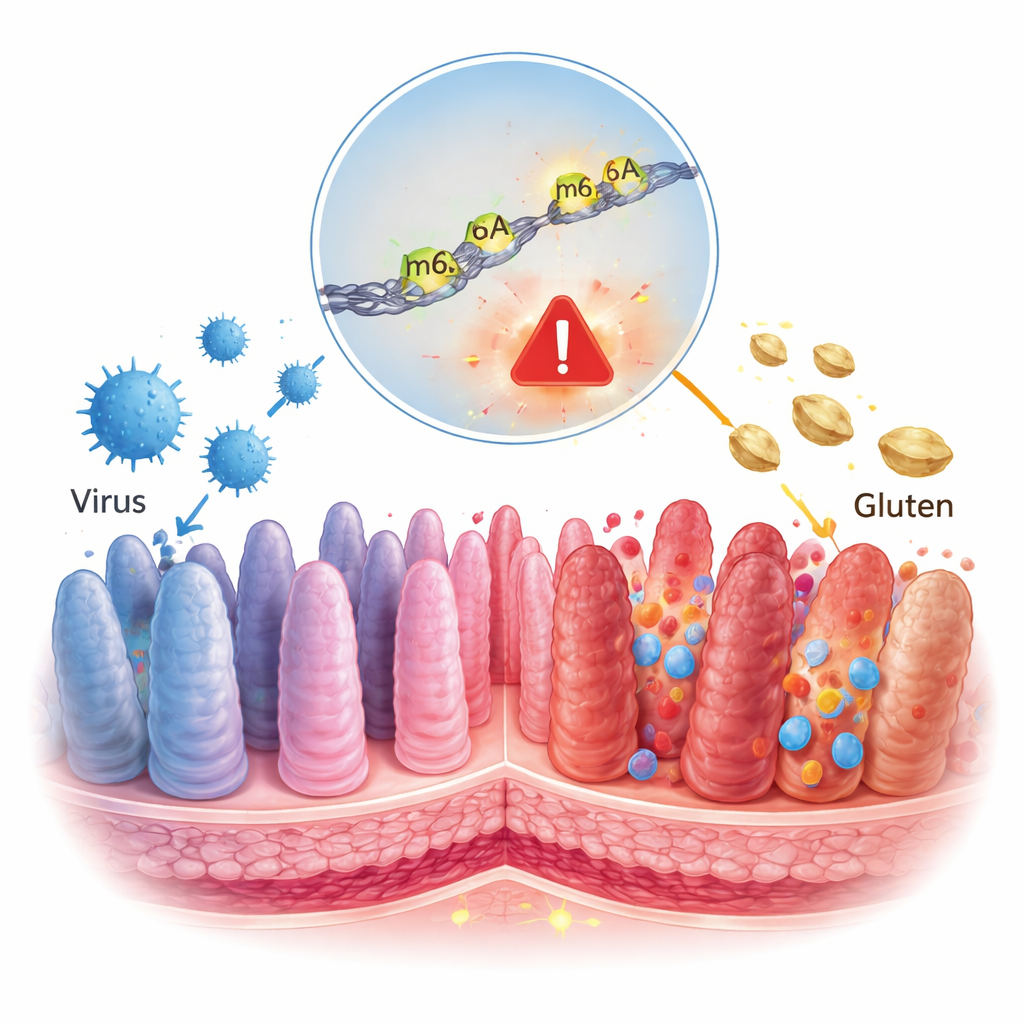
Ein verborgenes Zeichen auf unseren genetischen Botschaften
Unsere Zellen lesen ständig Gene und kopieren sie in RNA, kurze „Botschaften“, die der Zelle sagen, welche Proteine hergestellt werden sollen. Diese Botschaften sind nicht unveränderlich; sie können mit chemischen Markierungen versehen werden, die wie Textmarker wirken und beeinflussen, wie stark eine Botschaft gelesen wird. Eine der häufigsten Markierungen heißt m6A, eine winzige Änderung an den RNA-Bausteinen. Es ist bekannt, dass Viren diese RNA-Markierungen in infizierten Zellen verändern, und frühere Arbeiten hatten bereits einen Zusammenhang zwischen m6A und der Art und Weise gezeigt, wie Gluten Entzündungen im zöliakischen Darm auslöst. Die Autorinnen und Autoren dieser Arbeit fragten, ob eine virusbedingte Veränderung von m6A helfen könnte, das Immunsystem von Nahrungsmitteltoleranz auf Angriff umzuschalten.
Hinweise aus Proben von Patientinnen und Patienten mit Zöliakie
Die Forschenden untersuchten zunächst Blut- und Darmbiopsien von Menschen mit aktiver Zöliakie und von Nicht-Zöliakie-Kontrollen. Sie fanden, dass Zöliakie-Patienten erhöhte Antikörperspiegel gegen Reovirus trugen, ein doppelsträngiges RNA-Virus, das den Darm infiziert, was auf häufigere oder stärkere Exposition hindeutet. Im Darmgewebe dieser Patientinnen und Patienten waren wichtige antivirale Warngene, insbesondere IRF7, auf höheren Niveaus aktiviert, zusammen mit entzündlichen Molekülen wie STAT1 und dem Immunzell-Anlockungsmolekül CXCL10. Gleichzeitig war die Maschinerie, die m6A-Markierungen anbringt und liest, aktiver, und die Gesamtmenge an m6A auf der RNA war erhöht. Die Expression antiviraler Gene stieg und fiel parallel zu m6A-verwandten Genen, was darauf hindeutet, dass dasselbe Kontrollsystem sowohl die Virusabwehr als auch autoimmune Schäden antreiben könnte.
Wie Gluten den viralen Alarm verstärkt
Um Ursache und Wirkung zu klären, bauten die Forscher ein zöliakieähnliches Modell in im Labor gezüchteten Darmzellen auf. Sie ahmten eine Virusinfektion mit einer synthetischen doppelsträngigen RNA nach und fügten dann verdautete Glutenfragmente hinzu, ähnlich denen, die nach einer Mahlzeit im Darm vorkommen würden. Der virale Imitator erhöhte allein sowohl IRF3 als auch IRF7, zwei Schaltstellen für antivirale Antworten. Wurde jedoch zusätzlich Gluten zugegeben, zeigte IRF7 einen deutlich stärkeren Anstieg, während IRF3 das nicht tat. Die Forschenden entdeckten, dass unter diesen Bedingungen m6A-Markierungen in einem bestimmten Bereich der IRF7-RNA zunahmen und dass diese RNA physisch mit einem m6A-Schreibenzym (METTL3) und einem Entfernungsenzym (ALKBH5) interagierte. Eine Erhöhung von m6A, entweder durch verstärkte METTL3-Zufuhr oder durch Reduktion von ALKBH5, trieb die IRF7-Spiegel weiter in die Höhe und verband so die Gluten‑und‑Virus-Synergie direkt mit dieser RNA-Modifikation. 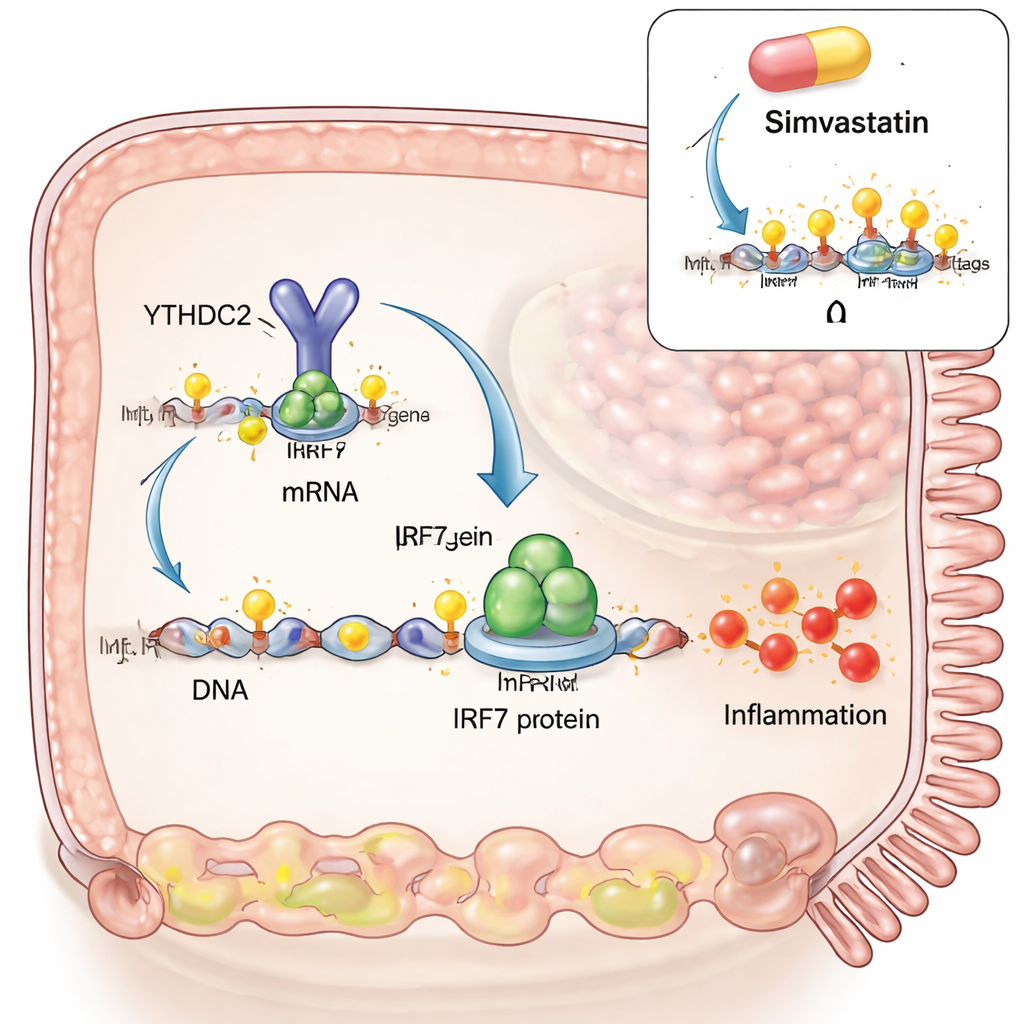
Der molekulare Vermittler und ein überraschendes Medikament
Als Nächstes untersuchten die Autorinnen und Autoren, wie m6A-Markierungen auf der IRF7-RNA das zelluläre Verhalten tatsächlich verändern. Sie konstruierten eine Version der IRF7-RNA mit demselben Proteincode, aber ohne die m6A-Stellen. Diese RNA erzeugte ähnliche Mengen an Transkript, aber deutlich weniger IRF7-Protein und löste keine nachgeschalteten entzündlichen Gene wie STAT1 und CXCL10 aus. Die fehlende Verbindung war ein Leserprotein namens YTHDC2, das normalerweise m6A innerhalb des protein-kodierenden Bereichs bindet und die effiziente Translation in Protein fördert. Ohne die m6A-Stellen konnte YTHDC2 nicht mehr an die IRF7-RNA binden. Das Blockieren des m6A-Schreibers METTL3 im Zellmodell reduzierte IRF7-Protein und CXCL10 und senkte so die Entzündungsantwort. Ein cholesterinsenkendes Medikament, Simvastatin, das kürzlich in anderen Geweben gezeigt wurde, m6A zu reduzieren, verminderte ebenfalls m6A auf der IRF7-RNA, senkte IRF7-Protein in Zellen und dämpfte IRF7-assoziierte Gene in frisch entnommenen zöliakischen Darmbiopsien, die ex vivo kultiviert wurden. Groß angelegte Vergleiche der Genexpressionsprofile deuteten darauf hin, dass Simvastatin das Gewebe von Zöliakie-Patienten in Richtung eines Profils verschiebt, das eher dem von Patientinnen und Patienten auf glutenfreier Diät ähnelt.
Was das für Menschen mit Zöliakie bedeutet
Diese Arbeit zeichnet das Bild, dass ein Darvirus und Gluten zusammen auf einer fein abgestimmten Ebene der RNA-Kontrolle wirken. Bei anfälligen Personen scheint eine Virusinfektion die m6A-Markierung der IRF7-RNA in Darmzellen zu verstärken. Glutenexposition potenziert dieses markierte Signal weiter, was zu mehr IRF7-Protein, stärkeren antiviralen Alarmen und höheren Mengen entzündlicher Botenstoffe führt, die den autoimmune Angriff auf die Darmschleimhaut vorantreiben. Durch das Absenken der m6A-Markierungen — entweder genetisch oder mit einem Medikament wie Simvastatin — lässt sich die Kettenreaktion zumindest in Labor- und ex vivo-Modellen abschwächen. Für Laien ist die zentrale Botschaft, dass Zöliakie nicht nur von der Nahrung abhängt, sondern auch davon, wie Infektionen und subtile chemische Markierungen auf RNA die Entscheidung des Immunsystems zwischen Toleranz und Angriff beeinflussen. Das Anvisieren dieser RNA-Markierungen könnte eines Tages die glutenfreie Diät ergänzen und neue Behandlungen für ein breiteres Spektrum autoimmuner Erkrankungen inspirieren.
Zitation: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Schlüsselwörter: Zöliakie, RNA-Methylierung, antivirale Immunität, IRF7, Simvastatin