Clear Sky Science · de
CRISPR-AuNP: physikochemische Optimierung einer Goldnanopartikel-Plattform für kostengünstiges und modulares nicht-virales Gen-Editing in HSPCs
Gene Editing für mehr Patientinnen und Patienten zugänglich machen
Geneditierwerkzeuge wie CRISPR haben bereits das Leben von Menschen mit erblichen Blutkrankheiten verändert; die Behandlungen sind jedoch weiterhin teuer, technisch anspruchsvoll und größtenteils auf einige wenige spezialisierte Zentren beschränkt. Dieser Artikel beschreibt eine neue Methode, CRISPR in blutbildende Stammzellen zu bringen, mithilfe winziger goldbasierter Partikel, die in nur wenigen Stunden auf einer Laborbank zusammengesetzt werden können. Ziel ist es, leistungsfähige Geneditieransätze einfacher, günstiger und leichter in mehr Regionen der Welt einsetzbar zu machen.
Warum Blutstammzellen wichtig sind
Blutbildende Stamm- und Vorläuferzellen sitzen im Knochenmark und erneuern kontinuierlich alle verschiedenen Blutzelltypen im Körper. Wenn Ärztinnen und Ärzte krankheitsverursachende Mutationen in diesen Zellen sicher beheben können, könnte eine einmalige Behandlung eine lebenslange Heilung für Erkrankungen wie Sichelzellanämie und bestimmte Immundefekte bieten. Bislang erfolgt die gängigste Methode, CRISPR in diese Zellen zu bringen, über Elektroporation — ein Verfahren, das elektrische Pulse nutzt, um Öffnungen in Zellmembranen zu erzeugen. Obwohl wirksam, ist Elektroporation belastend für die Zellen, erfordert teure Geräte und spezialisierte Reagenzien und lässt sich nur schlecht skalieren oder in ressourcenarmen Umgebungen einsetzen. Sicherere virale Vektoren sind für viele Gentherapien exzellent, eignen sich jedoch weniger gut für CRISPR, weil sie die Editierwerkzeuge über einen zu langen Zeitraum produzieren und so das Risiko von unbeabsichtigten Veränderungen erhöhen.
Ein winziges goldbasiertes Transportsystem bauen
Die Forschenden wollten ein zuvor beschriebenes Goldnanopartikel-System verbessern, das CRISPR-Komponenten an seiner Oberfläche trug. In früheren Designs wurde die RNA, die das CRISPR-Schneiderprotein zum Ziel führt, direkt am Goldkern verankert und anschließend mit dem Cas9-Protein gekoppelt. Das funktionierte bei einem CRISPR-Enzym-Typ einigermaßen, zeigte jedoch schlechte Ergebnisse mit Cas9, das für viele therapeutische Strategien zentral ist. Durch genaue Untersuchungen, wie Cas9 und seine Leit-RNA unter den sauren Bedingungen der Partikelassemblierung reagieren, fanden die Autorinnen und Autoren heraus, dass das RNA-Duplex auf der Goldoberfläche instabil wurde, sodass wenig bis kein aktives Cas9 am Partikel haftete. Konfokale Mikroskopie deutete außerdem darauf hin, dass die Polymerbeschichtung, die den Partikeln beim Entkommen aus zellulären Kompartimenten helfen sollte, sich ablöste, bevor sie ihre Funktion erfüllen konnte.
Schrittweise Neuentwicklung der Plattform
Um diese Probleme zu beheben, bauten die Wissenschaftlerinnen und Wissenschaftler das System in drei Stufen von Grund auf neu auf. Zunächst formten sie statt das nackte RNA an das Gold zu verankern komplette CRISPR-Ribonukleoproteinkomplexe (Protein plus Leit-RNA), bevor sie diese mit der Goldoberfläche in Kontakt brachten. Sie identifizierten eine leicht saure Bedingung, die es diesen Komplexen erlaubte, an die Partikel zu binden, während das Schneiderprotein aktiv blieb. Anschließend umhüllten sie die beladenen Partikel mit speziell entwickelten Polymeren, die positiv geladene Ketten—nötig für das Entkommen aus zellulären Kompartimenten—mit flexiblen, wasserliebenden Polyethylenglykolsegmenten kombinierten, die das Verklumpen verhindern. Durch Messungen von Größe, Oberflächenladung und Proteingehalt zeigten sie, dass sich reproduzierbar dutzende CRISPR-Komplexe pro Partikel laden ließen, während die Stabilität in Lösung erhalten blieb.
Die Abwehr der Zelle überwinden
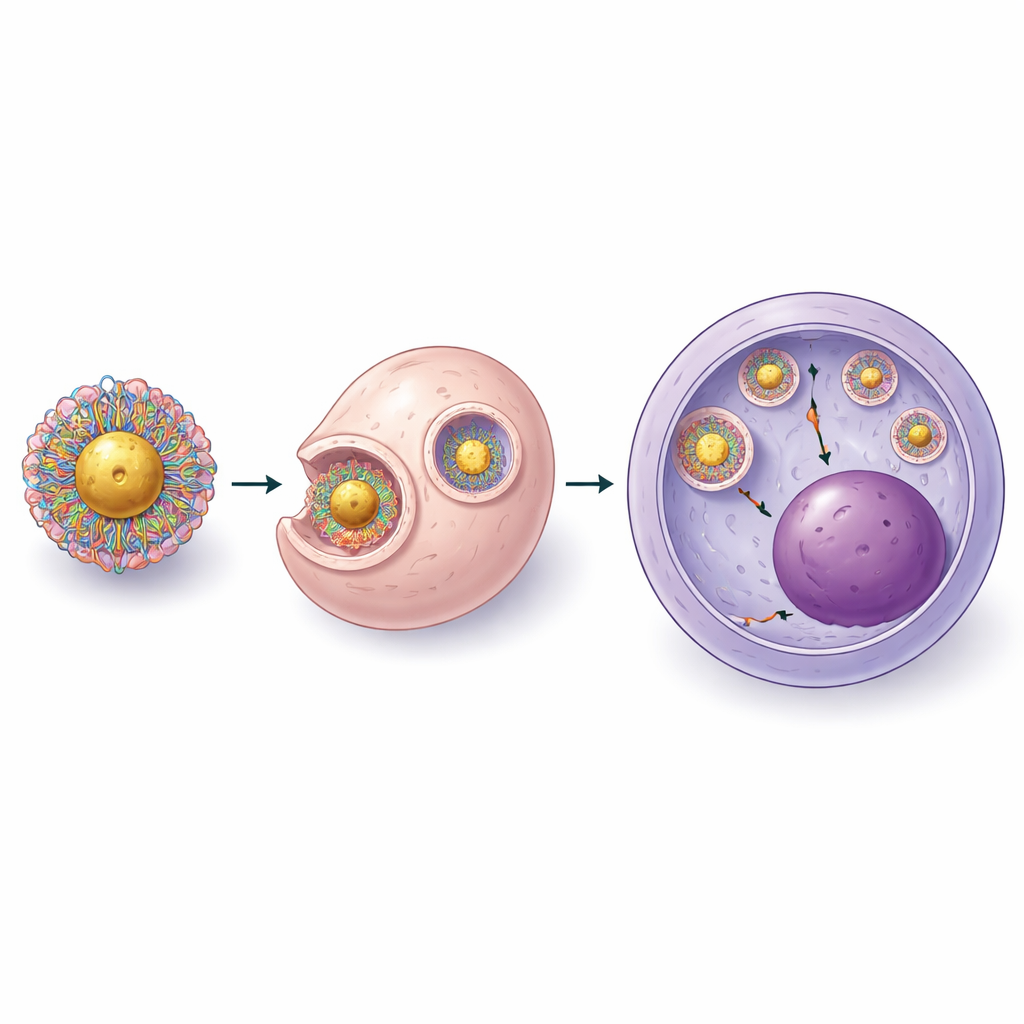
Selbst mit verbesserter Beladung hatten die Partikel der zweiten Generation noch ein zentrales Problem: CRISPR aus den intrazellulären Vesikeln in den Zellkern zu bringen, wo die DNA liegt. Daher justierte das Team systematisch die Chemie der Polymerbeschichtung und das Verhältnis zwischen positiven Gruppen am Polymer und negativen Gruppen am CRISPR-Komplex. Sie entdeckten, dass das Hinzufügen von mehr kurzen Polyethylenglykol-Ketten und einer kontrollierten Anzahl schwefelhaltiger Anker sowohl die Partikelstabilität als auch die Fähigkeit verbesserte, endosomale Membranen zu stören, ohne die Zellen zu schädigen. Im finalen, dritten Generationen-Design bildeten sie zunächst kompakte Komplexe aus CRISPR und Polymer und befestigten diese dann an konzentrierten Goldkernen. Elektronenmikroskopie zeigte eine dünne Schicht aus CRISPR und Polymer um jede Goldkugel, und Live-Zell-Bildgebung in Stammzellen bestätigte, dass die Fracht aus den Kompartimenten entkommen und den Zellkern erreichen konnte.
Editorische Ergebnisse mit verschiedenen CRISPR-Werkzeugen
Um die Wirksamkeit der optimierten Partikel zu prüfen, zielten die Forschenden auf ein Gen namens Beta-2-Mikroglobulin, das ein Protein produziert, das auf der Oberfläche nahezu aller Blutzellen zu finden ist und leicht mittels Durchflusszytometrie gemessen werden kann. Mit ihrer Goldplattform der dritten Generation erreichten sie in primären humanen blutbildenden Stamm- und Vorläuferzellen mehr als 10 % präzise Disruptionen dieses Gens—Werte, die für viele therapeutische Anwendungen als bedeutsam gelten—bei gleichzeitiger hoher Zellüberlebensrate. Zwar liegt diese Effizienz unter der von Elektroporation erreichbaren, doch erforderte das Goldsystem keine spezialisierten Geräte und belastete die Zellen nur minimal. Wichtig ist, dass dieselbe Plattform mit unterschiedlichen CRISPR-Proteinen verwendbar war, einschließlich Cas9, Cas12a und einem neueren Enzym namens Cas12a-M29-1, mit ähnlichen Editierniveaus und keiner nachweisbaren Toxizität, was die modulare Natur des Designs unterstreicht.
Was das für künftige Therapien bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass es möglich ist, einen kleinen, sorgfältig konstruierten goldbasierten Träger zu bauen, der CRISPR-Werkzeuge in empfindliche Blutstammzellen bringen kann—ohne Strom oder Viren—unter Verwendung handelsüblicher Materialien für weniger als siebzig Dollar pro Million Zellen. Während weitere Verbesserungen nötig sind, um die Effizienz der derzeit besten klinischen Methoden zu erreichen, insbesondere für Krankheiten, die sehr hohe Anteile korrigierter Zellen erfordern, senkt diese am Labortisch zusammengesetzte Plattform praktische Hürden für anspruchsvolles Gen-Editing. Mit fortgesetzter Verfeinerung und Sicherheitstests könnten solche Nanopartikel dazu beitragen, die Vorteile CRISPR-basierter Therapien über spezialisierte Zentren hinaus zu verbreiten und heilende Behandlungen für Patientinnen und Patienten weltweit besser zugänglich zu machen.
Zitation: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Schlüsselwörter: CRISPR-Geneditierung, Goldnanopartikel, hämatopoetische Stammzellen, nicht-virale Lieferung, Nanomedizin