Clear Sky Science · de
Genomik der facioscapulohumeralen Muskeldystrophie im Telomere‑to‑Telomere‑Zeitalter neu denken: Fallstricke in der verborgenen Landschaft der D4Z4‑Repeats
Warum diese Geschichte über eine Muskelerkrankung wichtig ist
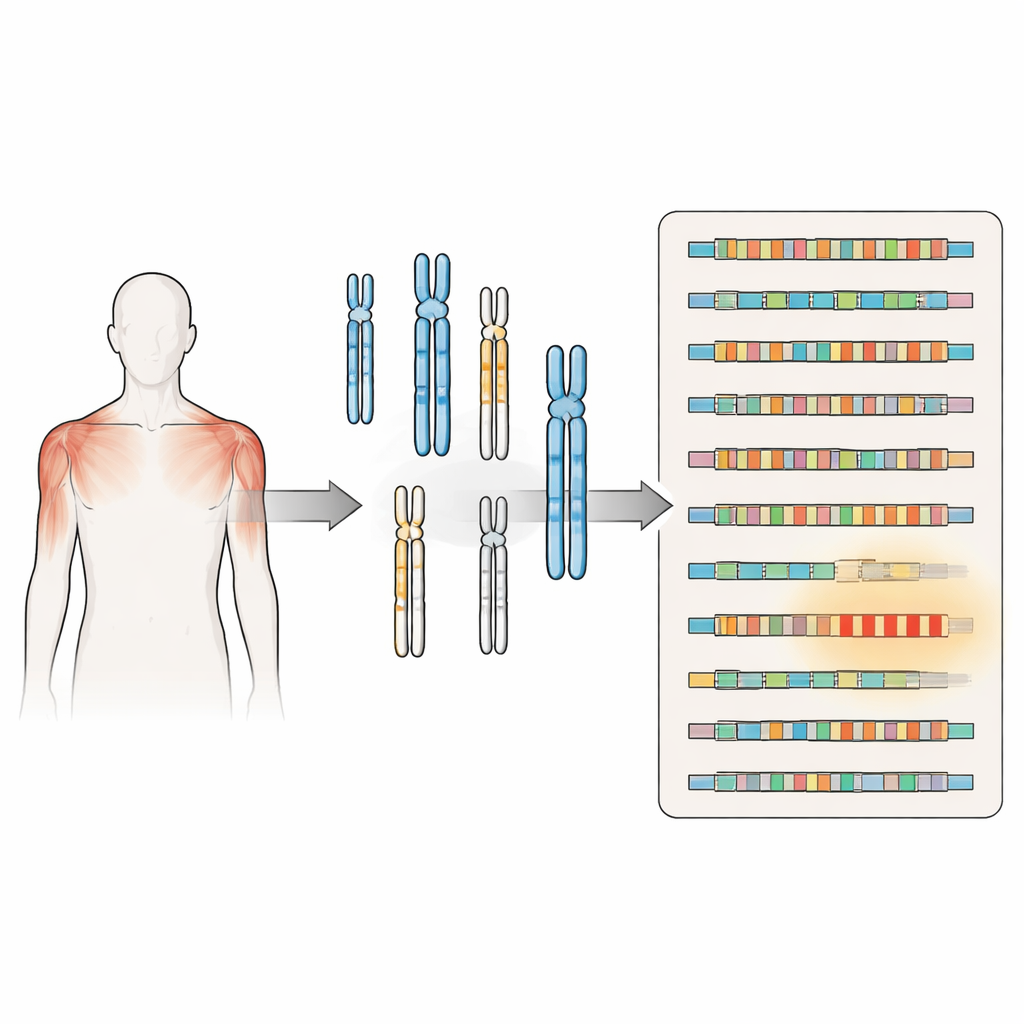
Die facioscapulohumerale Muskeldystrophie (FSHD) gehört zu den häufigsten erblichen Muskelschwundkrankheiten und schwächt oft die Gesichtsmuskulatur und Schultermuskeln ansonsten gesunder junger Erwachsener. Jahrelang konzentrierten sich Forscher auf einen einzigen DNA‑Abschnitt nahe der Spitze von Chromosom 4 als Verursacher. Diese neue Studie zeigt, dass das Bild viel komplexer ist: Ähnliche DNA‑Repeats sind im gesamten Genom verstreut, und viele gebräuchliche Labortests können sie nicht voneinander unterscheiden. Das Verständnis dieser verborgenen Landschaft ist entscheidend für eine genaue Diagnose, bessere Forschung und letztlich sicherere Therapien.
Ein näherer Blick auf eine rätselhafte Muskelerkrankung
FSHD wird seit langem mit der Verkürzung einer wiederholten DNA‑Sequenz namens D4Z4 am Ende von Chromosom 4 in Verbindung gebracht. Wenn dieser Repeat‑Bereich unter eine bestimmte Größe schrumpft und auf einem bestimmten genetischen Hintergrund liegt, erlaubt er die Produktion eines Proteins namens DUX4, das Muskelzellen schädigen kann. Eine zweite Form der Erkrankung entsteht, wenn Gene mutiert sind, die normalerweise diesen Bereich eng verpackt und still halten; auch hier wird DUX4 wieder möglich. Beide Wege laufen auf dasselbe Problem hinaus: Ein Gen, das im erwachsenen Muskel größtenteils abgeschaltet sein sollte, wird sporadisch aktiv und trägt so zu Muskelschwäche und -abbau bei.
Verborgene Repeats im gesamten Genom
Frühere Karten des menschlichen Genoms waren unvollständig, besonders in Bereichen mit vielen Wiederholungen an Chromosomenenden und in der Nähe von Zentromeren. Mit der neuen Telomere‑to‑Telomere‑Human‑Genomassemblierung, die diese Lücken schließt, durchsuchten die Autoren das gesamte Genom erneut mithilfe der D4Z4‑Sequenz von Chromosom 4 als Suchvorlage. Sie entdeckten Cluster und isolierte Kopien D4Z4‑ähnlicher Repeats auf mindestens zehn weiteren Chromosomen. Einige dieser Repeats sind strukturell vollständig und liegen neben Signalen, die DUX4‑ähnliche RNAs stabilisieren könnten, was darauf hindeutet, dass sie unter bestimmten Bedingungen verwandte Proteine oder RNA‑Moleküle produzieren könnten.
Wenn Labortests mehr als einen Ort gleichzeitig sehen
FSHD‑Forschung und Diagnostik stützen sich häufig auf Tests, die bestimmte DNA‑ oder RNA‑Fragmente mit kurzen Primersequenzen vervielfältigen — eine Strategie, die als PCR bekannt ist. Diese Primer wurden ursprünglich unter der Annahme entworfen, dass D4Z4‑Repeats nur auf den Chromosomen 4 und 10 vorkommen. Durch die Kombination von Computervorhersagen mit Experimenten an Zellen, die einzelne menschliche Chromosomen tragen, zeigen die Autoren, dass viele weit verbreitete Primersätze nicht nur an die krankheitsassoziierte Region auf Chromosom 4 binden, sondern auch an ähnlich aussehende Repeats im ganzen Genom. Primer, die auf das wichtige DUX4‑Exon oder auf benachbarte lange nicht-kodierende RNAs abzielen, amplifizieren häufig Produkte von mehreren Chromosomen gleichzeitig, sodass nicht mehr festgestellt werden kann, woher ein bestimmtes Signal wirklich stammt.
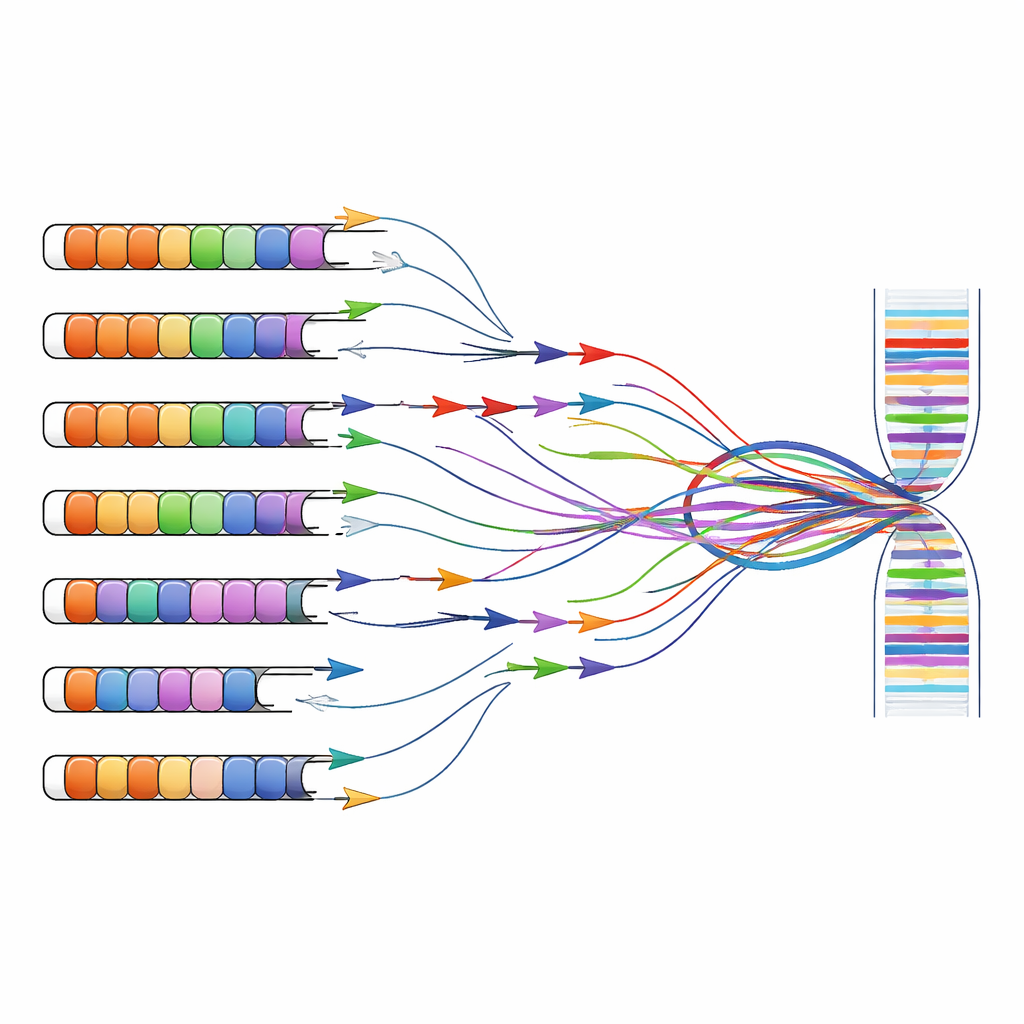
Diagnostische und Forschungswerkzeuge neu überdenken
Dieses Multi‑Orts‑Problem reicht über die Grundlagenforschung hinaus bis in die Klinik. Neuere Tests, die DNA‑Methylierung messen (eine chemische Markierung, die mit Genstilllegung assoziiert ist) oder kurzen‑Read‑Sequenzierung verwenden, fassen häufig Signale vieler nahezu identischer Repeats zusammen. Infolgedessen können Messungen von „D4Z4‑Methylierung“ oder „DUX4‑Transkripten“ in öffentlichen Datensätzen tatsächlich ein Gemisch von Beiträgen von Chromosom 4, Chromosom 10 und anderen Stellen widerspiegeln. Die Autoren argumentieren, dass Forscher zur korrekten Zuordnung genetischer Veränderungen zu Symptomen nun repeat‑bewusste Methoden einsetzen müssen, die einzelne Loci unterscheiden — zum Beispiel Lang‑Read‑Sequenzierung, die ganze Repeat‑Blöcke überspannen und deren Methylierungsmuster sowie RNA‑Produkte vollständig erfassen kann.
Was das für Patienten und zukünftige Therapien bedeutet
Die Studie widerlegt nicht die zentrale Rolle der verkürzten D4Z4‑Region auf Chromosom 4 bei FSHD, zeigt aber, dass diese Region in einer dicht besiedelten Nachbarschaft ähnlicher Sequenzen liegt. Signale, die einst als Beleg für Aktivität am Krankheitslokus galten, können tatsächlich teilweise von genomischen Verwandten stammen. Für Patienten bedeutet das, dass die zuverlässigsten Diagnosetools diejenigen sein werden, die physisch das genaue Chromosom und das beteiligte Repeat‑Array auflösen, anstatt sich nur auf indirekte Messgrößen zu verlassen. Für Forscher und Arzneimittelentwickler unterstreicht es die Notwendigkeit hochspezifischer Designs, die vermeiden, unbeabsichtigt harmlose Repeats an anderen Stellen des Genoms zu treffen. Im Telomere‑to‑Telomere‑Zeitalter wird das Verständnis und die Behandlung von FSHD davon abhängen, die vollständige Repeat‑Landschaft zu sehen, nicht nur ein einzelnes Wahrzeichen.
Zitation: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Schlüsselwörter: facioscapulohumerale Muskeldystrophie, D4Z4‑Repeats, DUX4, Telomere‑to‑Telomere‑Genom, genetische Diagnostik