Clear Sky Science · de
Künstliche Chaperone: von herkömmlichen Entwürfen zu intelligenten Systemen
Wie Moleküle beim richtigen Falten geholfen wird
In jeder lebenden Zelle müssen lange Ketten von Proteinen und genetischem Material sich genau in die richtige Form biegen und drehen, um korrekt zu funktionieren. Wenn sie fehlfalten, können sie verklumpen, ihre Funktion verlieren und sogar Krankheiten wie neurodegenerative Erkrankungen auslösen. Die Natur setzt „Chaperon“-Moleküle ein, um dieses mikroskopische Durcheinander zu ordnen, doch diese natürlichen Helfer sind teuer, empfindlich und außerhalb der Zelle schwer einsetzbar. Dieser Artikel beleuchtet, wie Wissenschaftler heute künstliche Chaperone entwickeln—konstruktive Helfer, die fehlgeleitete Moleküle zurück in die richtige Form bringen können und sich wie intelligente Werkzeuge an- und ausschalten lassen.
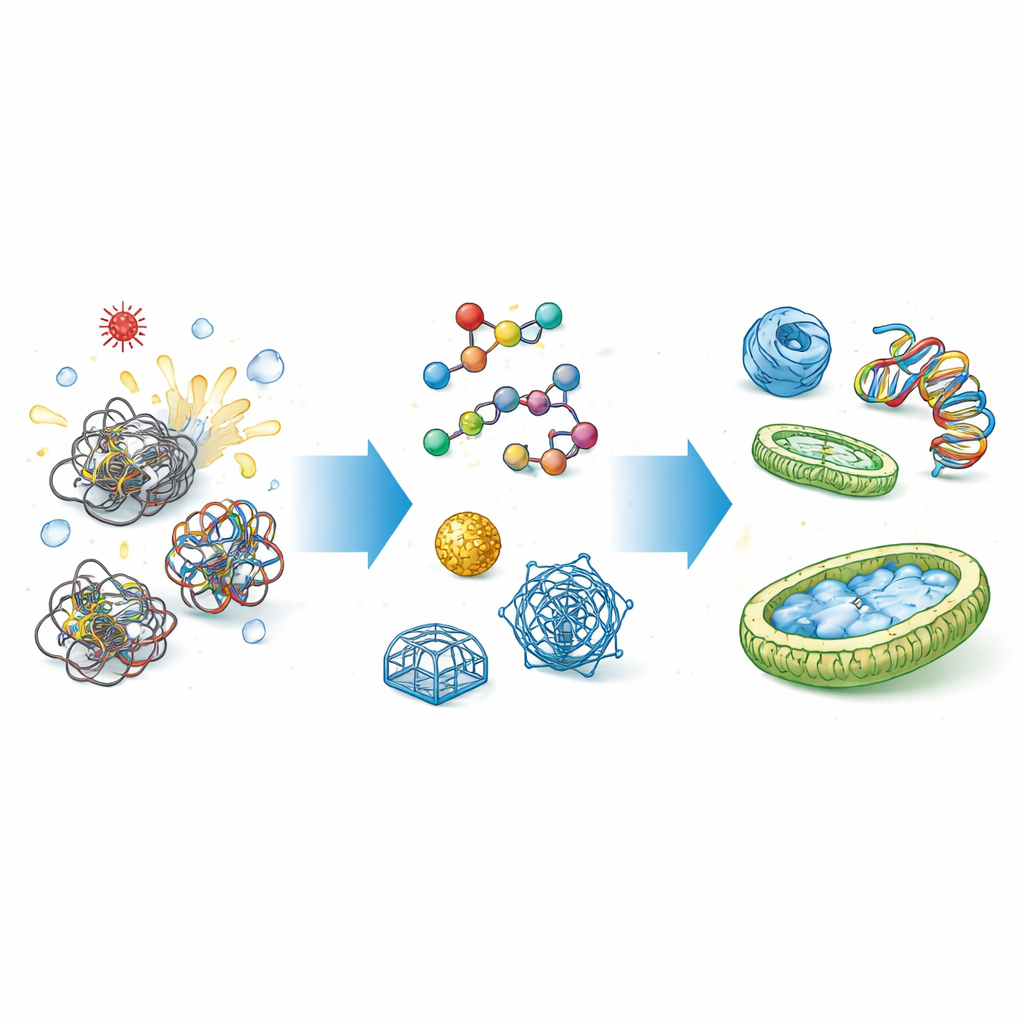
Warum Zellen Falthilfen brauchen
Proteine und Nukleinsäuren (wie DNA und RNA) werden nicht fertig geboren; sie müssen sich zu komplexen dreidimensionalen Strukturen falten. Der Weg zu diesen Formen ist voller Fallstricke, an denen Ketten stecken bleiben oder aneinander haften können. Natürliche Chaperone, etwa Hitzeschockproteine, fassen diese schlaffen Ketten, decken ihre klebrigen Stellen ab und bieten einen geschützten Raum, in dem sie korrekt gefaltet werden können. Für Nukleinsäuren übernehmen Chaperone ähnliche Führungsaufgaben, indem sie Knoten auflösen und Basenpaarungen neu anordnen. Versagt diese Kontrolle, kann das zu Funktionsverlust, toxischen Ablagerungen, Krankheiten und teuren Ausfällen in der industriellen Proteinproduktion führen.
Von einfachen Chemikalien zu Designer‑Polymeren
Die ersten künstlichen Chaperone waren vergleichsweise einfache Chemikalien, die das Umfeld der Moleküle veränderten. Bestimmte Lösungsmittel und Detergenzien können klebrige Bereiche von Proteinen verbergen, Aggregation verhindern und ihnen eine zweite Chance zum Umfalten geben. Einige kleine Fettsäuren beispielsweise helfen mutiertem Kollagen, korrekter zu falten, und lindern den Stress in Zellen bei erblichen Erkrankungen. Diese chemischen Helfer müssen jedoch meist in hohen Dosen zugegeben werden, sind schwer auf spezifische Ziele zuschneidbar und können andere Komponenten in komplexen Gemischen stören. Um mehr Kontrolle zu gewinnen, wandten sich Forscher größeren, maßgeschneiderten Polymeren zu—flexiblen Ketten, die mit geladenen oder wasserliebenden Verzweigungen bestückt werden können, um DNA, RNA und Proteine selektiver zu stützen.
Polymer- und Nanogel‑Werkzeuge
Designer‑Polymere können an geladene Rückgrate der DNA oder an exponierte Bereiche von Proteinen andocken und so die Energieoberfläche glätten, damit diese Moleküle schneller und zuverlässiger ihre bevorzugten Formen finden. Für Nukleinsäuren können kationische (positiv geladene) Polymere die Abstoßung zwischen Strängen neutralisieren, wodurch Basenpaarung, Strangaustausch und die Bildung ungewöhnlicher Strukturen für DNA‑Computing und Biosensoren beschleunigt werden. Bei Proteinen können Polymere wie speziell geformte Polyethylenglykol‑Schlaufen oder synthetische Polyanionen einige natürliche Chaperone bei der Verhinderung hitzeinduzierter Aggregation übertreffen. Andere Systeme koppeln flexible Chaperon‑Polymere mit kurzen Peptiden, um zellähnliche Membranen in flache Nanoschichten oder Vesikel umzuwandeln und so reversible zweidimensionale Plattformen für Nutzlastlieferung und Gewebetechnik zu schaffen.

Aufbau intelligenter, schaltbarer Chaperone
Über das bloße Halten und Freigeben von Klienten hinaus können moderne künstliche Chaperone nun auf ihre Umgebung reagieren. Forscher haben Nanogele, Nanopartikel und Polymernetzwerke entwickelt, deren Griff an Proteinen sich bei Änderungen von Säuregrad, Temperatur, Licht oder bestimmten Chemikalien wie Glukose verstärkt oder lockert. Manche Mizellen werden bei mild saurem pH‑Wert hydrophober und imitieren natürliche Chaperone, indem sie bedrohte Proteine einfangen und bei Änderung des pH‑Werts wieder freigeben. Temperatur‑reaktive Polymere kollabieren oder dehnen sich aus, wenn sie einen Schwellenwert überschreiten, sodass sie geschädigte Proteine bei einer Temperatur sequestrieren und umgefaltete bei einer anderen wieder freigeben können. Lichtempfindliche Gruppen dienen als molekulare Schalter, die DNA‑Assemblierungswege per Lichtblitz ein‑ oder ausschalten, während zuckerempfindliche Partikel ein therapeutisches Hormon schützen und es bevorzugt freisetzen können, wenn der Blutzucker hoch ist.
Was das für Medizin und Technik bedeutet
Der Artikel schlussfolgert, dass sich künstliche Chaperone von einfachen chemischen Stabilisatoren zu hoch programmierbaren „molekularen Werkzeugen“ entwickeln, die auf Abruf viele Arten biologischer Strukturen erkennen, schützen und umgestalten können. Durch sorgfältiges Austarieren attraktiver und abstoßender Kräfte und durch die Integration von Empfindlichkeit gegenüber Reizen wie pH, Wärme, Licht oder mechanischem Stress können diese Systeme Zielmoleküle am richtigen Ort zur richtigen Zeit falten. Langfristig könnten solche intelligenten Helfer die industrielle Proteinproduktion effizienter machen, Biosensoren schärfen, molekulare Computer antreiben und neue Wege eröffnen, Krankheiten anzugehen, die mit fehlgefalteten Proteinen zusammenhängen—möglicherweise einschließlich Erkrankungen wie Alzheimer—wobei sie die subtile Kontrolle nachahmen, die Zellen bereits leisten.
Zitation: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Schlüsselwörter: künstliche Chaperone, Proteinfaltung, intelligente Polymere, Nanomedizin, stimuli-responsive Materialien