Clear Sky Science · de
Superatomare Moleküle: natürliche und nicht‑natürliche, atomähnliche Bindungen zwischen Superatomen
Winzige Bausteine, die sich wie Atome verhalten
Die meisten von uns lernen, dass Atome die grundlegenden Bausteine der Materie sind. Dieser Übersichtsartikel zeigt, dass sich auf sehr kleinen Skalen Gruppen von Dutzenden Metallatomen selbst wie „Super‑Atome“ verhalten können und dass sich diese Superatome zu „superatomaren Molekülen“ verbinden können. Durch das Verständnis und die gezielte Gestaltung dieser ungewöhnlichen Bausteine hoffen Wissenschaftler, neue Materialien mit fein abgestimmten Licht-, Elektronen‑ und katalytischen Eigenschaften zu schaffen, die gewöhnliche Moleküle nicht bieten können.
Cluster, die einzelne Atome nachahmen
Superatome sind ultrasmallere Metallcluster – oft aus Gold, Silber oder Kupfer – deren Elektronen sich in wohlgeordneten, schalenartigen Mustern anordnen, ähnlich den Schalen in einer Lehrbuchabbildung eines Atoms. Wenn diese Schalen vollständig besetzt sind, bei bestimmten „magischen Zahlen“ von Elektronen, wird der Cluster besonders stabil. Chemiker können diese Cluster weiter stabilisieren, indem sie sie mit organischen Molekülen, sogenannten Liganden, umhüllen und so präzise Nanoobjekte mit genau definierten Größen und Formen erzeugen. Viele dieser Superatome sind nahezu kugelförmig, und ihre Stabilität lässt sich mit einem einfachen Modell erklären, in dem die freien Elektronen des Metalls wie in einem glatten, positiv geladenen Tropfen umherwirbeln.
Wenn Superatome wie gewöhnliche Moleküle binden
Einige Metallcluster sind überhaupt nicht kugelförmig. Stattdessen sehen sie aus, als wären zwei oder mehr Superatome miteinander verschmolzen und bildeten das, was die Autorin als superatomare Moleküle bezeichnet. Zur Erklärung dieser Strukturen entwickelten Forscher die „Super‑Valenzbindungs‑Theorie“, die jedes Superatom wie ein riesiges Atom mit eigenen Orbitalen behandelt und beschreibt, wie diese Orbitale sich mischen, um gemeinsame „superatomare Molekülorbitale“ zu bilden. In vielen Fällen verhalten sich diese Kombinationen genau wie vertraute chemische Bindungen. Beispielsweise können Paare von Gold‑Superatomen superatomare Versionen der Bindung im Fluormolekül bilden, während komplexere Verschmelzungen Analogien zu Sauerstoffmolekülen mit höheren Bindungsordnungen oder sogar dreizentrenähnliche Bindungen ähnlich Ozon liefern. Diese Anordnungen schaffen reiche Bindungsmuster – einfach, mehrfach und mehrzentrig –, die die Bindungsregeln der gewöhnlichen Chemie widerspiegeln, nun jedoch auf der Skala von Clustern mit Dutzenden von Atomen. 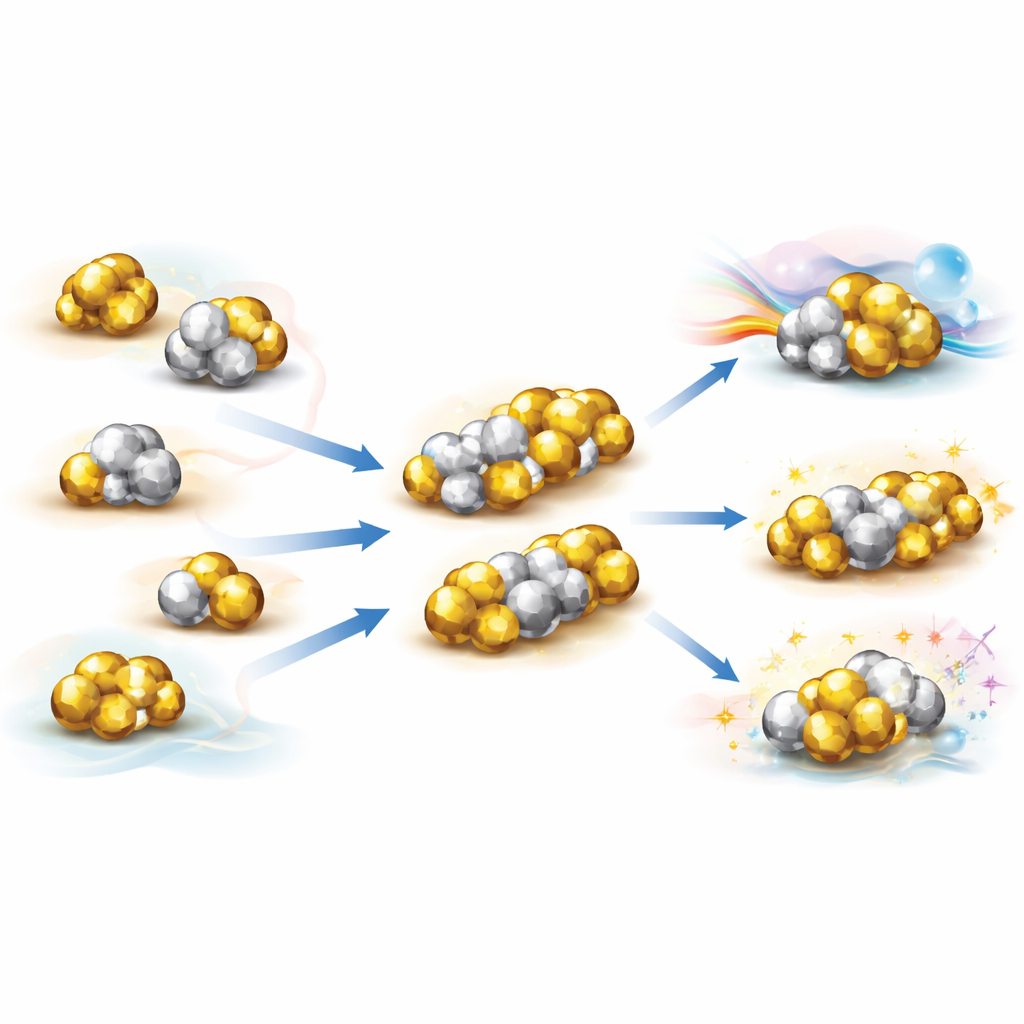
Seltsame Bindungen mit edelgasähnlichen Einheiten
Superatomare Moleküle sind nicht auf saubere Analogien zu Alltagsbindungen beschränkt. Die Übersicht hebt „nicht‑natürliche“ Bindungsmotive hervor, bei denen Superatome mit geschlossenen Elektronenschalen – ähnlich im Geiste zu Edelgasen wie Helium oder Neon – sich zu größeren Strukturen kombinieren, obwohl nach den üblichen Zählregeln eigentlich keine Bindung vorhanden sein sollte. In diesen Systemen können Superatome ein einzelnes Metallatom teilen, kante‑zu‑kante sitzen oder sich zu zyklischen und stäbchenförmigen Assemblies verbinden. Formal ist ihre Bindungsordnung null, dennoch stabilisieren Wechselwirkungen zwischen ihren Elektronenwolken und den umgebenden Liganden die Gesamtstruktur. Bemerkenswerterweise zeigen diese Anordnungen neue Absorptionsbanden und andere elektronische Merkmale, die in den isolierten Superatomen fehlen, und machen deutlich, dass subtile Orbitalwechselwirkungen völlig neue optische Reaktionen erzeugen können.
Von Superringen zu Superketten
Der Artikel beleuchtet auch exotischere Beispiele, in denen Superatome Ringe und Ketten mit kollektivem Verhalten bilden. Ein bemerkenswerter Fall ist ein Goldcluster, der aus fünf icosaedrischen Superatomen besteht, die zu einem Ring angeordnet sind; theoretische Studien legen nahe, dass dieser „Super‑Ring“ mit der richtigen Elektronenzahl aromatisch werden kann, indem er seine Elektronen über die Schleife verteilt – eine direkte Analogie zu klassischen aromatischen Molekülen wie Benzol oder dem Cyclopentadienyl‑Ion. Eine weitere Strukturfamilie verknüpft winzige dreiatomige Goldeinheiten zu stäbchenförmigen Ketten. Obwohl die Verbindungen zwischen benachbarten Einheiten schwach und teilweise antibindend sind, wirkt das wiederkehrende Muster wechselwirkender Orbitale wie ein „superatomares Polymer“ und führt zu starker Absorption im nahen Infrarotbereich, was auf Anwendungen in photothermischen und optoelektronischen Geräten hinweist. 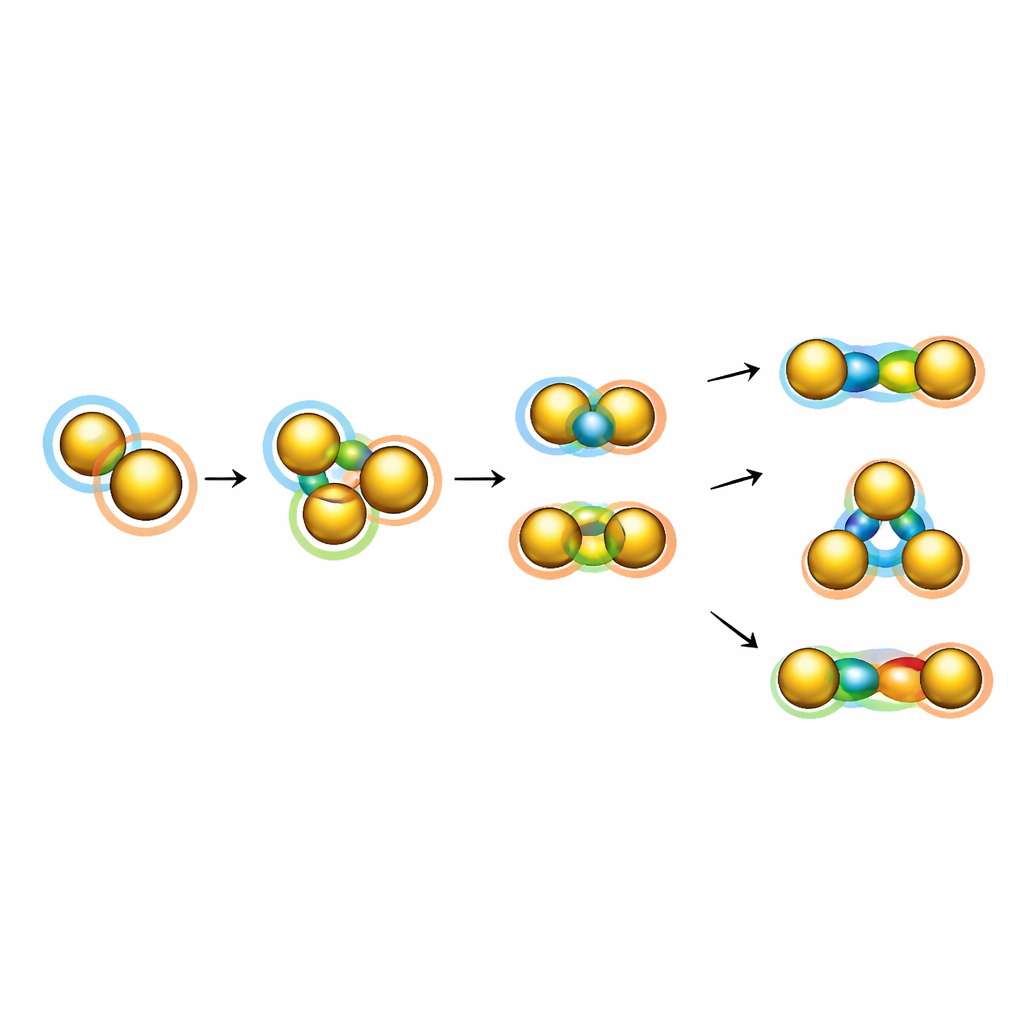
Warum diese winzigen Supermoleküle wichtig sind
Insgesamt argumentiert die Übersicht, dass die Behandlung metallischer Cluster als atomähnliche Einheiten, die zu superatomaren Molekülen binden können, eine mächtige Designsprache für neue Materialien bietet. Durch die Wahl der Elektronenzahl jedes Superatoms, ihrer Verknüpfung und der umgebenden Liganden können Wissenschaftler nicht nur Stabilität, sondern auch Lichtabsorption, Ladungstransport, Magnetismus und katalytische Aktivität gezielt steuern. Naturnahe Bindungen liefern vertraute Gestaltungsregeln, während nicht‑natürliche und schwach gebundene Assemblies Verhaltensweisen eröffnen, die keine direkte Entsprechung in der gewöhnlichen Chemie haben. Mit der Reifung dieses Verständnisses könnten superatomare Moleküle zu einem Werkzeugkasten für die Gestaltung der nächsten Generation von Katalysatoren, lichtabsorbierenden Systemen und elektronischen Bauteilen werden, die aus präzise angeordneten Atomclustern aufgebaut sind.
Zitation: Isozaki, K. Superatomic molecules: natural and non-natural atom-like bonding between superatoms. NPG Asia Mater 18, 9 (2026). https://doi.org/10.1038/s41427-026-00636-9
Schlüsselwörter: Superatome, metallische Nanocluster, superatomare Moleküle, Nanomaterialien, optoelektronische Eigenschaften