Clear Sky Science · de
Onkolytisches Virus M1 reaktiviert CD8+-T‑Zell‑Immunität gegen Glioblastom durch B‑Zell‑abhängige Antigen‑Kreuzpräsentation in der Milz
Das Immunsystem wieder einschalten
Glioblastom gehört zu den tödlichsten Hirntumoren, zum Teil weil es besonders gut darin ist, die Abwehrkräfte des Körpers auszuschalten. Diese Studie untersucht einen neuen Ansatz, dieses Abschalten umzukehren, mithilfe eines speziell konstruierten Virus, das über den Blutkreislauf verabreicht wird, sowohl Tumorzellen angreift als auch Immunzellen mobilisiert, um den Krebs zu bekämpfen. Die Arbeit enthüllt einen unerwarteten Schlüsselakteur in dieser Reaktion: Immunzellen in der Milz, die dabei helfen, tumorvernichtende T‑Zellen zu wecken.
Ein Virus, das Krebszellen bevorzugt
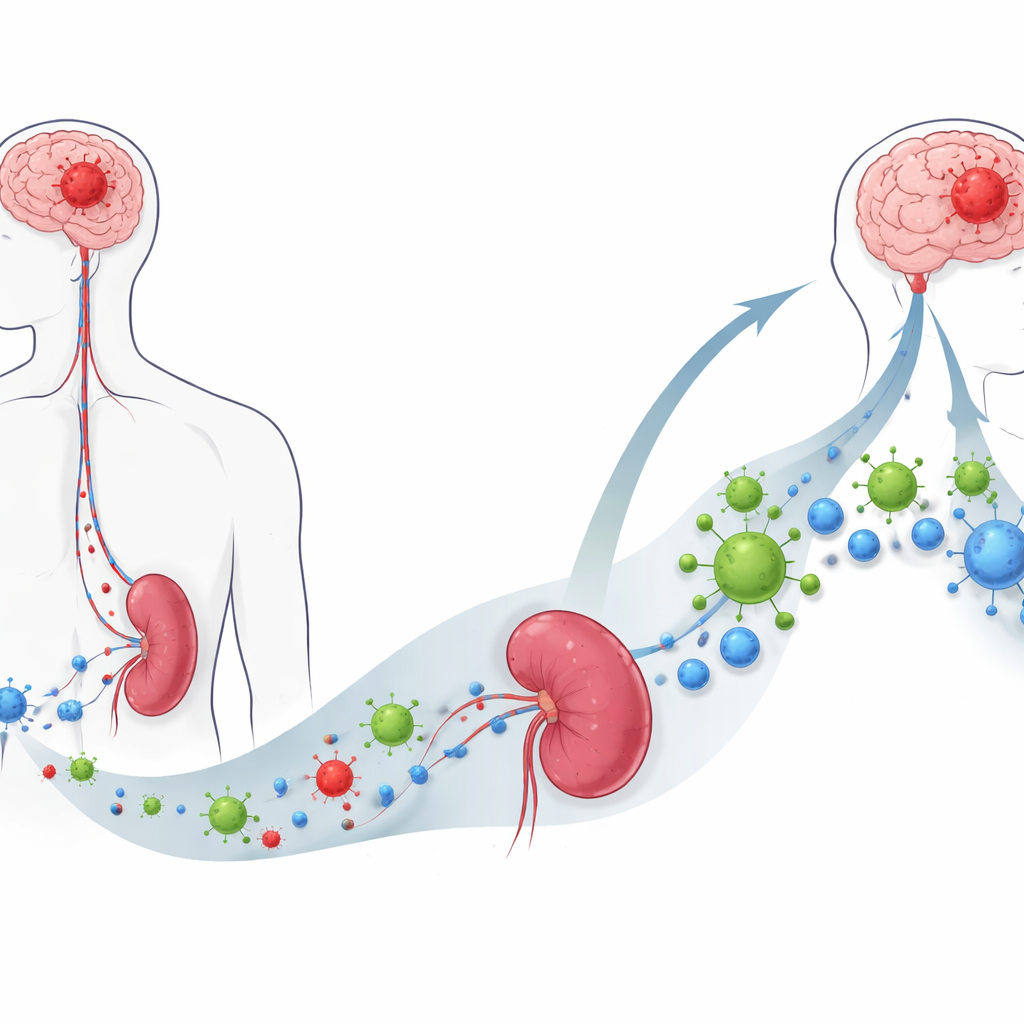
Die Forschenden untersuchten eine experimentelle Therapie namens onkolytisches Virus M1, kurz OVM, ein modifiziertes Alphavirus, das bevorzugt Krebszellen infiziert und tötet, während normales Gewebe verschont bleibt. In Zellkultur drang OVM effizient in verschiedene Maus‑ und humane Glioblastom‑Zelllinien ein und löste eine Form des Zelltods aus, die molekulare „Gefahrensignale“ hinterlässt. An frisch entnommenen menschlichen Tumorfragmenten replizierte OVM stark in Glioblastom‑Gewebe, jedoch nicht in benachbarten nicht‑krebsartigen Hirnproben, was nahelegt, dass es bösartige von gesunden Zellen besser unterscheiden kann als Standardchemotherapie, die beide schädigte.
Umkehr des systemischen Immunversagens
Über das Gehirn hinaus verursacht Glioblastom einen weitreichenden Immunzusammenbruch: Patient:innen und Mausmodelle zeigen geschrumpfte Milzen und einen starken Verlust zirkulierender T‑Zellen. Nach intravenöser OVM‑Behandlung bei tumortragenden Mäusen änderte sich dieses Bild dramatisch. Die Milzen erlangten ihre Größe zurück, die Blutspiegel von CD4‑ und CD8‑T‑Zellen erholten sich, und immundämpfende Moleküle wie IL‑10 und TGF‑beta sanken. Am Tumorort wanderten mehr T‑Zellen — insbesondere CD8‑„Killer“‑T‑Zellen, die ein Modell‑Tumorantigen erkennen — ins Gehirn ein und verwandelten eine zuvor „kalte“ Tumorumgebung in eine, die von Immunzellen dicht besiedelt war.
Warum die Milz wichtig ist
Überraschenderweise erwies sich die Milz als unverzichtbar für den Erfolg von OVM. Wurde die Milz chirurgisch entfernt, verlangsamte das Virus das Tumorwachstum nicht mehr und verlängerte nicht die Überlebenszeit; der Anstieg der T‑Zellen im Blut und im Gehirn verschwand weitgehend. Einzelzell‑RNA‑Sequenzierung splenischer Immunzellen zeigte, dass nach OVM‑Behandlung B‑Zellen in der Milz besonders starke Kommunikationsnetzwerke mit T‑Zellen bildeten. In In‑Vitro‑Experimenten ließen B‑Zellen aus OVM‑behandelten Mäusen CD8‑T‑Zellen deutlich effektiver proliferieren und aktivieren als B‑Zellen aus unbehandelten Tieren, während dendritische Zellen diese Steigerung nicht zeigten — was auf B‑Zellen als zentrale Vermittler hinweist.
Spezielle B‑Zellen, die Tumorkiller primen
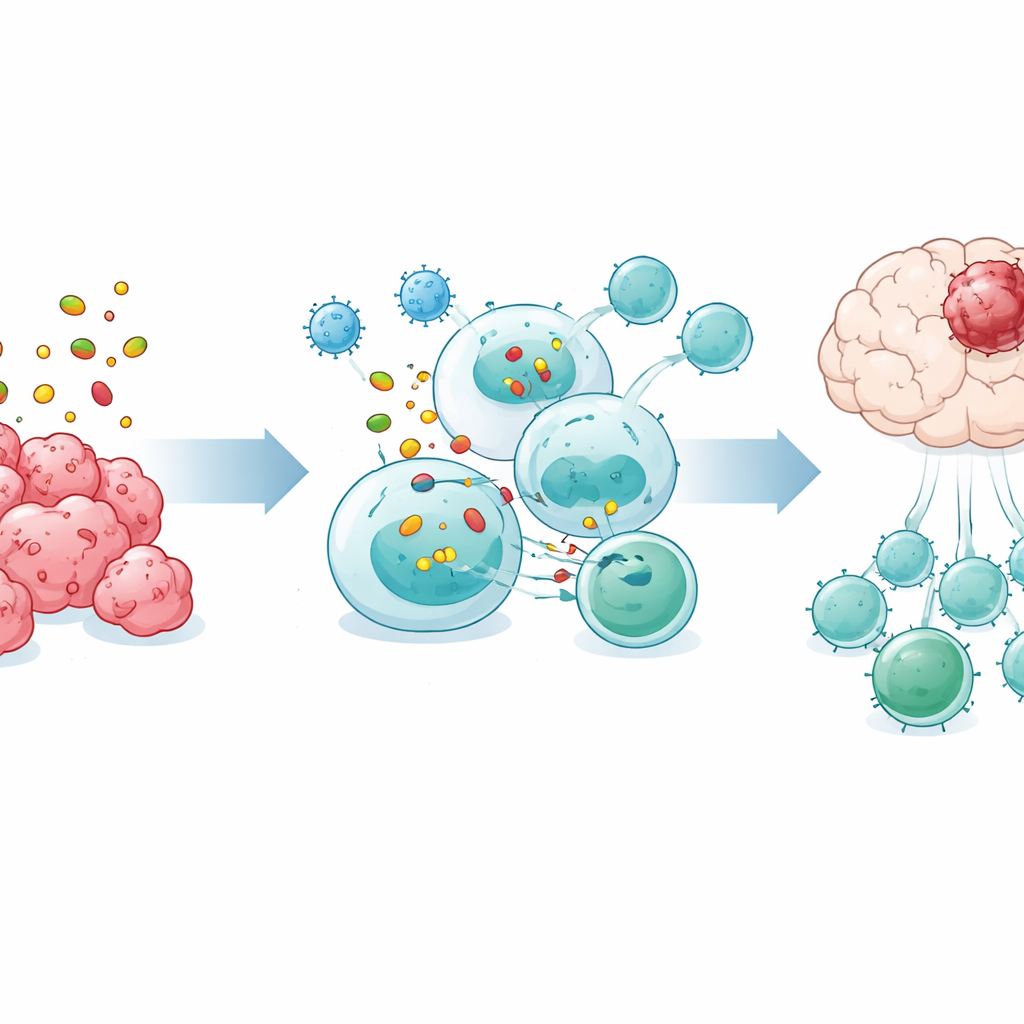
Bei genauerer Untersuchung entdeckte das Team eine charakteristische B‑Zell‑Untergruppe, die durch ein Oberflächenmolekül namens Bst2 gekennzeichnet ist und nach OVM‑Behandlung in der Milz vermehrt auftrat. Diese Bst2‑positiven B‑Zellen zeigten eine Anreicherung von Genen, die an der Aufnahme von Tumormaterial, dessen intrazellulärer Verarbeitung und der Präsentation von Peptidfragmenten auf der Zelloberfläche beteiligt sind — so, dass CD8‑T‑Zellen diese erkennen können. Experimente zeigten, dass diese Zellen Tumorantigene effizienter aufnahmen, enge Kontaktzonen mit CD8‑T‑Zellen bildeten und für die Aktivierung der T‑Zellen direkten Zell‑zu‑Zell‑Kontakt sowie einen spezifischen Proteinverarbeitungsweg benötigten. Als isolierte Bst2‑positive B‑Zellen in B‑Zell‑defiziente Mäuse mit Hirntumoren übertragen wurden, verlängerten sie das Überleben signifikant, während andere B‑Zell‑Typen dies nicht taten.
Stärkung der Wirkung von Checkpoint‑Therapie
Die derzeit führenden Immuntherapien — Checkpoint‑Inhibitoren, die PD‑1 oder PD‑L1 blockieren — zeigten bei Glioblastom enttäuschende Ergebnisse. In den hier verwendeten Mausmodellen bewirkten PD‑1‑ oder PD‑L1‑Antikörper allein wenig. Die Kombination von OVM mit einem PD‑1‑blockierenden Antikörper erhöhte jedoch deutlich die Zahl der CD8‑T‑Zellen in den Hirntumoren, verschob zirkulierende T‑Zellen von einem naiven in einen aktivierten Zustand, stellte die Milzgröße wieder her und verlängerte das Überleben. OVM‑Behandlung erhöhte außerdem die PD‑1‑Expression auf tumorinfiltrierenden CD8‑T‑Zellen, wodurch diese anfälliger für eine Wiederherstellung durch PD‑1‑Blockade wurden.
Was das für Patient:innen bedeuten könnte
Insgesamt deutet diese Arbeit darauf hin, dass ein intravenös verabreichtes onkolytisches Virus mehr leisten kann als nur Glioblastomzellen zu infizieren und zu lysieren. Indem es eine spezialisierte Gruppe von B‑Zellen in der Milz rekrutiert, die Tumormaterial verarbeiten und CD8‑T‑Zellen präsentieren, baut OVM die systemische Immunität wieder auf und treibt Killer‑T‑Zellen zurück ins Gehirn, um den Tumor anzugreifen. In präklinischen Modellen unterdrückt diese Strategie nicht nur allein das Tumorwachstum, sondern macht resistente Hirntumoren auch empfindlich für PD‑1‑Checkpoint‑Therapie. Wenn sich diese Befunde auf den Menschen übertragen lassen, könnten OVM und Bst2‑positive B‑Zellen die Grundlage neuer Kombinationsbehandlungen — und sogar personalisierter Impfstoffe — bilden, die dem Immunsystem endlich eine echte Chance gegen Glioblastom geben.
Zitation: Han, Y., Guo, C., Chen, C. et al. Oncolytic virus M1 reinvigorates CD8+ T-cell immunity against glioblastoma through B-cell-dependent antigen cross-presentation in the spleen. Cell Mol Immunol 23, 349–366 (2026). https://doi.org/10.1038/s41423-026-01396-w
Schlüsselwörter: glioblastom, onkolytisches Virus, Tumorimmunologie, B‑Zellen, Immun-Checkpoint‑Therapie