Clear Sky Science · de
Die Bekämpfung der Cuproptose: von metabolischer Umprogrammierung bis zur therapeutischen Nutzung bei Krebs
Wenn ein nützliches Metall gegen Krebs arbeitet
Kupfer ist vor allem als Bestandteil von elektrischen Leitern und Sanitäranlagen bekannt, doch es durchdringt leise unsere Zellen und hilft Enzymen bei der Energiegewinnung und beim Schutz vor Schäden. Dieser Übersichtsartikel beleuchtet eine überraschende Wendung: Unter bestimmten Bedingungen kann zu viel Kupfer Krebszellen in eine spezielle Form des Zelltods treiben. Das Verständnis dieses Prozesses — genannt „Cuproptose“ — könnte neue Wege eröffnen, Tumore zu behandeln, die Standardtherapien bereits ausgetrickst haben.
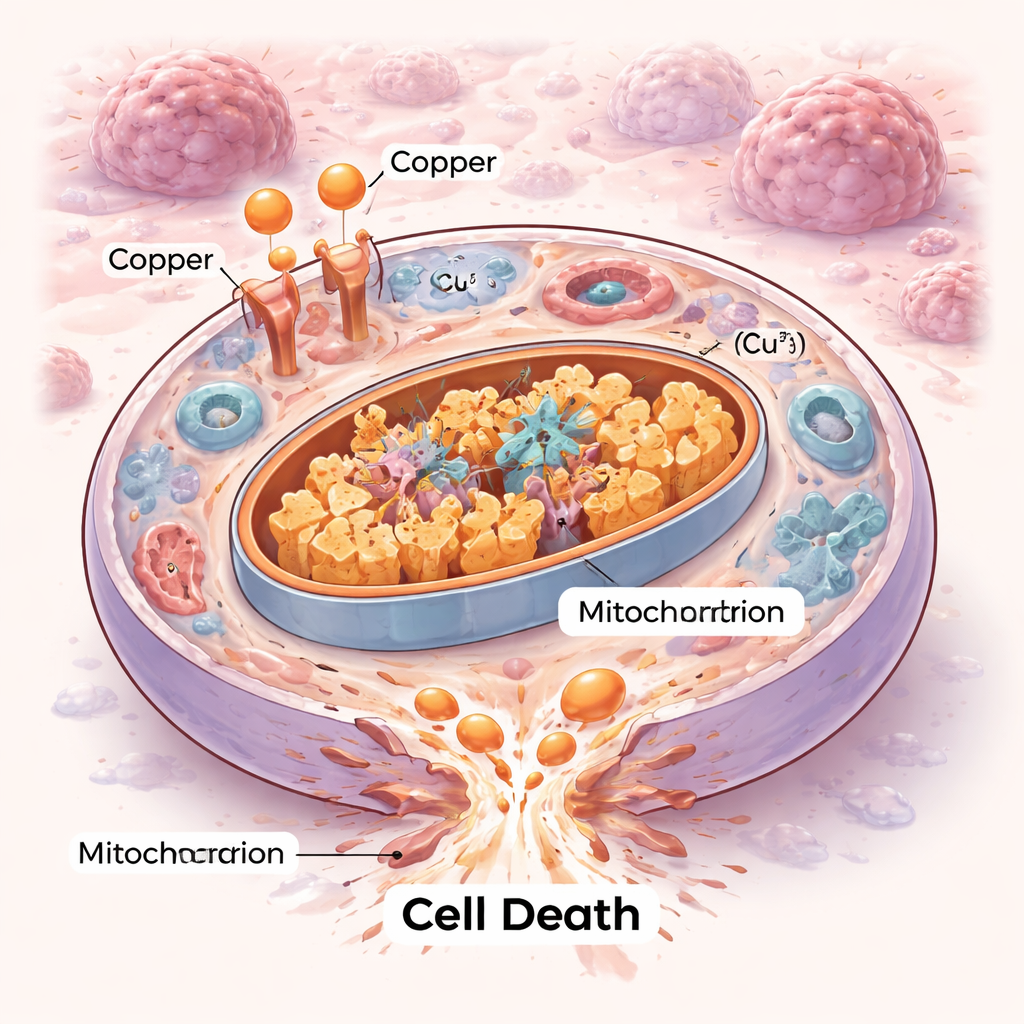
Eine neue Art, wie Zellen sterben können
Zellen sterben nicht alle auf dieselbe Weise. Jahrzehntelang haben Wissenschaftler geordnete Selbstzerstörungsprogramme wie die Apoptose und neuere Formen wie die Ferroptose kartiert. Cuproptose ergänzt dieses Spektrum. Dabei überflutet überschüssiges Kupfer die Kraftwerke der Zelle — die Mitochondrien — und bindet an bestimmte Stoffwechselenzyme, die normalerweise beim Verbrennen von Brennstoff helfen. Diese Bindung führt dazu, dass sich diese Enzyme verklumpen und winzige Eisen‑Schwefel‑Komponenten destabilisiert werden, die die Mitochondrien zur Funktion benötigen. Das Ergebnis ist eine Art innerer Stau und mechanischer Zusammenbruch, den die Zelle nicht reparieren kann, und der in einem Tod durch proteotoxischen Stress endet, statt über die klassischen Selbstmordwege.
Wie Krebszellen Kupfer und Energie steuern
Weil Kupfer gleichzeitig lebenswichtig und gefährlich ist, unterhalten Zellen ein ausgeklügeltes Logistiknetz, um es sicher zu bewegen. Spezialisierte Transporter bringen Kupfer in die Zelle, Chaperon‑Proteine eskortieren es zu Mitochondrien und anderen Zielen, und Speicherstoffe wie Metallothioneine und Glutathion fangen überschüssiges Kupfer ab. Tumore verändern dieses System oft. Einige steigern Importeure oder Chaperone, um ihren hohen Energiebedarf zu decken; andere erhöhen Exporteure oder Speicherproteine, um eine Kupferüberladung zu vermeiden. Gleichzeitig verlagern viele Krebsarten ihren Stoffwechsel — sie schalten zwischen oberflächlicher Zuckerverbrennung und tiefergehender mitochondrialer Atmung hin und her. Die Übersichtsarbeit erklärt, dass Cuproptose am stärksten dort zuschlägt, wo Zellen noch stark auf Mitochondrien angewiesen sind, wodurch Tumore mit diesem metabolischen Profil besonders verwundbar werden.
Schaltzentralen, die die Kupfersensitivität regeln
Wesentliche zelluläre „Entscheider“ beeinflussen, ob Cuproptose eintreten kann. Der Tumorsuppressor p53 zum Beispiel neigt dazu, Zellen von schneller Zuckerfermentation hin zu geordneterer mitochondrialer Brennstoffnutzung zu lenken. Dadurch und durch die Veränderung der Handhabung kupferbindender Enzyme kann p53 Krebsarten anfälliger für kupferinduzierten Tod machen — während mutierte Formen von p53 häufig das Gegenteil bewirken. Dagegen hilft der Hypoxiefaktor HIF‑1α, der in schlecht durchlüfteten Tumorkernen aktiviert wird, Zellen, der Cuproptose zu entkommen, indem er wichtige mitochondriale Enzyme herunterregelt und kupferbindende Schutzmechanismen hochfährt. Weitere Signalwege wie Wnt/β‑Catenin und AKT fördern Resistenz, indem sie den Kupferaustrag antreiben oder entscheidende Proteine chemisch so verändern, dass sie nicht mehr auf Kupferüberladung reagieren. Zusammen wirken diese Netzwerke wie Thermostate, die die Sensitivität eines Tumors gegenüber kupferbasierten Therapien erhöhen oder senken.
Kupfer, das Immunsystem und intelligentere Wirkstoffabgabe
Die Rolle von Kupfer beschränkt sich nicht auf das direkte Töten von Krebszellen; es formt auch die Immunlandschaft rund um Tumore. Kontrollierter Kupferstress kann sterbende Krebszellen „sichtbarer“ machen, indem er Gefahrensignale freisetzt, die T‑Zellen, dendritische Zellen und Makrophagen anziehen und aktivieren. Kupfer kann zudem die Regulation von Immuncheckpoints wie PD‑L1 beeinflussen, die Tumore nutzen, um Anti‑Tumor‑T‑Zellen auszuschalten, was die Kombination kupfer‑zielender Wirkstoffe mit modernen Immuntherapien nahelegt. Weil freies Kupfer gesunde Gewebe schädigen kann, entwickeln Forscher präzise Werkzeuge — kleinmolekulare Ionophore, die Kupfer selektiv in Krebszellen schleusen, und Nanomedizinplattformen, die Kupfer oder kupfergetriebene Wirkstoffe in zielgerichteten Partikeln oder Hydrogelen verpacken. Diese Technologien zielen darauf ab, Kupfer innerhalb von Tumoren auf tödliche Werte anzuheben und gleichzeitig den Rest des Körpers in einem sicheren Bereich zu halten.
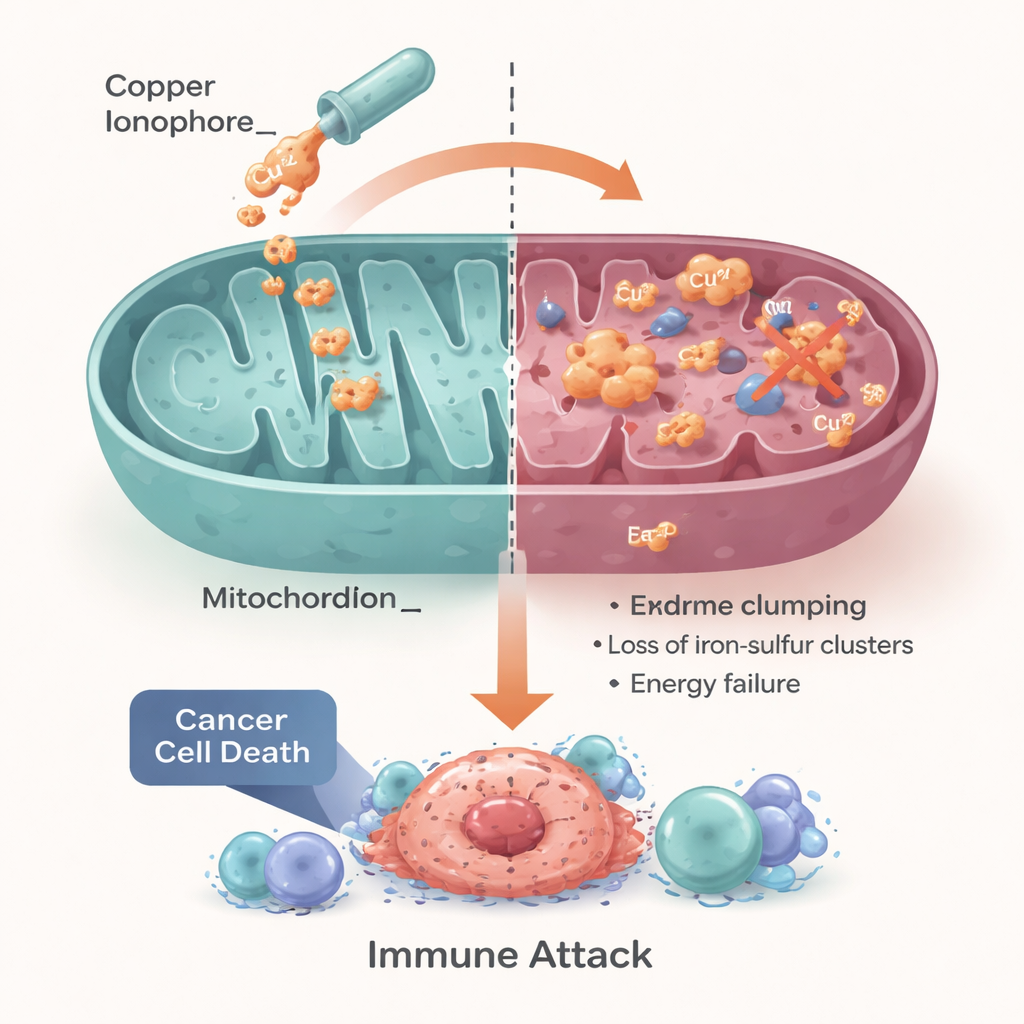
Eine zelluläre Schwäche in eine Therapie verwandeln
Die Autoren schließen, dass Cuproptose ein grundlegendes zelluläres Bedürfnis — die sorgfältige Verwaltung von Kupfer und Energie — in eine potenzielle Achillesferse für Krebs verwandelt. Tumore mit gestörter Kupferverarbeitung oder einer Überabhängigkeit von mitochondrialem Stoffwechsel könnten besonders empfindlich gegenüber kupferbasierten Strategien sein, einschließlich umgenutzter Medikamente wie Disulfiram und Elesclomol sowie moderner Nanopartikel. Sie betonen jedoch, dass der Erfolg davon abhängen wird, die richtigen Patienten mit dem passenden Ansatz zu matchen, mithilfe von Biomarkern, die über Kupfertransporter, mitochondriale Aktivität sowie den Immun‑ und Sauerstoffstatus des Tumors Auskunft geben. Wenn diese Hürden überwunden werden können, könnte das Nutzen der Cuproptose Onkologen einen neuen, metallschonenden Hebel geben, um Tumore zu behandeln, die derzeit nur wenige gute Optionen haben.
Zitation: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Schlüsselwörter: cuproptose, Kupferstoffwechsel, Krebstherapie, Tumormetabolismus, Krebsimmuntherapie