Clear Sky Science · de
Dynamische magneto‑mechanische Kräfte in Lysosomen induzieren dauerhafte Makrophagen‑Reprogrammierung für antitumorale Immunität
Sanfte Kräfte, um das Immunsystem zu wecken
Krebs überlebt häufig, indem er die Abwehrkräfte des Körpers in einen schläfrigen Zustand versetzt. Diese Studie untersucht einen unerwarteten Weg, sie wieder zu wecken: indem man winzige Kompartimente in Immunzellen mit magnetisch gesteuerten Nanopartikeln physikalisch zieht. Statt sich ausschließlich auf Medikamente zu stützen, verwenden die Forschenden sorgfältig abgestimmte mechanische Kräfte innerhalb von Zellen, um Immunzellen, sogenannte Makrophagen, in lang anhaltende Tumorkämpfer umzuprogrammieren.
Warum solide Tumoren schwer zu behandeln sind
Moderne Krebsimmuntherapien, wie Checkpoint‑blockierende Antikörper und gentechnisch veränderte Immunzellen, haben die Behandlung mancher Blutkrebserkrankungen revolutioniert. Bei vielen Menschen mit soliden Tumoren, etwa Lungenkrebs, helfen diese Ansätze jedoch nur einer Minderheit. Ein Hauptgrund ist das Tumormikromilieu. Tumoren sind von einer schützenden Nische umgeben, gefüllt mit Zellen und Signalen, die die Immunität dämpfen. Makrophagen, die Tumoren entweder angreifen (ein M1‑ähnlicher Zustand) oder unterstützen können (ein M2‑ähnlicher Zustand), werden häufig in den tumorfördernden M2‑Modus gedrängt. Dieses „schlechte“ Programm in dauerhafter Weise mit konventionellen biochemischen Wirkstoffen umzukehren, war schwierig.
Nanopartikel als winzige mechanische Motoren
Das Team entwickelte magnetische Nanomotoren—nanoskalige Partikel aus zinkdotiertem Eisenoxid, beschichtet mit einem positiv geladenen Polymer—die leicht von Makrophagen aufgenommen werden und sich in Lysosomen, den Recycling‑ und Signalzentralen der Zelle, anreichern. Ein externes rotierendes Magnetfeld bringt diese Partikel dazu, sich zu stäbchenähnlichen Ketten auszurichten und zu rotieren, wodurch die zähe Flüssigkeit innerhalb der Lysosomen umgerührt und winzige Wirbel erzeugt werden. Computersimulationen und Modellmembran‑Experimente zeigten, dass durch sorgfältiges Einstellen der Rotationsfrequenz die Schubspannung auf die lysosomale Membran auf einen optimalen Bereich gesetzt werden kann: stark genug, um die Membran kurzfristig durchlässig zu machen, aber nicht so stark, dass sie dauerhaft zerstört wird.
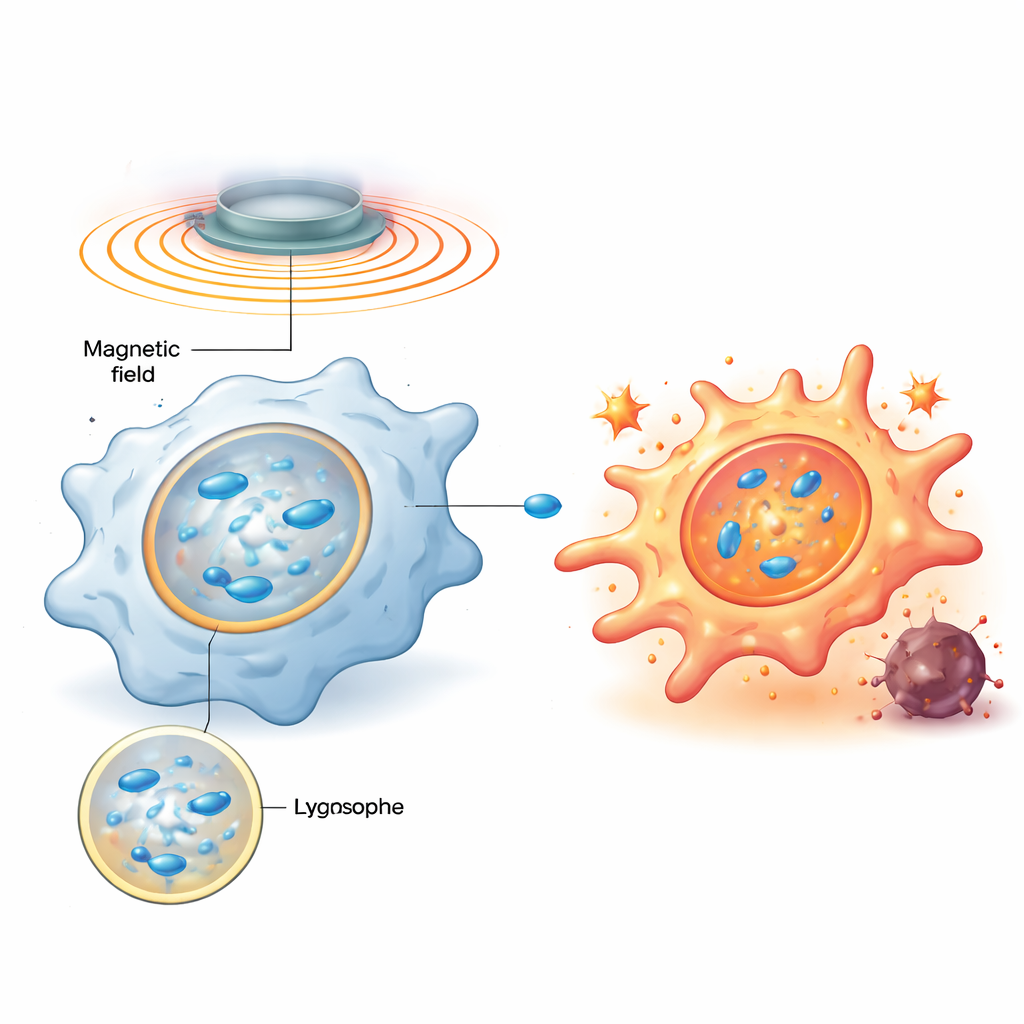
Mechanischer Anstoß löst einen biochemischen Alarm aus
Wenn die lysosomale Membran kurz gestört wird, eilt ein zuckerbindendes Protein namens Galectin‑9 zu den beschädigten Stellen und fungiert als Sensor für diesen mechanischen Stress. Die Studie zeigt, dass dies wiederum ein wichtiges Energiesensor‑Enzym, AMPK, aktiviert, das dann den NF‑κB‑Signalweg stärkt—bekannt dafür, Entzündungs‑ und antimikrobielle Reaktionen zu steuern. Gemeinsam lenken diese Signale den Stoffwechsel der Makrophagen weg von einem ruhigen, energieeffizienten Zustand hin zu schneller Glykolyse, einem Muster, das mit einer feindseligen, M1‑ähnlichen Funktion verbunden ist. Wichtig ist, dass sich das Lysosom repariert und die Signalgebung nach Abschalten des Magnetfelds abschwächt; beim erneuten Einschalten des Felds wird derselbe Weg wieder aktiviert. Dieses programmierbare An‑ und Ausschalten erlaubt es den Forschenden, denselben mechanischen Schalter wiederholt zu „tippen“, ohne die Zellen zu töten.
Makrophagen umschulen, um Tumoren zu bekämpfen
In Zellkulturen verwandelte diese magnetisch induzierte lysosomale Permeabilisierung—bezeichnet als MagLMP—Makrophagen, die in einen tumorfördernden M2‑ähnlichen Zustand gedrängt waren, zurück in einen proinflammatorischen M1‑ähnlichen Zustand. Diese umprogrammierten Zellen produzierten mehr entzündungsfördernde Zytokine und behielten ihr M1‑ähnliches Profil über Tage hinweg bei, selbst in tumorabgeleiteten Kulturmedien, die sie gewöhnlich in Richtung M2 treiben. In Maus‑Tumormodellen verlangsamte das Einbetten magnetischer Nanomotoren in Tumoren und die tägliche Anwendung zyklischer rotierender Felder das Wachstum verschiedener Krebsarten. Wurden Makrophagen experimentell entfernt, verschwand der Nutzen größtenteils, was zeigt, dass diese Zellen zentral für die Wirkung der Behandlung sind. Einzelzellanalyse der Tumorgewebe zeigte außerdem, dass MagLMP den Anteil M1‑ähnlicher Makrophagen erhöhte, antitumorale Neutrophile und Effektor‑CD8‑T‑Zellen stärkte und NF‑κB‑bezogene sowie Glykolyse‑Gene in Makrophagen hochregulierte.
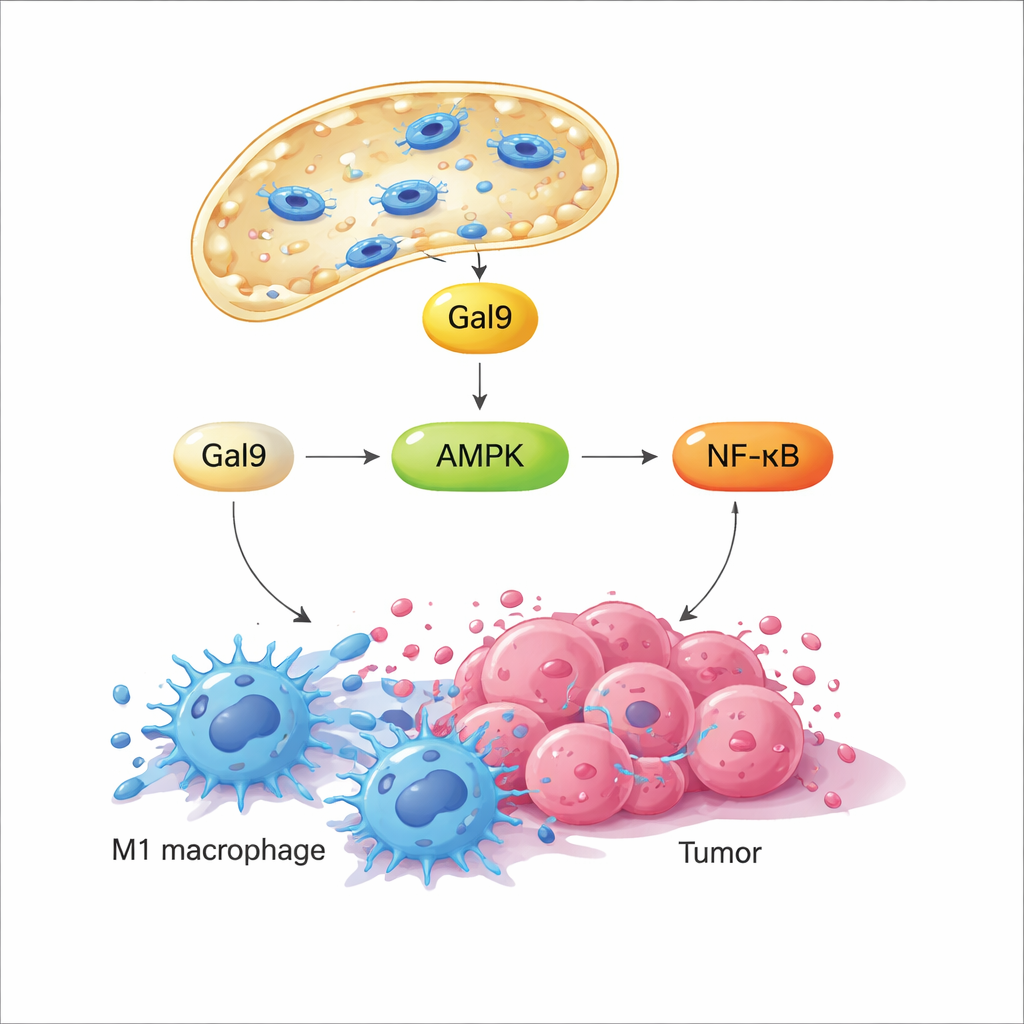
Von lokaler Kontrolle zu systemischer Therapie
Die Forschenden fragten dann, ob dieser Ansatz eher wie eine reale Behandlung über den Blutstrom verabreicht werden könnte. Sie injizierten die Nanomotoren intravenös und nutzten einen einfachen externen Magneten, um sie innerhalb von Tumoren zu konzentrieren, und zeigten damit eine effiziente Aufnahme durch Makrophagen im Tumorbett. Die anschließende MagLMP‑Behandlung verschob erneut Makrophagen in den M1‑ähnlichen Zustand und bremste das Tumorwachstum. In einem Mausmodell von frühzeitigem Lungenkrebs, das im Lungengewebe wuchs, führte die Kombination aus magnetischer Führung und zyklischem MagLMP zu deutlich verlängertem Überleben: etwa ein Drittel der behandelten Mäuse lebte länger als 300 Tage, verglichen mit nur Wochen bei Kontrolltieren. Die Kombination von MagLMP mit einem PD‑1‑Checkpoint‑Inhibitor verbesserte die Tumorkontrolle in schwer behandelbaren Modellen weiter.
Eine neue Möglichkeit, Immunität von innen heraus zu steuern
Diese Arbeit zeigt, dass winzige, gut kontrollierte mechanische Kräfte innerhalb eines spezifischen Organells genutzt werden können, um das Immunverhalten in lebenden Organismen zu lenken. Durch wiederholtes und reversibles „Pieken“ der Lysosomen aktiviert MagLMP eine Galectin‑9–AMPK–NF‑κB‑Achse, die Makrophagen in dauerhafte Tumorkämpfer umprogrammiert, ohne die Zellen breit zu schädigen. Für Nicht‑Spezialisten ist die zentrale Idee, dass physikalische Signale—zugeliefert durch magnetisch gesteuerte Nanomotoren—wie ein Einstellrad fürs Immunsystem wirken können und eine neue Klasse von Werkzeugen bieten, die Medikamente in zukünftigen Krebsimmuntherapien ergänzen könnten.
Zitation: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Schlüsselwörter: Krebsimmuntherapie, Makrophagenreprogrammierung, magnetische Nanopartikel, Mechanotransduktion, Lysosom‑Signalgebung