Clear Sky Science · de
Chronobiologie neurotropher Viren: rhythmischer Viruseintritt und arrhythmische Wirtsuhren
Warum der Zeitpunkt bei Hirninfektionen eine Rolle spielt
Viele gefährliche Viren, darunter Tollwut- und Herpesviren, haben die Fähigkeit, Gehirn und Nervensystem zu befallen. Diese Studie stellt eine überraschend einfache Frage mit großen Konsequenzen: Verändert die Tageszeit, wie leicht diese „neurotropen“ Viren in unser Nervensystem eindringen können, und können die Viren im Gegenzug unsere inneren Uhren aus dem Gleichgewicht bringen? Das Verständnis dieses zweiseitigen Dialogs zwischen Körperuhren und Viren könnte neue Möglichkeiten eröffnen, Impfungen, antivirale Therapien oder sogar Schichtarbeit so zu timen, dass das Risiko reduziert wird.
Tägliche Körperuhren und virale Eingangspforten
Fast jede Zelle des Körpers besitzt ein eingebautes 24‑Stunden-Zeitsystem, oft als circadiane Uhr bezeichnet. Es wird von einem Satz Kern-Clock‑Proteine angetrieben, darunter BMAL1 und REV-ERBα, die tausende Gene in rhythmischen Wellen an- und ausschalten. Die Autoren konzentrierten sich auf die „Türgriffe“, die Viren nutzen, um in Zellen einzudringen — Rezeptorproteine auf der Zelloberfläche — für Dutzende von hirn‑zielenden oder ins Gehirn eindringenden Viren. Anhand von gehirnähnlichen Organoiden aus Stammzellen, nervenabgeleiteten Zelllinien und Mausgewebe fanden sie heraus, dass die meisten dieser viralen Rezeptoren im Tagesverlauf ansteigen und fallen. Diese Rhythmen korrelierten eng mit der Aktivität der Uhrenkomponenten, was darauf hindeutet, dass unser tägliches Zeitsystem still und leise kontrolliert, wie viele virale Eintrittspunkte zu einer bestimmten Stunde verfügbar sind.
Ein Zellzyklusfaktor wird zum Boten der Uhr
Tiefer gehend fragten die Forscher, wie ein Protein, das normalerweise für die Steuerung der Zellteilung bekannt ist — E2F8 — in dieses Zeitnetz integriert ist. Sie entdeckten, dass E2F8 selbst der circadianen Kontrolle unterliegt und wie eine Relaisstation zwischen der Uhr und mindestens einem wichtigen Tollwutrezeptor, p75NTR, fungiert. Wenn das Uhrenprotein REV-ERBα aktiv ist, unterdrückt es E2F8. Niedrige E2F8-Werte heben dann die Bremse am p75NTR-Gen auf, sodass mehr dieses Rezeptors produziert wird und Zellen empfänglicher für das Tollwutvirus werden. Bemerkenswerterweise wirkt E2F8 auch rückkoppelnd auf die Uhr: Es kann direkt an Steuerregionen von Kern-Clock-Genen wie REV-ERBα und PER2 binden und deren Aktivität dämpfen. So entsteht eine Rückkopplungsschleife, in der ein Zellzyklusregulator die täglichen Rhythmen mitprägt und damit die Verwundbarkeit von Nervenzellen gegenüber Infektionen beeinflusst.
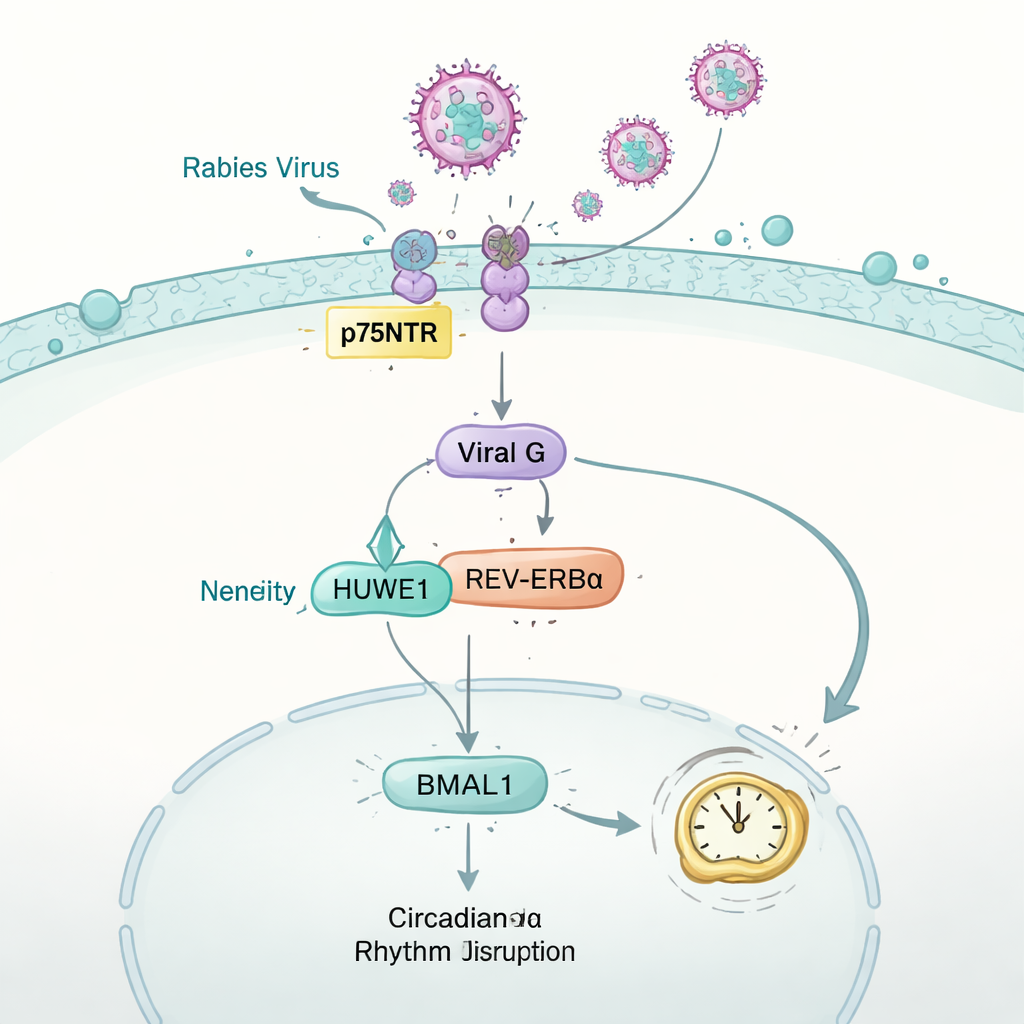
Wie das Tollwutvirus die Uhr aus dem Takt bringt
Die Studie drehte die Frage um: Kann ein Virus auf die Uhr zurückschlagen? An Mäusen, die mit Tollwut infiziert wurden, überwachte das Team Laufaktivität, Stoffwechsel und Atemchemie. Trotz normaler Nahrungsaufnahme in frühen Infektionsstadien verloren die Tiere allmählich die regulären Tag-Nacht-Muster, die gesunde Mäuse zeigen. In Gehirn und mehreren anderen Organen fielen die Mengen des zentralen Uhrenproteins BMAL1 stark ab. In nervenähnlichen Zellen ließ sich dieser Effekt auf das Tollwut-Glykoprotein „G“ zurückführen, ein Oberflächenprotein, das dem Virus normalerweise beim Verschmelzen mit Zellen hilft. G kaperte ein Wirtsenzym namens HUWE1, das normalerweise ein anderes Uhrenprotein, REV-ERBα, für den Abbau markiert. Durch die Konkurrenz um HUWE1 stabilisierte das virale G-Protein REV-ERBα, was zu einer verstärkten Unterdrückung von BMAL1 und letztlich zur Störung des Uhrwerks führte, das die Physiologie im 24‑Stunden-Rhythmus hält.
Zeitpunkt, Jetlag und Schwere der Infektion
Um zu prüfen, ob diese molekularen Veränderungen für den ganzen Organismus relevant sind, infizierte das Team Mäuse mit Tollwut zu verschiedenen Tageszeiten, unter normalen Licht‑Dunkel-Zyklen, unter chronischen „Jet‑lag“-Bedingungen und in Tieren, die genetisch kein REV-ERBα besitzen. Mäuse, die zu Beginn ihrer aktiven (nächtlichen) Phase infiziert wurden, in der der Tollwutrezeptor p75NTR seinen Höhepunkt hat, verloren schneller an Gewicht, wiesen in mehreren Hirnregionen höhere Viruslasten, stärkere Gehirnentzündungen auf und starben früher als Mäuse, die zu Beginn ihrer Ruhephase infiziert wurden. Mäuse, die wiederholten Phasenverschiebungen ausgesetzt waren, die rotierende Schichtarbeit nachahmen, verloren die normalen Uhr-Rhythmen im Gehirn, zeigten dauerhaft höhere p75NTR‑Spiegel, schwächere basale antivirale Signale und erkrankten schwerer. Im Gegenteil zeigten Mäuse ohne REV-ERBα weniger p75NTR, trugen niedrigere Viruslasten und überlebten nach der Infektion länger, was darauf hinweist, dass diese Uhrenkomponente ein entscheidender Wächter für die Schwere der Tollwuterkrankung ist.
Was das für Menschen bedeutet
Einfach ausgedrückt zeigt die Studie: Unsere inneren Uhren legen nicht nur Schlafzeiten fest; sie öffnen und schließen auch molekulare Türöffnungen, die ins Gehirn eindringende Viren nutzen, und diese Viren können zurückschlagen, indem sie die Uhr durcheinanderbringen. Ein einzelner Faktor, REV-ERBα, steht an einer wichtigen Kreuzung: Zusammen mit E2F8 prägt er sowohl Rezeptorniveaus als auch den Tagesrhythmus, während das Tollwutvirus ihn zu seinem Vorteil manipuliert. Diese Erkenntnisse deuten auf praktische Ansätze hin. Impfstoffe oder antivirale Medikamente könnten zu bestimmten Tageszeiten besser wirken, wenn Rezeptoren niedrig sind oder die Immunantwort stark. Menschen mit chronisch gestörten Rhythmen — etwa Schichtarbeiter oder Vielreisende — könnten ein erhöhtes Risiko für bestimmte neurotrope Infektionen haben. Die gezielte Beeinflussung von REV-ERBα oder verwandten Wegen könnte helfen, das Gleichgewicht zugunsten des Wirts zu verschieben, Infektionen weniger schwer zu machen und die Ergebnisse zu verbessern.
Zitation: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Schlüsselwörter: circadiane Uhr, neurotrope Viren, Tollwut, virale Rezeptoren, Chronotherapie