Clear Sky Science · de
Dynamische Veränderungen des immunologischen Mikromilieus bei Ovarialkarzinom nach neoadjuvanter Chemotherapie
Warum diese Forschung für Frauen mit Eierstockkrebs wichtig ist
Fortgeschrittener Eierstockkrebs wird häufig mit wirkstarker Chemotherapie vor oder nach einer Operation behandelt, doch bei vielen Frauen tritt die Erkrankung erneut auf und spricht nicht mehr auf die Medikamente an. Diese Studie stellt eine drängende Frage: Wie formt Chemotherapie still und leise die körpereigenen Abwehrkräfte rund um den Tumor um, und können wir diese Reaktion so beeinflussen, dass die Behandlung länger wirksam bleibt? Durch die Analyse einzelner Zellen und die Erprobung neuer Wirkstoffkombinationen in Mäusen identifizieren die Forschenden eine verborgene Rolle fetter, hormonähnlicher Moleküle — der Prostaglandine — dabei, Tumoren nach einer Chemotherapie dem Immunsystem zu entziehen.
Ein sich veränderndes Schlachtfeld um den Tumor
Ovarialtumoren wachsen nicht isoliert: sie liegen in einer dichten „Nachbarschaft“ aus Immunzellen, Bindegewebe und Flüssigkeit im Bauchraum. Schon vor der Behandlung ist dieses Umfeld oft zugunsten des Krebses verschoben, mit wenigen aggressiven Killer‑T‑Zellen und vielen Zellen, die die Immunantwort dämpfen. Das Team wertete zuvor veröffentlichte Einzelzell‑RNA‑Sequenzierungsdaten von Frauen mit hochgradig serösem Ovarialkarzinom aus und verglich Proben vor und nach neoadjuvanter Chemotherapie (vor der Operation verabreichte Chemotherapie). Sie stellten fest, dass die Chemotherapie nicht nur Tumorzellen abtötete; sie löste auch vorübergehend eine Immunreaktion aus, erhöhte Signale, die mit T‑Zell‑Stimulation und Entzündung verbunden sind, und verringerte zugleich einige regulatorische T‑Zellen, die normalerweise Angriffe unterdrücken.
Wenn hilfreiche Veränderungen schädlich werden
Trotz dieses kurzen Schubs treten die meisten Patientinnen weiterhin ein Rezidiv auf und entwickeln eine Resistenz gegenüber Platinpräparaten wie Cisplatin. Um den Grund zu verstehen, untersuchten die Forschenden genauer, wie verschiedene Zelltypen nach der Behandlung miteinander kommunizieren. Sie entdeckten, dass die Chemotherapie die Expression von Genen, die an der Prostaglandinproduktion beteiligt sind, in tumornahen Makrophagen und Fibroblasten stark erhöhte und die Kommunikation zwischen diesen Zellen und T‑Zellen verstärkte. Mit fortgeschrittenen mathematischen Methoden zeigten sie, dass das Gesamtenvironment sich in einen proinflammatorischen, letztlich jedoch unterdrückenden Zustand wandelte, mit steigenden Konzentrationen von Chemokinen, die myeloide Zellen anziehen, und verstärkten Signalwegen, die T‑Zellen mit der Zeit erschöpfen können. Das legt nahe, dass Prostaglandine als molekularer Schalter wirken könnten, der einen zunächst hilfreichen Immunanstieg in eine langanhaltende Bremse der Anti‑Tumor‑Immunität verwandelt.
Chemotherapie, Prostaglandine und stummgeschaltete T‑Zellen
Um diese Idee experimentell zu prüfen, nutzte das Team ein Mausmodell des Eierstockkrebses, das mit Cisplatin behandelt wurde. Die Einzelzellanalyse von Zehntausenden Zellen aus der Bauchhöhle zeigte, dass Cisplatin Tumorzellen reduzierte und die Gesamtzahl der T‑Zellen erhöhte, gleichzeitig aber myeloid‑abgeleitete Suppressorzellen (MDSCs) und erschöpfte Killer‑T‑Zellen deutlich vermehrte. Sowohl Tumorzellen als auch diese Suppressorzellen produzierten hohe Mengen an Enzymen zur Prostaglandinbildung. In Ko‑Kulturen führten cisplatinbehandelte Tumorzellen dazu, dass Knochenmarkszellen einen MDSC‑ähnlichen Zustand annahmen und die Aktivität sowie das Wachstum von CD8+ Killer‑T‑Zellen geschwächt wurde. Die Forschenden führten diesen Effekt auf den NF‑κB‑Signalweg in Tumorzellen zurück, der das Gen PTGES einschaltete — ein entscheidender Schritt zur Produktion von Prostaglandin E2. Die Blockade dieses Weges reduzierte PTGES‑Spiegel und die Prostaglandinausschüttung.
Das Blatt wenden mit Kombinationstherapie
Die praktischste Frage war, ob die Hemmung von Prostaglandinen die Wirksamkeit der Chemotherapie erhöhen kann. Bei Mäusen nutzten die Wissenschaftler genetischen Verlust von Ptges in Tumorzellen, Antikörper, die Prostaglandin E2 neutralisieren, sowie kleinmolekulare Hemmer der Prostaglandin‑E‑Synthase. Alle diese Ansätze senkten die Prostaglandinspiegel, verringerten die Ansammlung von MDSCs und stellten die Fähigkeit der CD8+‑T‑Zellen zum Töten sowie ihre stamzellähnliche Widerstandskraft wieder her. In Kombination mit Cisplatin oder mit dem Standardregime Cisplatin‑Paclitaxel verlangsamten Prostaglandinhemmer das Tumorwachstum und die Ausbreitung effektiver als die Chemotherapie allein. Die Daten deuten darauf hin, dass prostaglandinvermittelte Immunsuppression kein Randphänomen ist, sondern ein zentraler Grund dafür, dass Tumoren nach einer anfänglichen Ansprechphase entkommen.
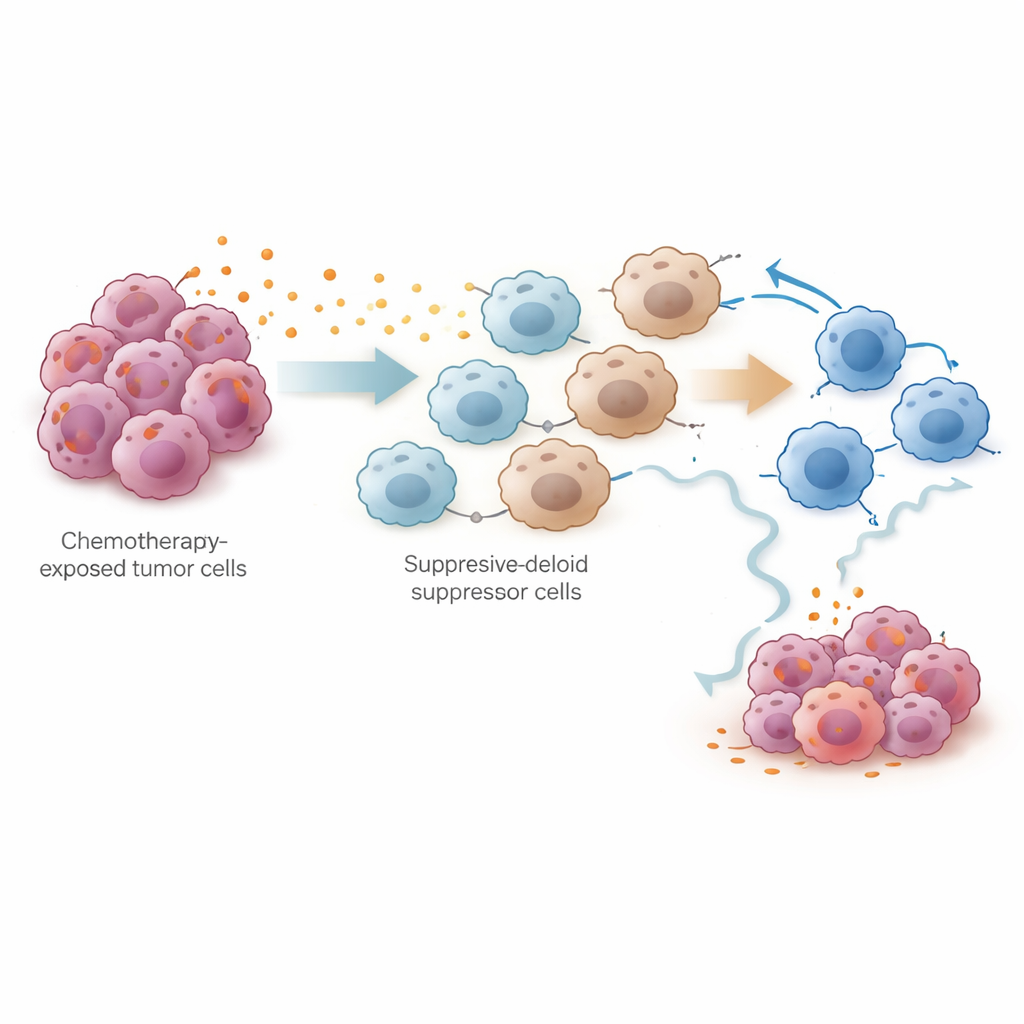
Ein neuer Ansatz, um die Wirksamkeit der Behandlung zu erhalten
Einfach gesagt legt diese Arbeit nahe, dass die Chemotherapie die Umgebung des Tumors in zwei Phasen verändert: Zuerst schwächt sie den Krebs und mobilisiert kurzzeitig das Immunsystem, doch dann löst sie eine Welle von Prostaglandinen aus, die Suppressorzellen anlocken und die körpereigenen tumorabtötenden Kräfte ermüden. Indem die Studie die PTGES‑getriebene Prostaglandinproduktion als Hauptschuldigen identifiziert, weist sie auf eine konkrete Strategie hin: Die Kopplung standardmäßiger Platinchemotherapie mit Medikamenten, die Prostaglandinwege blockieren, könnte helfen, eine starke Immunantwort aufrechtzuerhalten und Rezidive beim Eierstockkrebs zu verzögern oder zu verhindern. Klinische Studien sind zwar noch erforderlich, doch dieser Kombinationsansatz eröffnet eine hoffnungsvolle neue Richtung, um den Nutzen vorhandener Therapien zu verlängern.
Zitation: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Schlüsselwörter: Eierstockkrebs, Tumormikroumgebung, Chemotherapie‑Resistenz, Prostaglandine, Immuntherapie