Clear Sky Science · de
ATP6V1B2 lindert hepatische Steatose, indem es die lysosomale Ansäuerung in Hepatozyten fördert
Warum eine Fettleber wichtig ist
Viele Menschen tragen unbemerkt überschüssiges Fett in ihrer Leber. Dieser Zustand, inzwischen als metabolisch-dysfunktion-assoziierte steatotische Lebererkrankung (MASLD) bezeichnet, betrifft etwa ein Viertel der Weltbevölkerung und kann still zu Vernarbung, Leberversagen und anderen schweren Erkrankungen fortschreiten. Dennoch fehlen den Ärzten verlässliche Methoden, um vorherzusagen, wer sich verschlechtern wird, und nur wenige Therapien richten sich direkt gegen die zugrunde liegenden zellulären Probleme. Diese Studie zeigt, wie eine wenig bekannte zelluläre "Säurepumpe" Leberzellen dabei unterstützt, überschüssiges Fett zu entsorgen, und deutet auf einen neuen Ansatz für Diagnose und Therapie hin.
Ein verborgener Helfer in Leberzellen
In jeder Leberzelle gibt es winzige Recyclingzentren, die Lysosomen genannt werden. Sie sind auf ein inneres Säurebad angewiesen, um abgenutzte Bestandteile und überschüssige Fette abzubauen. Die Säure wird von einer molekularen Pumpe aufrechterhalten, der V-ATPase, die aus mehreren Proteinbausteinen besteht. Die Autorinnen und Autoren konzentrierten sich auf ein entscheidendes Bauteil, ATP6V1B2, das besonders wichtig für die Aufrechterhaltung der Lysosomenacidität ist. Sie fragten, ob Veränderungen dieses Proteins erklären könnten, warum sich bei MASLD Fett ansammelt, und ob seine Konzentration im Blut ein Krankheitszeichen sein könnte.
Hinweise aus Patienten- und Tiermodellen
Als die Forschenden öffentliche genetische Datenbanken und Blutproben von Patientinnen und Patienten untersuchten, stellten sie fest, dass die ATP6V1B2-Spiegel bei Menschen mit MASLD durchgehend niedriger waren und bei denen mit Zirrhose, einer schweren Form von Leberschaden, noch weiter verringert waren. Niedrigere ATP6V1B2-Spiegel in der Leber korrelierten mit mehr Entzündungen, ausgeprägterer Vernarbung und höheren Blutwerten für Leberschäden. In Mausmodellen, die mit fettreichen oder nährstoffveränderten Diäten gefüttert wurden — gängige Methoden, um MASLD nachzuahmen — sank die Leberversorgung mit ATP6V1B2 ebenfalls. Zusammengenommen deuten diese Befunde darauf hin, dass der Verlust dieses Proteins nicht nur eine Begleiterscheinung ist, sondern eng mit dem Fortschreiten der Erkrankung verbunden sein könnte.
Was in gestressten Leberzellen schiefläuft
Um zu sehen, was passiert, wenn ATP6V1B2 gestört ist, wandte sich das Team kultivierten Leberzellen zu, die mit Fettsäuren überladen wurden und so eine "lipotoxische" Umgebung nachbilden. Bei künstlicher Reduktion von ATP6V1B2 vergrößerten sich Fetttröpfchen in den Zellen, schädliche Sauerstoffnebenprodukte stiegen an und die Energieproduktionsstätten der Zelle (Mitochondrien) begannen zu versagen. Stresssignale innerhalb der Zelle stiegen an, und ein zentrales fettsäurebildendes Enzym, die Fettsäuresynthase (FASN), nahm stark zu. Im Gegensatz dazu bewältigten Zellen mit erhöhtem ATP6V1B2 die Fettbelastung deutlich besser: Lipidtröpfchen schrumpften, oxidativer Stress ließ nach und die Mitochondrien erholten sich. Diese Experimente zeigen, dass ATP6V1B2 als schützende Bremse gegen Fettansammlung und Zellschädigung wirkt.
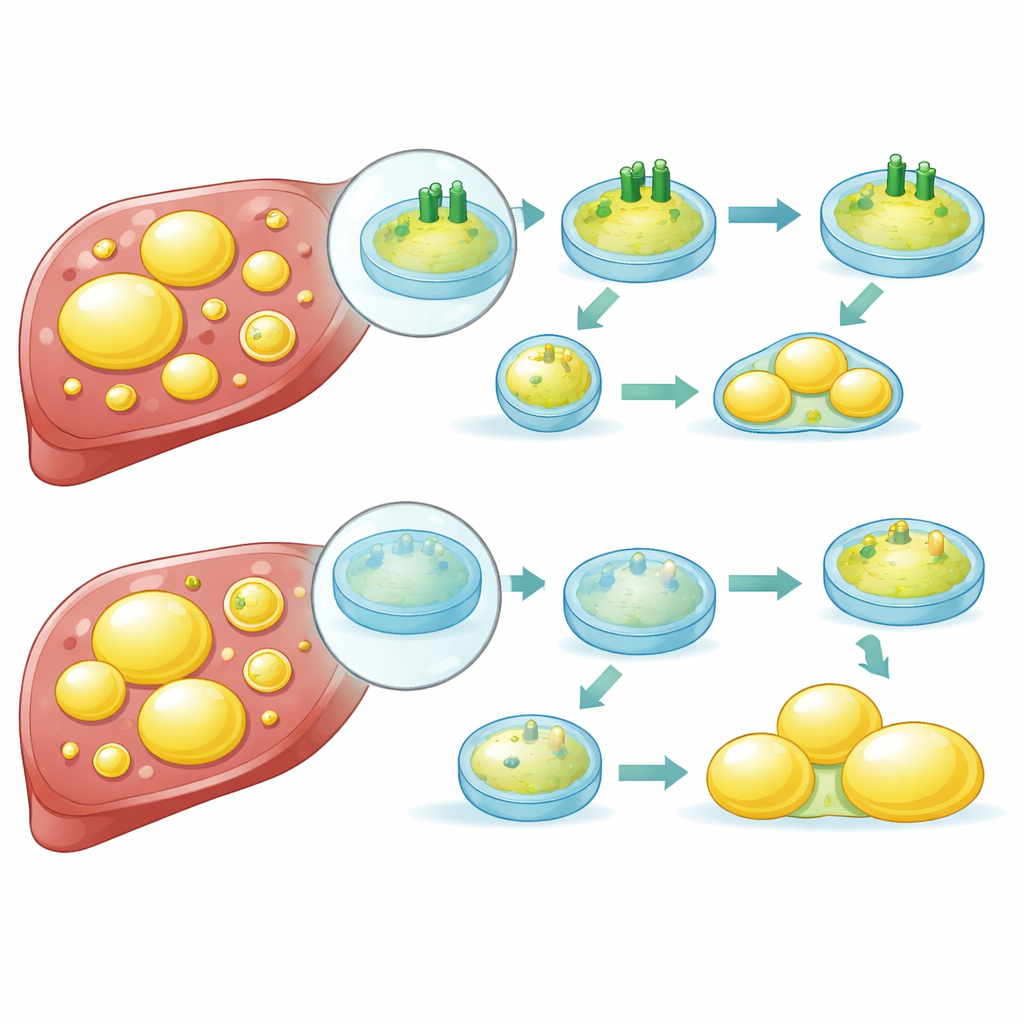
Wie defektes Recycling zur Fettansammlung führt
Bei genauerer Untersuchung entdeckten die Forschenden, dass ATP6V1B2 steuert, wie sauer und aktiv Lysosomen bleiben. Wenn das Protein reduziert war, verloren Lysosomen ihre Acidität, ihre Fähigkeit, Fracht zu zersetzen, nahm ab, und der Materialfluss durch das zelluläre Recyclingsystem (Autophagie) wurde blockiert. Unter normalen Bedingungen kann FASN zur Zerstörung an Lysosomen gesendet werden. Mit funktionierendem ATP6V1B2 läuft dieser Weg effizient, hält die FASN-Spiegel in Schach und begrenzt die Neubildung von Fett. Ist ATP6V1B2 jedoch knapp, können Lysosomen FASN nicht richtig abbauen. Das Enzym sammelt sich an, die Zelle erhöht die Fettsynthese, und die Fetttröpfchen wachsen weiter. Die Studie deutet außerdem an, dass Stresswege innerhalb der Zelle die FASN-Produktion weiter steigern, wenn ATP6V1B2 niedrig ist, und so einen Teufelskreis erzeugen.
Was das für die zukünftige Versorgung bedeutet
Für Nicht-Spezialisten ist die Botschaft klar: Ein einzelnes Protein, das Lysosomen hilft, sauer zu bleiben, kann maßgeblich beeinflussen, ob Leberzellen Fett speichern oder abbauen. Niedrigere ATP6V1B2-Werte, beobachtet sowohl bei Patientinnen und Patienten als auch in MASLD-Modellen, schwächen das interne Recyclingsystem der Leber und erlauben, dass Fett und Schäden sich anhäufen. Die Messung dieses Proteins im Blut könnte Ärzten helfen, die Schwere der Erkrankung einzuschätzen, und Strategien, die die Lysosomenacidität wiederherstellen oder die ATP6V1B2-Aktivität steigern, könnten die Grundlage neuer Therapien bilden. Indem die Studie Licht auf diese "Säurepumpe" und ihre Kontrolle über fettverarbeitende Enzyme wirft, weist sie auf lysosomenfokussierte Therapien als vielversprechenden Weg hin, Fettlebererkrankungen aufzuhalten oder umzukehren.
Zitation: Xu, R., Yang, F., Zhang, Z. et al. ATP6V1B2 alleviates hepatic steatosis by promoting lysosomal acidification in hepatocytes. Cell Death Discov. 12, 170 (2026). https://doi.org/10.1038/s41420-026-03052-8
Schlüsselwörter: Fettlebererkrankung, Lysosomen, Autophagie, Lipidstoffwechsel, Leberentzündung