Clear Sky Science · de
Der epigenetische Kontext bestimmt die transkriptionelle Aktivität des kanonischen und nicht-kanonischen NF-κB-Signalwegs beim Pankreaskarzinom
Warum diese Studie für Patientinnen und Patienten wichtig ist
Pankreaskrebs gehört zu den tödlichsten Krebsarten, zum Teil weil seine Zellen besonders gut darin sind, Gefahrensignale aus ihrer Umgebung zu erkennen und darauf zu reagieren. Diese Studie betrachtet zwei solcher Signale, TNFα und TWEAK, und zeigt, wie sie in der DNA von Krebszellen verschiedene „Lesemodi“ aktivieren. Das Verständnis dieser Modi könnte neue Wege eröffnen, um Tumorwachstum zu verlangsamen, Metastasierung einzuschränken und Therapien wirksamer zu machen.
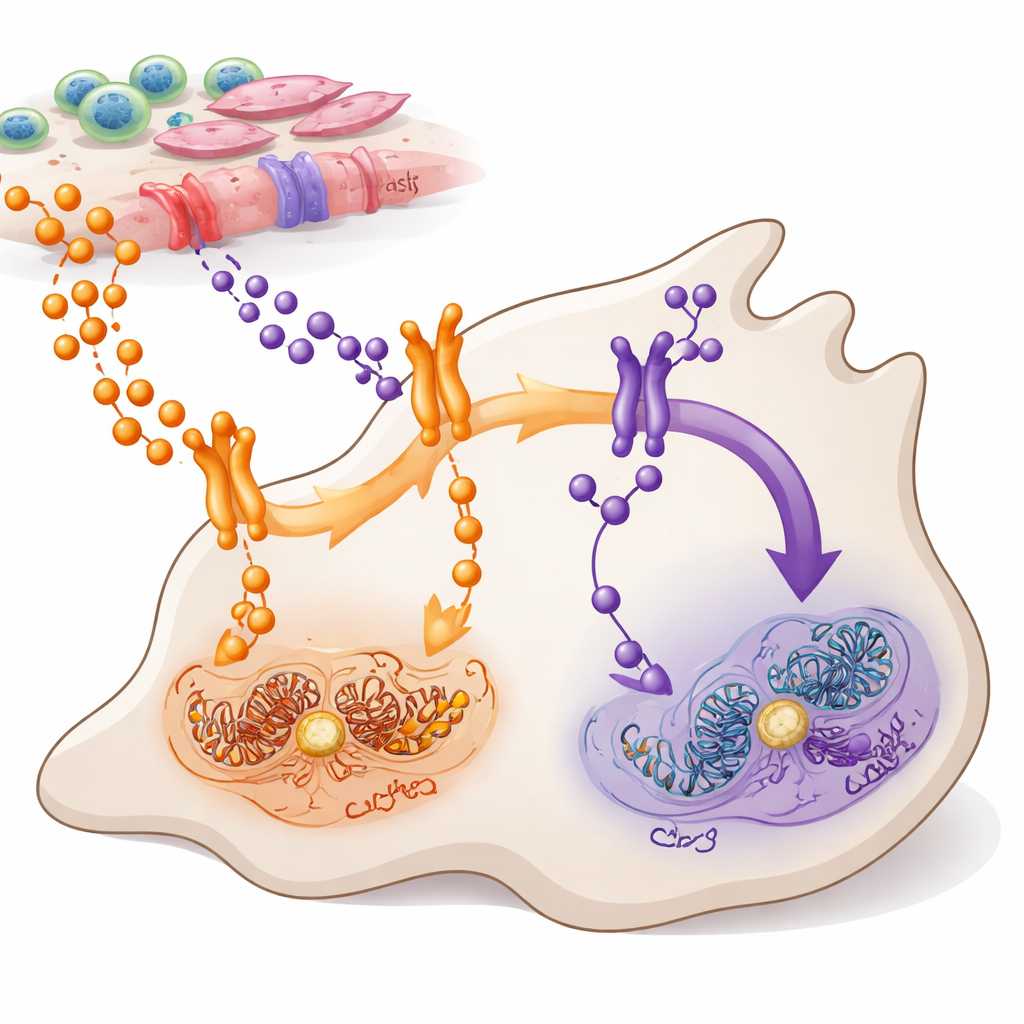
Zwei Signalwege in die Krebszellen
TNFα und TWEAK sind kleine Proteinboten, die von Zellen im und um einen Tumor freigesetzt werden. Beide sprechen ein wichtiges Kontrollsystem in den Zellen an, das als NF-κB bekannt ist und mitentscheidet, ob Zellen wachsen, sich bewegen oder sterben. Die Autorinnen und Autoren konzentrierten sich auf das duktale Adenokarzinom des Pankreas, die häufigste und aggressivste Form von Pankreaskrebs, in der NF-κB in den meisten Tumoren überaktiv ist. Sie kartierten, welche Zellen TNFα und TWEAK produzieren, welche Zellen deren Rezeptoren tragen und wie diese Signale über zwei verwandte NF-κB-Zweige — meist als kanonischer (via RELA) und nicht-kanonischer (via RELB) Weg bezeichnet — weitergeleitet werden.
Wer die Signale in der Tumornachbarschaft sendet
Durch die Kombination von Einzelzell-RNA-Sequenzierung aus tausenden Zellen von Patiententumoren mit fortgeschrittener Mikroskopie fanden die Forschenden heraus, dass TNFα hauptsächlich von Immunzellen stammt, insbesondere von Makrophagen sowie bestimmten T‑ und B‑Zellen. TWEAK hingegen wird von einer breiteren Gruppe produziert: Makrophagen, Fibroblasten, Endothelzellen und Sternzellen. Auch die Rezeptoren unterscheiden sich. Tumorzellen und benachbarte Fibroblasten exprimieren stark den Hauptrezeptor für TNFα und den wichtigen TWEAK-Rezeptor. Netzwerkanalysen deuteten darauf hin, dass TWEAK-basierte Signalgebung ein weiter gespanntes und komplexeres Kommunikationsnetzwerk zwischen Tumor- und Stützzellen bildet, während TNFα-Signalgebung stärker auf immunreiche Bereiche fokussiert ist.
Unterschiedliche Reaktionsstärken in Tumorzellen
In Pankreaskrebs-Zelllinien behandelten die Forschenden Zellen mit TNFα oder TWEAK und maßen, welche Gene sich im Zeitverlauf einschalteten. TNFα löste eine schnelle und breite Welle von Genaktivität aus, die mit Entzündung, Zellbewegung, Umbau von Gewebe und Überleben verknüpft ist. TWEAK induzierte eine kleinere, langsamere Veränderung, die größtenteils mit den Zielgenen von TNFα überlappte, anstatt ein völlig eigenständiges Programm zu starten. Beide Signale konnten Zellmigration fördern und unter bestimmten Bedingungen auch zum Zelltod führen, doch TNFα hatte den stärkeren Effekt auf die Bewegung. Bei der Auswertung von Patientendaten aus The Cancer Genome Atlas zeigten Tumoren mit hohen TNFα‑ oder hohen TWEAK‑Werten viele gemeinsame aktivierte Gene, was diese Muster auch in menschlichen Tumoren bestätigte.
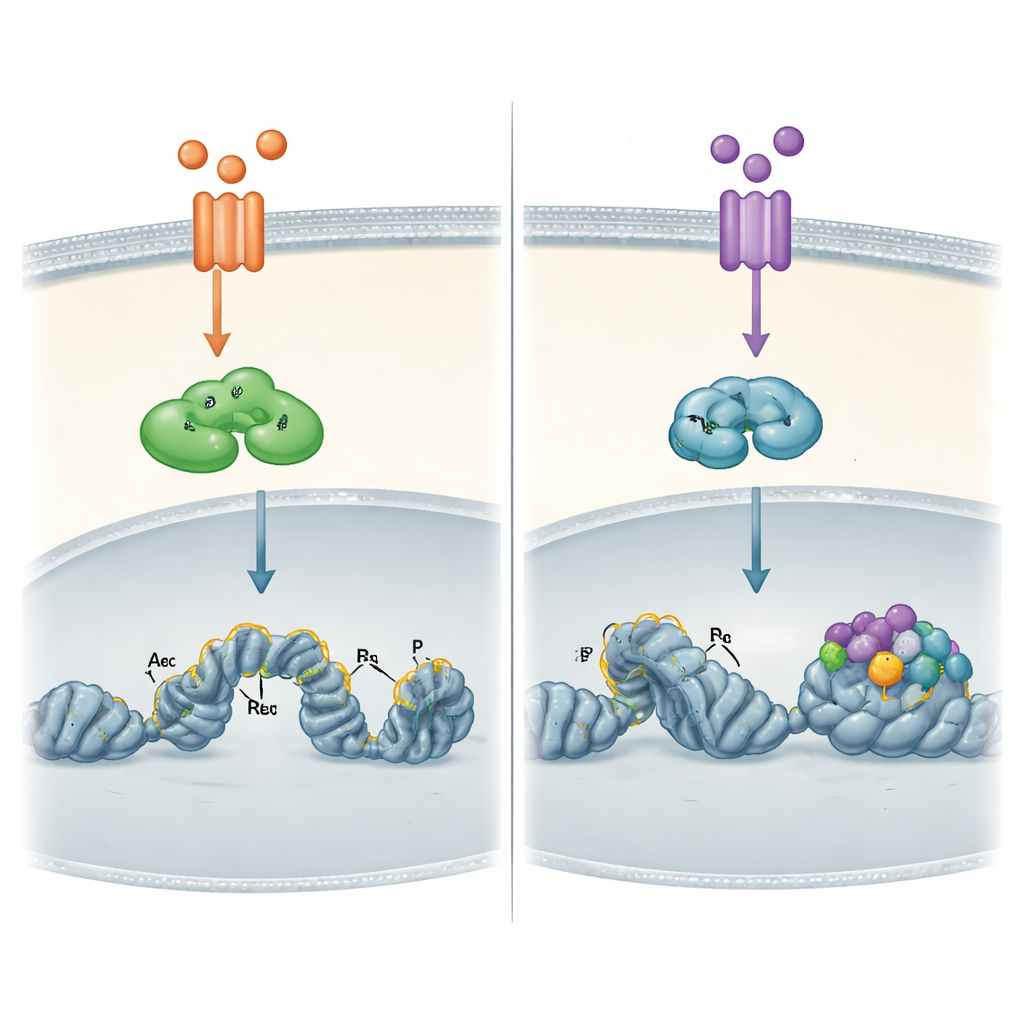
Wie die DNA-Landschaft jeden Weg formt
Die auffälligsten Unterschiede traten auf, als die Autorinnen und Autoren direkt das Chromatin der Krebszellen untersuchten — die kompakte Form von DNA und ihren assoziierten Proteinen. Mithilfe genomweiter Bindungskarten zeigten sie, dass das durch TNFα aktivierte RELA nicht nur an bereits offene DNA‑Regionen binden kann, sondern auch an stärker verpackte Bereiche und diese dann durch das Setzen chemischer Markierungen, die mit aktiven Schaltern assoziiert sind, „öffnen“ hilft. RELB, das später durch TWEAK aktiviert wird, band hingegen nahezu ausschließlich an Stellen, die bereits zugänglich und mit solchen aktiven Markierungen versehen waren. Diese RELB‑Stellen wiesen besonders viele Andockmotive für eine andere Faktorgruppe, AP‑1, auf, was darauf hindeutet, dass RELB auf andere Proteine angewiesen ist, die das Terrain vorbereiten, bevor es wirken kann.
Was das für zukünftige Behandlungen bedeutet
Für Nicht-Fachleute ist die zentrale Erkenntnis, dass TNFα und TWEAK dasselbe NF-κB‑Werkzeugset auf sehr unterschiedliche Weise nutzen. TNFα verhält sich über RELA wie ein Hauptschalter, der verschlossene Abschnitte der Krebszell‑DNA aufbrechen und ein breites Spektrum von Genen aktivieren kann, die an Wachstum, Überleben und Ausbreitung beteiligt sind. TWEAK wirkt über RELB eher wie ein Spezialist, der nur dort operieren kann, wo die DNA bereits offen ist und Ko‑Faktoren wie AP‑1 vorhanden sind. Diese Arbeitsteilung legt nahe, dass Medikamente, die Chromatin‑Remodelling, AP‑1 oder spezifische NF-κB‑Zweige ansprechen, schädliche Genprogramme beim Pankreaskrebs selektiv abschwächen könnten, während andere Funktionen weitgehend erhalten bleiben.
Zitation: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Schlüsselwörter: Pankreaskrebs, NF-kappaB-Signalgebung, Tumormikroumgebung, epigenetische Regulation, TNF und TWEAK