Clear Sky Science · de
Glutamat-Decarboxylase 1 (GAD1) unterdrückt das Fortschreiten von Glioblastom über den GSK3β/β-Catenin-Signalweg
Warum diese Studie zu Hirntumoren wichtig ist
Das Glioblastom gehört zu den tödlichsten Formen von Hirnkrebs: Die meisten Patientinnen und Patienten überleben nach der Diagnose kaum länger als ein Jahr. Die derzeitigen Behandlungen – Operation, Strahlentherapie und Chemotherapie – verhindern meist nicht, dass die Krankheit zurückkehrt. Diese Studie untersucht einen überraschenden Verbündeten, der bereits in Gehirnzellen vorhanden ist: das Enzym GAD1. Die Ergebnisse deuten darauf hin, dass eine Erhöhung seiner Aktivität das Tumorwachstum und die Ausbreitung verlangsamen könnte.
Ein stiller Verteidiger in Gehirnzellen
GAD1 ist vor allem für seine Rolle in gesunden Neuronen bekannt, wo es hilft, den beruhigenden Neurotransmitter GABA zu produzieren. Die Forschenden fragten sich, ob dieses Enzym auch Einfluss auf Gehirntumoren haben könnte. Beim Vergleich von Glioblastomzellen mit normalen Stütz- bzw. Gliazellen des Gehirns stellten sie fest, dass die GAD1-Spiegel in Krebszellen durchweg niedriger waren. Große Patientendatenbanken bestätigten, dass Tumoren mit geringerem GAD1 mit kürzeren Überlebenszeiten verbunden waren, was darauf hindeutet, dass GAD1 in dieser Erkrankung eher als Bremse denn als Beschleuniger wirkt.
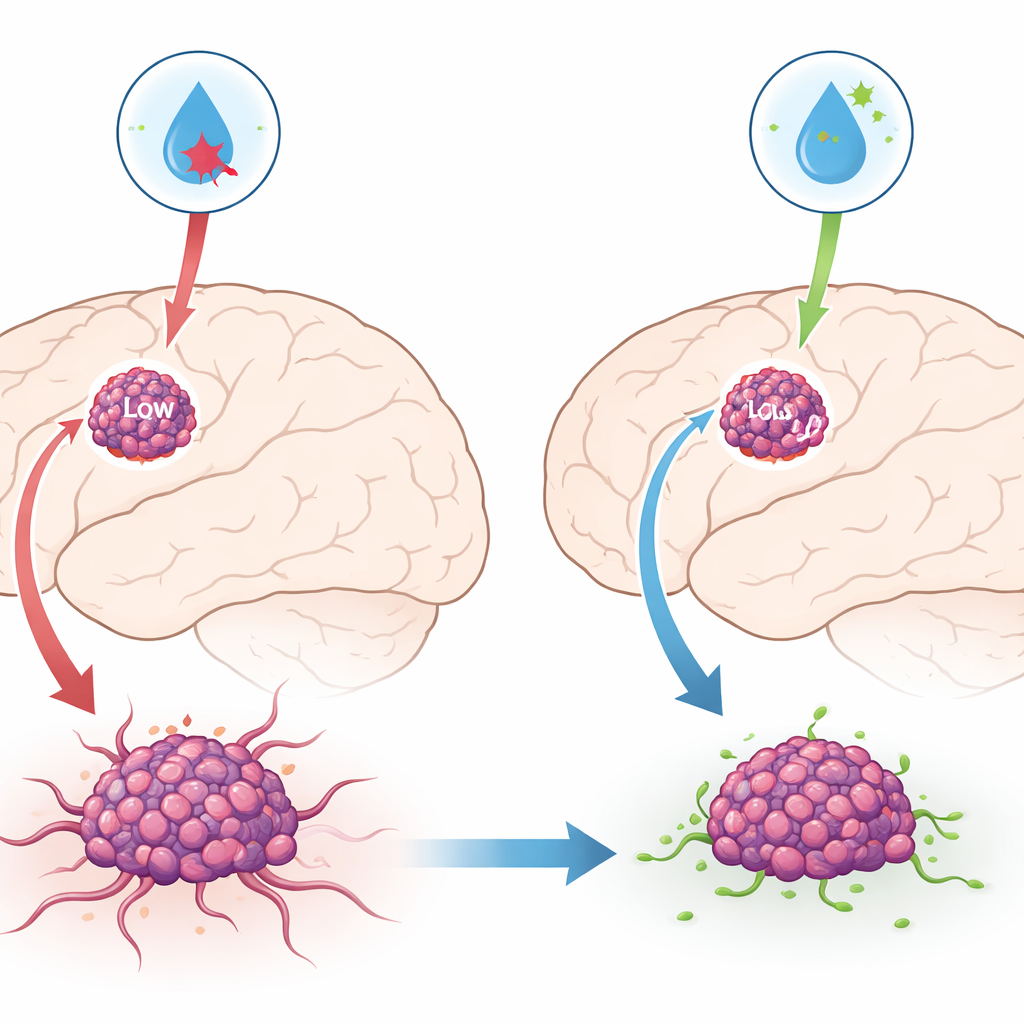
Die Bremse hoch- oder herunterziehen
Um diese Idee zu prüfen, veränderte das Team künstlich GAD1-Level in mehreren humanen Glioblastomzelllinien, die im Labor gezüchtet wurden. Bei gesteigertem GAD1 teilten sich die Tumorzellen langsamer, bildeten weniger Kolonien, wanderten weniger über einen künstlichen Kratzer in einer Schale und hatten größere Schwierigkeiten, durch ein Gel vorzudringen, das das umgebende Gewebe nachahmt. Bei reduzierten GAD1-Werten zeigte sich das Gegenteil: Die Zellen durchliefen den Zellzyklus schneller, breiteten sich leichter aus und drangen tiefer vor. Diese Experimente zeigen, dass GAD1 erheblichen Einfluss auf die Aggressivität von Glioblastomzellen hat.
Ein verborgenes Steuerkreislauf innerhalb des Tumors
Die Forschenden untersuchten anschließend, wie GAD1 diese Kontrolle ausübt. Ihr Blick richtete sich auf einen internen Signalweg um das Protein GSK3β und den bekannten Wachstumsregulator β-Catenin. In vielen Krebsarten fördert eine hohe Aktivität dieses Weges die Zellteilung und Invasion. Die Wissenschaftler fanden heraus, dass höhere GAD1-Werte zentrale Schritte dieses Pfades dämpften und dadurch die Mengen zweier wichtiger Proteine verringerten, die den Zellzyklus und die Gewebeinvasion antreiben. Eine Senkung von GAD1 schaltete diesen Weg an und stellte diese Wachstums- und Invasionssignale wieder her. Interessanterweise konnte die einfache Zugabe von zusätzlichem GABA – dem chemischen Produkt, dessen Bildung GAD1 normalerweise unterstützt – die Effekte des GAD1-Verlustes nicht rückgängig machen, was darauf hindeutet, dass das Enzym Tumorverhalten auch über zusätzliche, nicht-klassische Mechanismen beeinflusst.
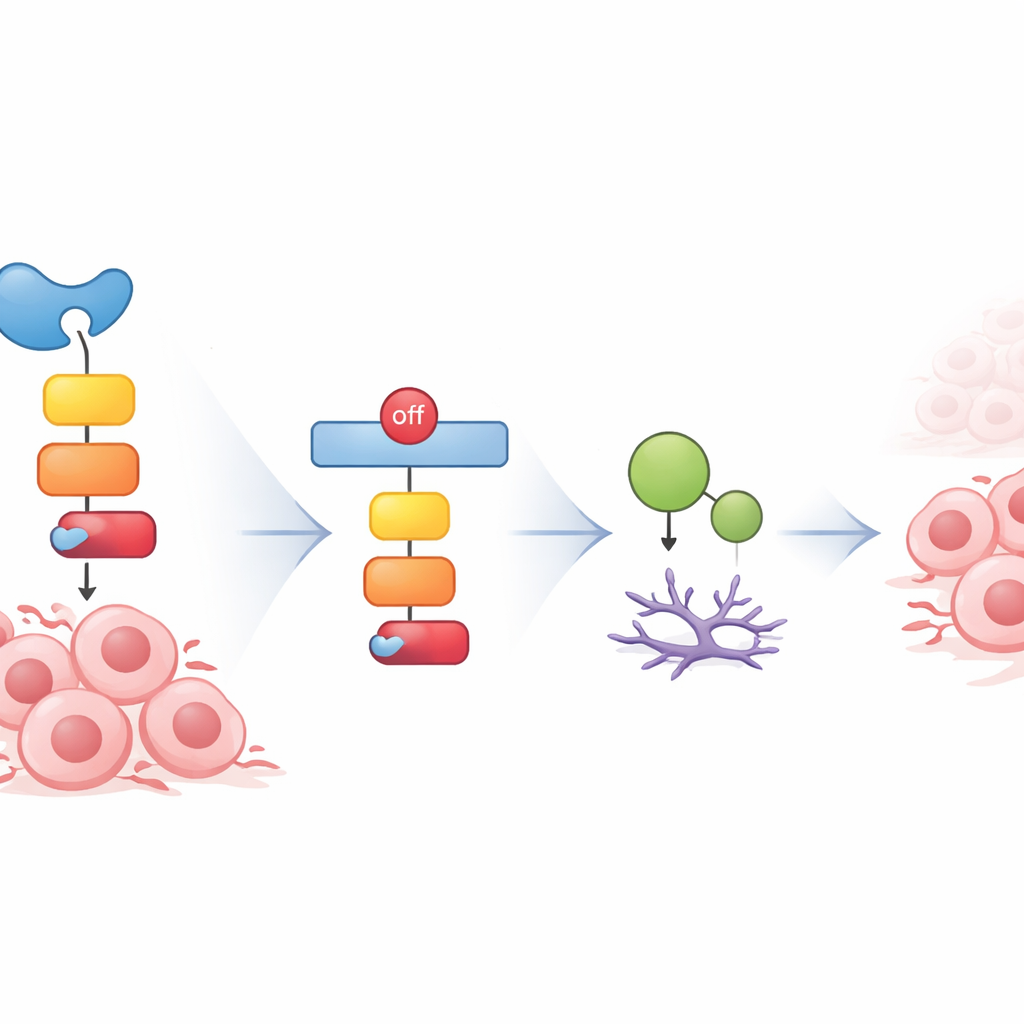
Medikamententests und kleine Fische zeigen Wirkung in lebenden Systemen
Da die Effekte von GAD1 über GSK3β liefen, verwendete das Team ein niedermolekulares Medikament, das diese Kinase blockiert, um zu prüfen, ob sich der Einfluss des GAD1-Verlusts neutralisieren lässt. In Glioblastomzellen mit reduziertem GAD1 reduzierte der Inhibitor die Proliferation, verlangsamte den Zellzyklus und verringerte die Invasion, während er gleichzeitig dieselben downstream liegenden Proteine abschwächte, die mit Wachstum und Ausbreitung verbunden sind. Um über Zellkulturbefunde hinauszugehen, implantierten die Forschenden fluoreszent markierte humane Tumorzellen in transparente Zebrafisch-Larven und schufen so ein lebendes Modell, in dem das Tumorwachstum in Echtzeit beobachtet werden konnte. Tumoren, die so verändert wurden, dass sie vermehrt GAD1 produzierten, blieben kleiner und die Fische überlebten länger, während GAD1-unterdrückte Tumoren größer wuchsen und die Überlebenszeit verkürzten.
Was das für künftige Behandlungen bedeuten könnte
In der Summe zeichnen die Ergebnisse ein Bild von GAD1 als eingebautem Schutzmechanismus, der das Glioblastom durch Abschwächung eines mächtigen Wachstums- und Invasionskreislaufs in Tumorzellen zurückhält. Bei niedrigen GAD1-Werten läuft dieser Kreislauf ungebremst, was erklärt, warum Patientinnen und Patienten mit solchen Tumoren schlechtere Prognosen haben. Zwar bleiben viele Fragen offen – etwa, wie genau GAD1 mit dem GSK3β-Schalter verbunden ist – doch macht diese Arbeit GAD1 und seinen nachgeschalteten Signalweg zu vielversprechenden Zielen für neue Therapien. Langfristig könnten Medikamente, die die Aktivität von GAD1 steigern oder seinen dämpfenden Einfluss auf dieses Signalisierungsnetz nachahmen, einen neuen Ansatz bieten, um eine der aggressivsten Formen von Hirnkrebs zu verlangsamen.
Zitation: Zheng, Y., Zhong, Z., Zhang, C. et al. Glutamate decarboxylase 1 (GAD1) suppresses the progression of glioblastoma through GSK3β/β-catenin pathway. Cell Death Discov. 12, 132 (2026). https://doi.org/10.1038/s41420-026-02997-0
Schlüsselwörter: Glioblastom, Gehirntumor, GAD1, Tumorsignalisierung, Zebrafischmodell