Clear Sky Science · de
Ausnutzung von Pyroptose in der Brustkrebsbehandlung: immunologische Mechanismen und aufkommende Biomaterial‑Strategien
Zellsterben als neue Waffe gegen Brustkrebs
Brustkrebs bleibt weltweit eine der häufigsten und hartnäckigsten Krebsarten. Viele Tumoren entziehen sich langfristig Operationen, Chemotherapie und selbst modernen Immuntherapien. Diese Übersicht beleuchtet eine aufkommende Idee: das gezielte Auslösen einer feurigen Form des Zellsterbens, der Pyroptose, innerhalb von Brusttumoren. Indem Krebszellen kontrolliert aufplatzen und entzündliche Signale freisetzen, hoffen Forscher, den Tumor direkt zu töten und das Immunsystem zur Unterstützung der Abwehr zu mobilisieren.
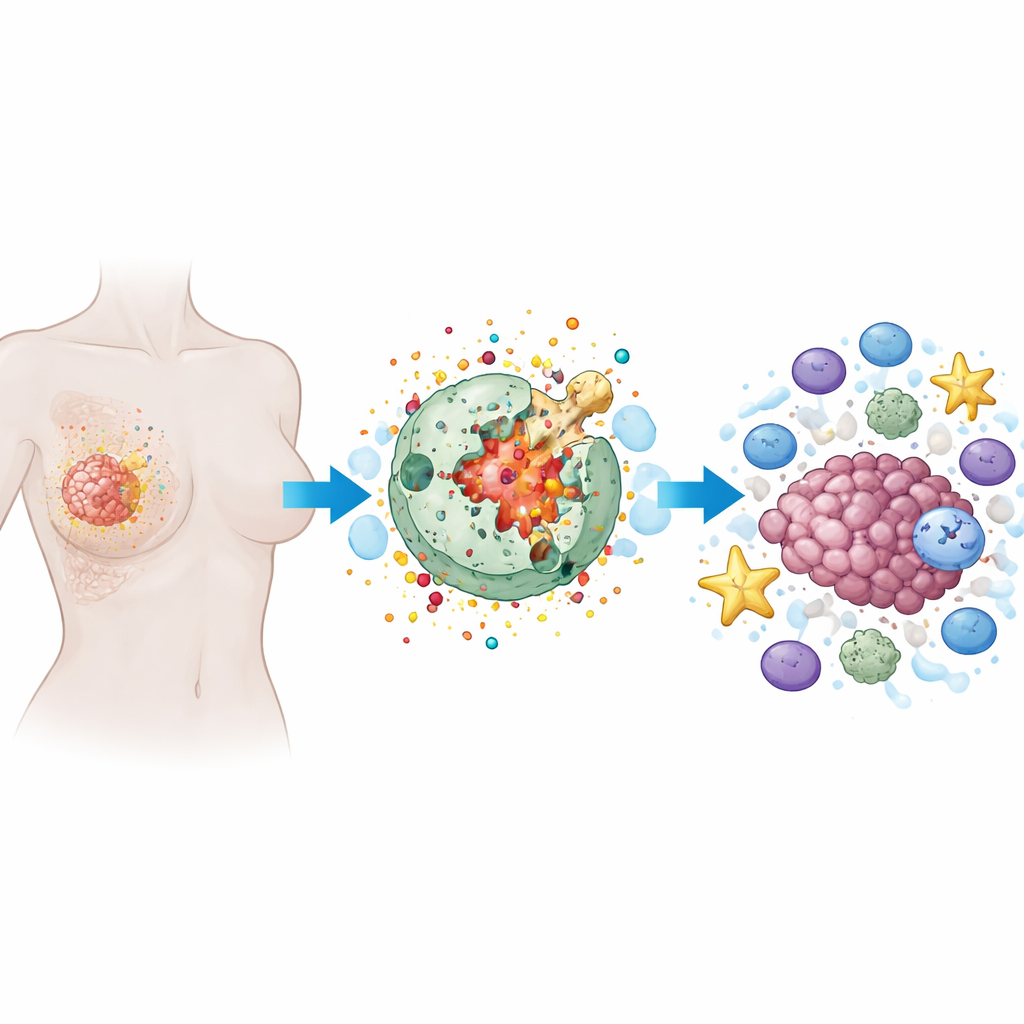
Wie eine feurige Form des Zellsterbens funktioniert
Pyroptose ist eine programmierte Form des Zellsterbens, bei der eine Zelle anschwillt, die Außenmembran von Poren durchsetzt wird und sie schließlich aufreißt und ihren Inhalt freisetzt. Anders als das stille, ordentliche Zellsterben, das bei vielen Therapien beobachtet wird, ist Pyroptose laut und entzündlich. Spezialisierte Proteine, vor allem eine Familie namens Gasdermine, wirken wie winzige Sprengladungen. Nach dem Schnitt durch intrazelluläre Enzyme bohren Gasdermine Löcher in die Zellmembran. Das zerstört nicht nur die Krebszelle, sondern setzt auch Alarm‑ und Entzündungssignale frei, die Immunzellen anziehen und aktivieren können.
Warum Brusttumoren eine besondere Herausforderung sind
Brustkrebs ist keine einzelne Krankheit, sondern ein Spektrum von Subtypen mit unterschiedlichen Eigenschaften. Einige, wie das triple‑negative Mammakarzinom, fehlen gängige Arzneimittelziele und zeigen häufig Therapieresistenz. Viele Brusttumoren gelten als „immunologisch kalt“, das heißt, sie enthalten nur wenige aktive Immunzellen. Die Übersicht erklärt, wie Merkmale des Tumormilieus — einschließlich Stromazellen, immunsuppressiver Zellen und lokaler Sauerstoffknappheit — sowohl Voraussetzungen für Pyroptose schaffen als auch, wenn schlecht kontrolliert, deren Entzündung als Treibstoff für Tumorwachstum und Metastasierung nutzen können. Diese Doppelwirkung macht besondere Präzision erforderlich.
Die Gasdermin‑Schalter in Tumorzellen
Ein zentrales Thema des Artikels ist, wie verschiedene Gasdermin‑Proteine als molekulare Schalter in Brustkrebszellen fungieren. Varianten wie GSDMD und GSDME können Signale aus Chemotherapie, Strahlentherapie oder angreifenden Immunzellen in eine vollständige Pyroptose umwandeln. Andere, etwa GSDMC und bestimmte Formen von GSDMB, sind in aggressiven Tumoren oft erhöht und können je nach Aktivierungsmodus Krankheit fördern oder hemmen. Viele Brustkrebserkrankungen schalten GSDME chemisch stumm, was Pyroptose und Immunaktivierung abschwächt. Die Wiederherstellung oder selektive Aktivierung der richtigen Gasdermine könnte darüber entscheiden, ob eine Therapie nur einige Zellen tötet oder den gesamten Tumor in eine in‑situ‑Vakzine verwandelt, die das Immunsystem alarmiert.
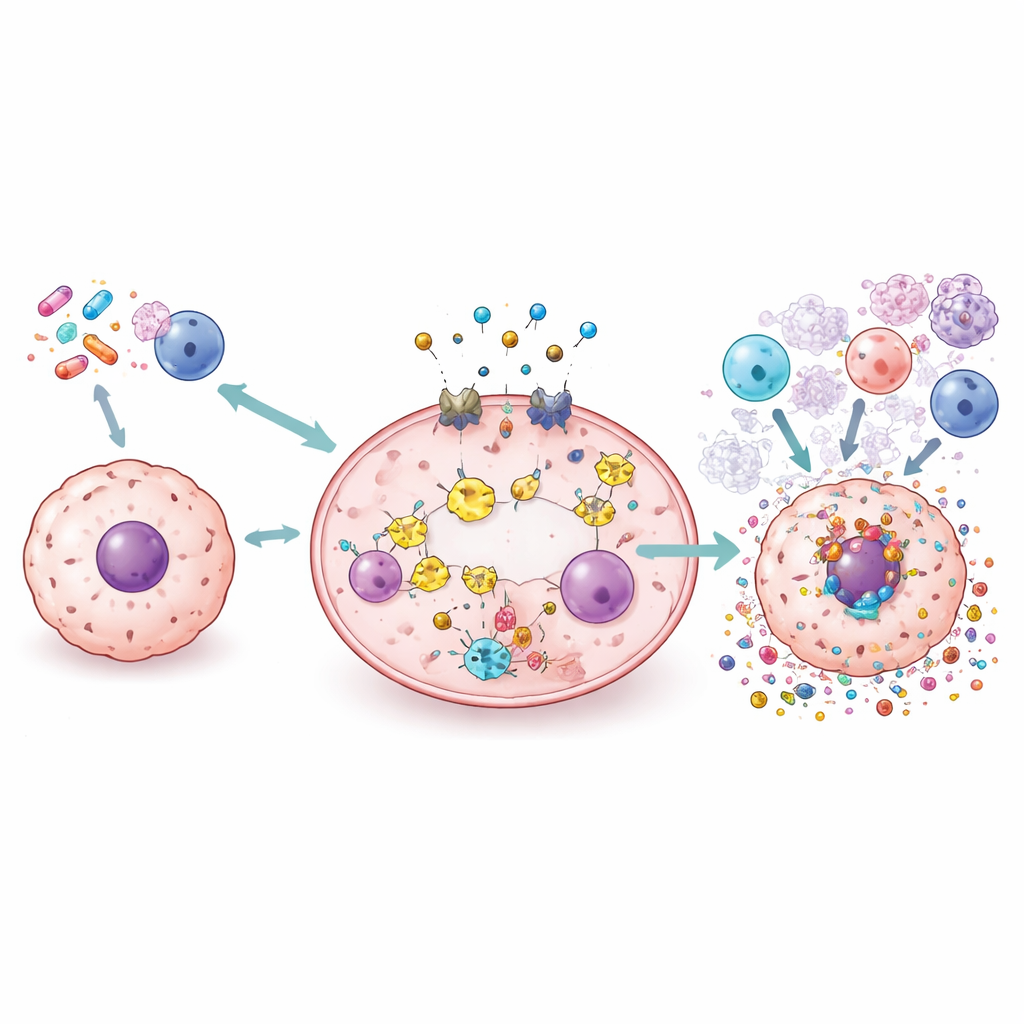
Neue Werkzeuge: Medikamente, Nanopartikel, Viren und Strahlung
Die Übersichtsarbeit beschreibt ein breites Spektrum an Strategien, die untersucht werden, um Pyroptose sicher zu nutzen. Standardmedikamente wie Cisplatin und Doxorubicin können umfunktioniert oder neu formuliert werden, um Krebszellen eher in gasderminvermittelte Explosionen als in stilles Sterben zu treiben. Kleine Moleküle können Teile des Signalwegs verstärken oder blockieren, um die Entzündungsreaktion fein zu justieren. Nanopartikel und biomimetische Träger werden entwickelt, um Chemotherapie, Kupferionen oder lichtaktivierbare Wirkstoffe direkt in Tumore zu liefern, wo sie Pyroptose auslösen und gesundes Gewebe schonen. Onkolytische Viren und Strahlentherapie lassen sich ebenfalls so gestalten oder kombinieren, dass sie Pyroptose provozieren und das immunologische Milieu des Tumors umformen, wodurch Immuncheckpoint‑Medikamente möglicherweise wirksamer werden.
Nutzen abwägen gegenüber realen Risiken
Da Pyroptose sehr entzündlich ist, können dieselben Reaktionen, die dem Immunsystem helfen, den Krebs zu bekämpfen, auch normales Gewebe schädigen oder bei chronischer Aktivität das Tumorwachstum fördern. Die Autoren heben frühe Biomarker hervor — wie Genprofile, Methylierungsmuster, Fragmente von Gasdermin‑Proteinen im Blut und Zytokinmuster —, die dabei helfen könnten zu identifizieren, welche Patientinnen am wahrscheinlichsten profitieren und wer ein erhöhtes Risiko für gefährliche "Zytokinstürme" hat. Fortschrittliche Nanomedizin‑Designs, sorgfältig gewählte Wirkstoffkombinationen und Echtzeitüberwachung entzündlicher Marker werden geprüft, um die Reaktion kraftvoll, aber kontrolliert zu halten.
Was das für zukünftige Patientinnen bedeuten könnte
Kurz gesagt argumentiert die Übersicht, dass das „laute Sterben“ von Krebszellen die Behandlung von Brustkrebs transformieren könnte. Durch das gezielte Auslösen von Pyroptose in einem präzisen Subset von Tumorzellen könnten Ärztinnen sowohl den Tumor verkleinern als auch eine starke, dauerhafte Immunantwort wecken, kalte Tumoren erwärmen und sie für moderne Immuntherapien empfänglicher machen. Pyroptose ist jedoch ein volatiler Verbündeter: Wird sie zu breit oder zu lange entfesselt, kann sie Entzündungen verschlimmern oder resistente Zellen begünstigen. Zukünftige Forschung wird sich darauf konzentrieren, zu kartieren, wer profitieren wird, zielgerichtete Liefersysteme zu perfektionieren und klinische Studien durchzuführen, die pyroptoseinduzierende Ansätze mit Immuntherapeutika kombinieren. Wenn diese Herausforderungen gemeistert werden, könnte die Nutzung von Pyroptose der Brustkrebsbehandlung eine neue, kraftvolle Dimension hinzufügen.
Zitation: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Schlüsselwörter: Pyroptose, Brustkrebs, Gasdermin, tumorales Mikroumfeld, Nanomedizin