Clear Sky Science · de
Absolute Dynamik und relative Statik: die Beziehung von Glykolyse und OXPHOS in der Krebsentwicklung
Warum die Energieentscheidungen von Krebs wichtig sind
Krebszellen gleichen Extremsportlern mit Ausdauermodus: Sie müssen sich ständig mit Energie versorgen, um zu wachsen, sich auszubreiten und Therapien zu entgehen. Diese Übersicht erklärt, wie Tumorzellen zwei Hauptenergiesysteme anzapfen—eines schnell, das andere effizient—und vor allem, wie sie diese mischen und zwischen ihnen wechseln. Das Verständnis dieser wechselnden Energiestrategien eröffnet neue Perspektiven für Diagnostik und Therapie über den gesamten Verlauf der Erkrankung.
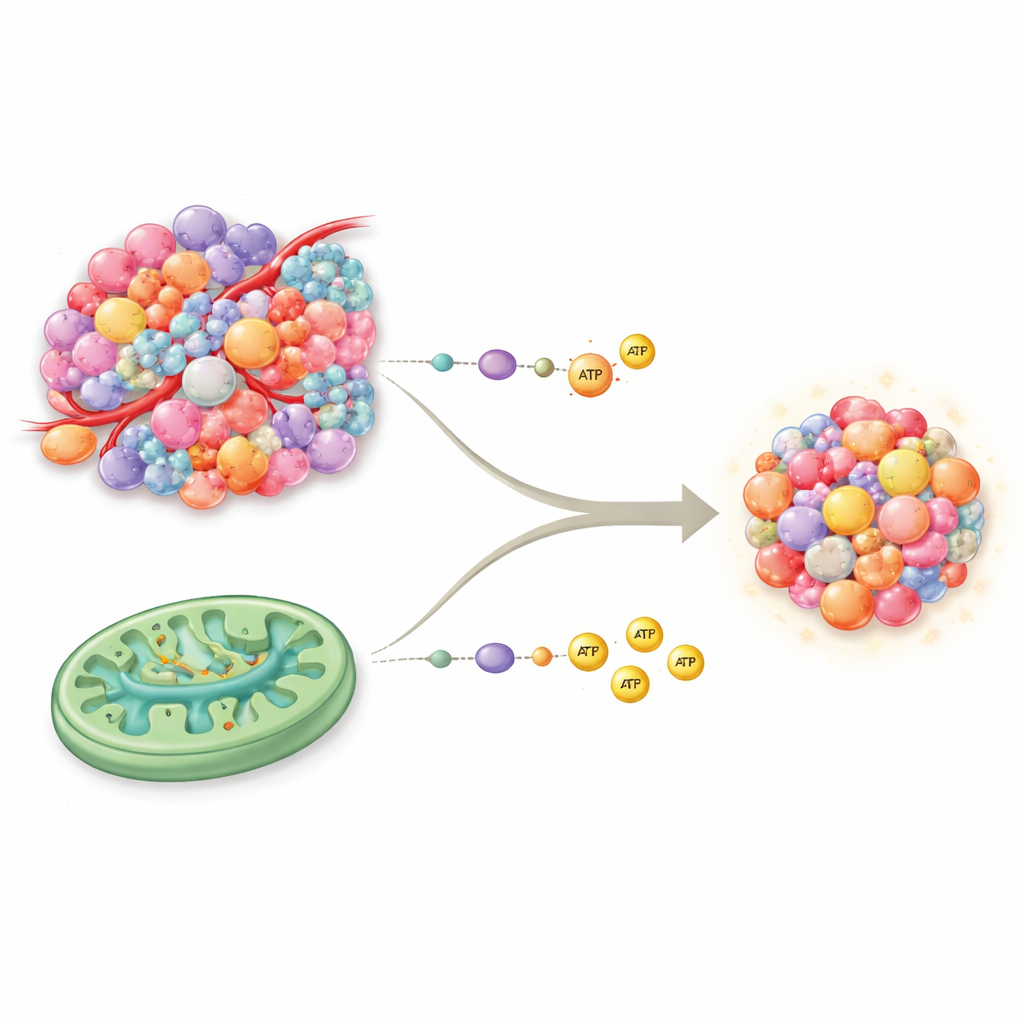
Zwei grundlegende Wege, wie Zellen Energie erzeugen
Unsere Zellen erzeugen Energie in der Regel über zwei Kernwege. Die Glykolyse ist das schnelle, „Bargeld“-System, das Zucker rasch abbaut, aber pro Einheit relativ wenig Energie liefert. Die oxidative Phosphorylierung, kurz OXPHOS, läuft in den Mitochondrien und ähnelt einem hocheffizienten Kraftwerk: Sie produziert deutlich mehr Energie, benötigt dafür aber gute Sauerstoff- und Nährstoffversorgung. Über Jahrzehnte hielt man Krebs für fast ausschließlich glykolytisch, selbst bei vorhandenen Sauerstoff—ein Muster, das als Warburg-Effekt bekannt ist. Neuere Befunde widerlegen diese einfache Sicht: Viele Tumoren besitzen voll funktionsfähige Mitochondrien und können OXPHOS und den Zitratzyklus (TCA) neben der Glykolyse nutzen, was ihnen ein reicheres und flexibleres Energieset verleiht als zuvor angenommen.
Viele Zelltypen, viele Energieoptionen
Ein Tumor ist keine einheitliche Masse. Er ist ein kleines Ökosystem aus Krebszellen, Stütz- und Gefäßzellen sowie Immunzellen, die jeweils unterschiedliche Energiebedürfnisse haben. Manche Krebszellen liegen nahe an Blutgefäßen und profitieren von reichlich Sauerstoff und Nährstoffen; andere sind in schlecht versorgten Regionen vergraben. Folglich können Zellen innerhalb desselben Tumors die Glykolyse bevorzugen, hauptsächlich auf OXPHOS setzen oder beide Wege gleichzeitig nutzen. Diese metabolische Vielfalt—auch Heterogenität genannt—entsteht durch Unterschiede in Durchblutung, Nährstoffkonzentration, Zelltyp und Signalen aus der Umgebung. Hinzu kommt oft metabolische Symbiose: glykolytische Zellen exportieren Laktat als scheinbares Abfallprodukt, das benachbarte OXPHOS‑abhängige Zellen importieren und als wertvollen Brennstoff verbrennen. Ähnliches Laktat-Sharing findet zwischen Krebszellen und Stützzellen wie Fibroblasten, Gefäßzellen oder immunsuppressiven Zellen statt und trägt gemeinsam dazu bei, dass der Tumor gedeiht und Therapien widersteht.
Ständig im Wandel: wie sich die Energie des Tumors über die Zeit verschiebt
Der Tumorstoffwechsel ist nicht nur zu einem gegebenen Zeitpunkt heterogen; er ist auch hochdynamisch. Während Tumoren wachsen, stoßen sie auf veränderte Bedingungen wie Sauerstoffmangel, Säureansammlung, Nährstoffknappheit und Schwankungen in der Gewebesteifigkeit. Unter rauen, sauerstoffarmen Bedingungen verlagern viele Krebszellen ihr Programm zugunsten der Glykolyse. Bei Säureansammlung oder Zuckermangel können sie wieder stärker auf OXPHOS zurückschwenken. Dieselbe Flexibilität zeigt sich bei wichtigen biologischen Stationen: Schnell teilende Zellen stützen sich auf Glykolyse, um Bausteine für DNA, Lipide und Membranen zu liefern. Ruhende oder im Blut zirkulierende Zellen sind oft stärker auf OXPHOS angewiesen. Während Invasion und Metastasierung passen Krebszellen ihre Energiewahl wiederholt an: Manche Schritte begünstigen Glykolyse, andere OXPHOS, und metastatische Zellen, die neue Organe besiedeln, justieren ihren Stoffwechsel so, dass er zum „Boden“ des Zielgewebes passt.
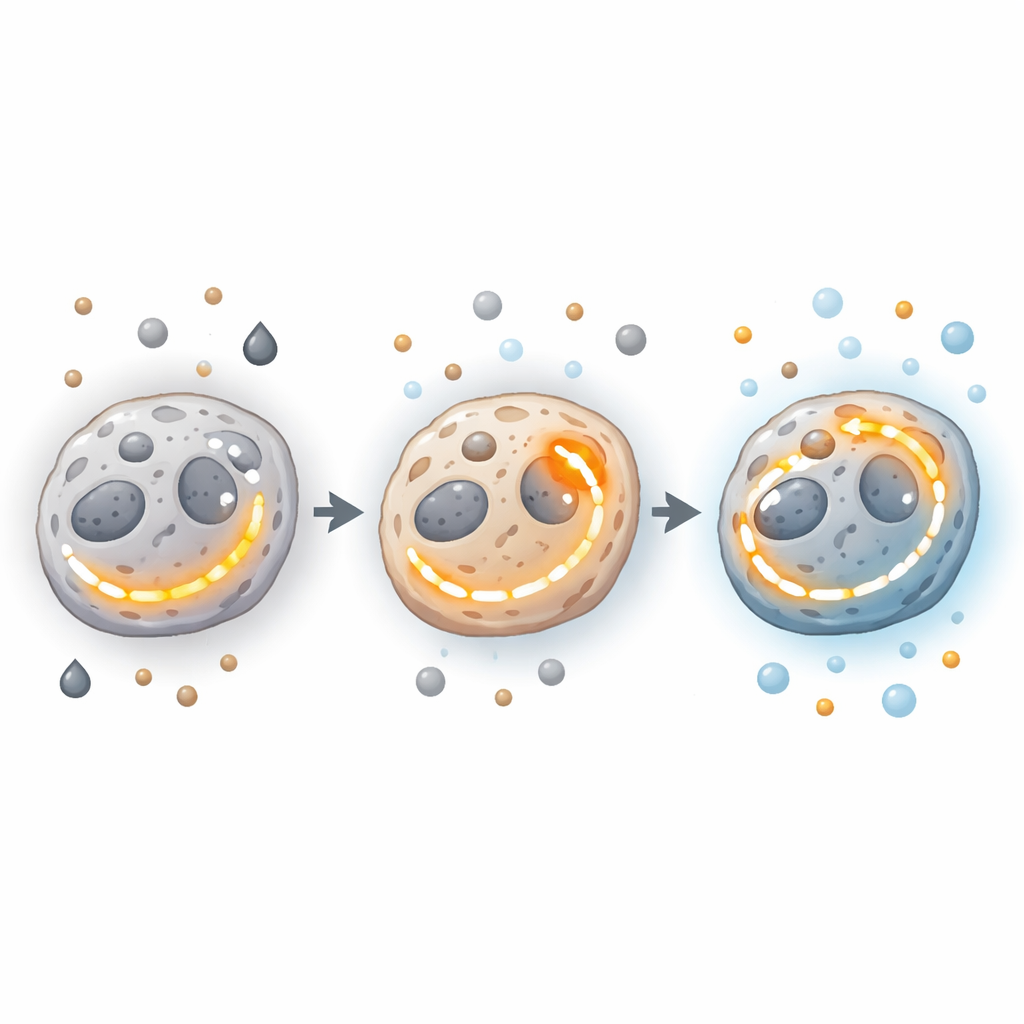
Gene, Enzyme und „Kraftwerke“, die den Wechsel steuern
Tief im zellulären Apparat lenken Gene und Enzyme diese Energieentscheidungen. Onkogene und Tumorsuppressoren können Zellen in Richtung Glykolyse oder OXPHOS drängen oder ihnen ermöglichen, beide Wege hochzufahren. Mutationen oder Änderungen in Schlüsselenzymen des TCA‑Zyklus, etwa solchen, die mit Citrats, Succinat oder Isocitrat umgehen, können das Gleichgewicht verschieben und gelegentlich krebserregende Signale wie Gefäßneubildung und Invasion fördern. Enzyme an entscheidenden Kreuzungen—wie Pyruvatkinase M2, die mitentscheidet, ob kohlenstoff aus Zucker zu Energie oder zu Baumaterial wird—verknüpfen Glykolyse und mitochondriale Funktion. Zugleich erweitern Unterschiede in Anzahl, Struktur und Leistung der Mitochondrien in verschiedenen Tumorregionen das Spektrum möglicher Energiestände weiter.
Therapie neu denken durch ein bewegliches Energie-Ziel
Weil Tumorzellen zwischen Glykolyse und OXPHOS wechseln können, reicht das bloße Blockieren eines Weges häufig nicht aus; der Krebs kann seine Brennstoffnutzung umlenken und überleben. Die Autorinnen und Autoren argumentieren, dass der Energiestoffwechsel von Krebs nur kurzzeitig stabil und prinzipiell konstant im Wandel ist. Sie schlagen vor, Tumoren als ein „Spektrum des Energiestoffwechsels“ zu betrachten, das über die Zeit gemessen werden muss und nicht nur einmal. Praktisch könnte das bedeuten, die Brennstoffpräferenzen eines Tumors in verschiedenen Krankheitsphasen zu verfolgen und Hemmstoffe der Glykolyse und von OXPHOS in maßgeschneiderten Kombinationen zu koppeln. Solche dynamischen, am Stoffwechsel orientierten Behandlungsstrategien könnten die Energiezufuhr des Tumors wirksamer abschneiden, seine Anpassungsfähigkeit begrenzen und die langfristige Kontrolle der Erkrankung verbessern.
Zitation: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Schlüsselwörter: Krebsstoffwechsel, Glykolyse, oxidative Phosphorylierung, tumormikroumgebung, metabolische Plastizität