Clear Sky Science · de
APOA2-vermittelte endotheliale mesenchymale Umstellung und Umprogrammierung des Lipidstoffwechsels von Krebszellen verleihen durch TGF-β Antiangiogenika-Resistenz
Warum diese Entdeckung für Patientinnen und Patienten wichtig ist
Ärztinnen und Ärzte setzen zunehmend Medikamente ein, die Lebertumoren durch das Abschneiden ihrer Blutversorgung aushungern sollen, doch viele Patientinnen und Patienten verlieren nach einem anfänglichen Ansprechen den Nutzen. Diese Studie stellt eine drängende Frage: Warum werden manche Leberkrebserkrankungen gegen diese gefäßblockierenden Behandlungen resistent, und wie könnte man sie überlisten? Die Forschenden decken eine bislang verborgene Zusammenarbeit zwischen einem Blutfett-Protein und einem starken Wachstumssignal auf, die es Tumoren erlaubt, sowohl ihre Blutgefäße als auch ihre Energienutzung umzubauen – und weist so auf einen alternativen Behandlungsweg für eine schwer zu heilende Krebsform hin.
Ein Tumor, der lernt, ohne seine gewohnte Lebensader zu überleben
Das hepatozelluläre Karzinom, die häufigste Form von Leberkrebs, ist stark auf neue Blutgefäße angewiesen, um zu wachsen. Standardmedikamente für fortgeschrittene Erkrankungen zielen darauf ab, einen zentralen Gefäßwachstumspfad zu blockieren, der um VEGF und dessen Rezeptor VEGFR2 organisiert ist. Dennoch gedeihen Tumore bei vielen Patientinnen und Patienten weiter, obwohl diese Mittel gegeben werden. Beim Vergleich von Tumorproben von Patientinnen und Patienten, die auf das Antiangiogenikum Apatinib ansprachen oder nicht, fiel ein Gen besonders auf: APOA2. Tumore aus resistenten Fällen zeigten deutlich höhere APOA2-Spiegel, ein Protein, das vor allem für den Transport von Fetten im Blut bekannt ist. Das deutete darauf hin, dass APOA2 den Tumoren helfen könnte, Gefäßzielgerichte Therapien zu entgehen.
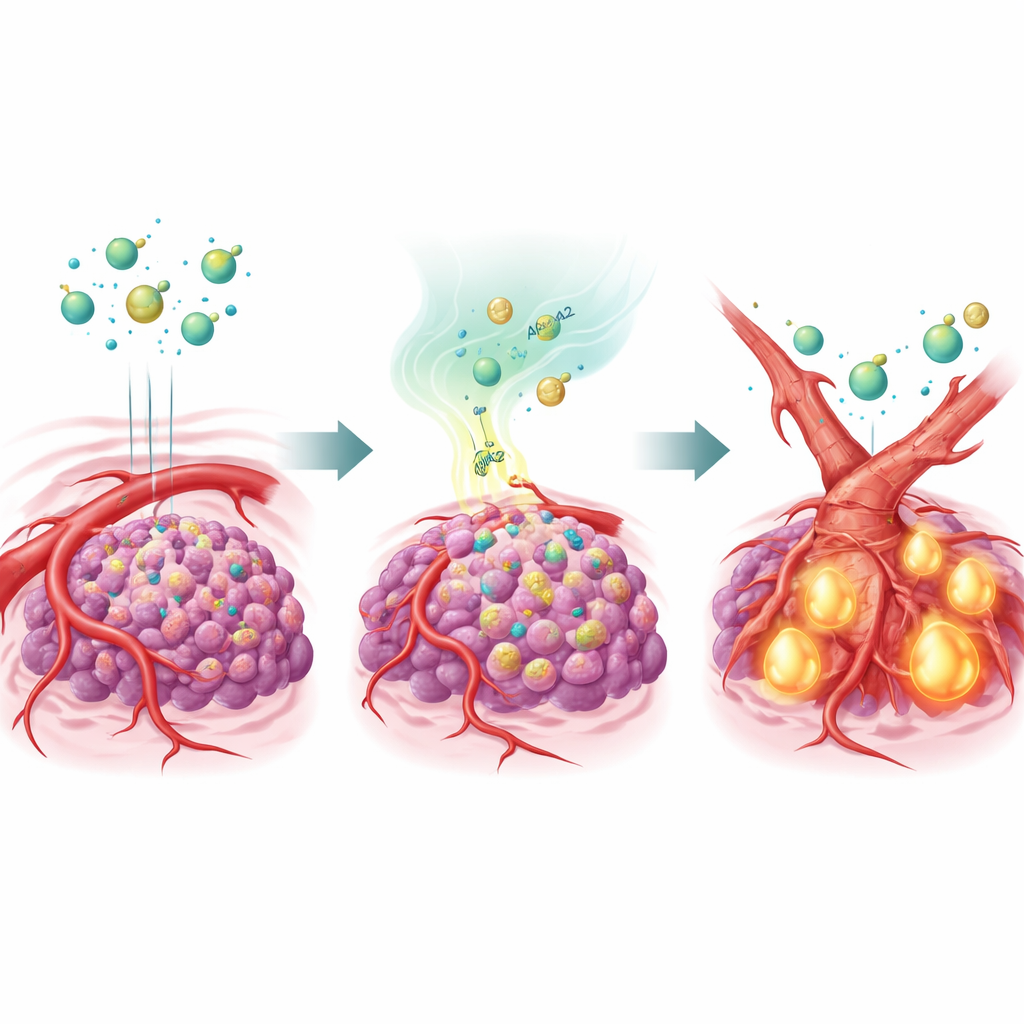
Ein Fetttransportprotein, das Gefäße umgestaltet
Um diese Idee zu testen, erzeugte das Team Leberkrebzellen, die zu viel APOA2 produzierten, und implantierte sie in Mäuse. Unter Behandlung mit verschiedenen Antiangiogenika ignorierten diese APOA2-reichen Tumore die Therapie weitgehend: Ihre Blutgefäße blieben bestehen und die Tumore wuchsen weiter. Detaillierte Analysen zeigten, dass ein Master-Signal namens TGF-β in diesen Tumoren stark aktiviert war und dessen Spiegel sowohl im Tumormilieu als auch im Blut der Tiere erhöht waren. TGF-β wirkte auf die Zellen, die Blutgefäße auskleiden, und trieb sie zu einem Identitätswechsel in einem Prozess namens endothelial-to-mesenchymal transition (EndMT). Während sie in einen narbenähnlicheren, mesenchymalen Zustand übergingen, verloren diese Zellen große Teile ihres VEGFR2 – genau den Ansatzpunkt, den Antiangiogenika anvisieren. Effektiv remodelten sich die Gefäße in eine Form, die die Medikamente nicht mehr anvisieren konnten.
Eine metabolische Umgehung, die Krebszellen weiter mit Energie versorgt
Die Geschichte endete nicht an der Gefäßwand. Dasselbe durch APOA2 getriebene TGF-β-Signal programmierte auch um, wie Krebszellen sich nähren. Anstatt sich hauptsächlich auf den Zuckerabbau zu verlassen, begannen APOA2-hohe Zellen, mehr freie Fettsäuren aus ihrer Umgebung aufzunehmen und diese in den Mitochondrien über die Fettsäureoxidation zu verbrennen. Experimente zur Messung von Nährstoffnutzung und Sauerstoffverbrauch zeigten, dass diese Zellen stärker von Fett als Energiequelle abhängig wurden und mehr zelluläre Energie (ATP) produzierten. Dieser Umbau erlaubte es Tumorzellen, sich weiterhin rasch zu teilen und dem Zelltod zu entgehen, selbst wenn die Blutversorgung durch Antiangiogenese beeinträchtigt war.
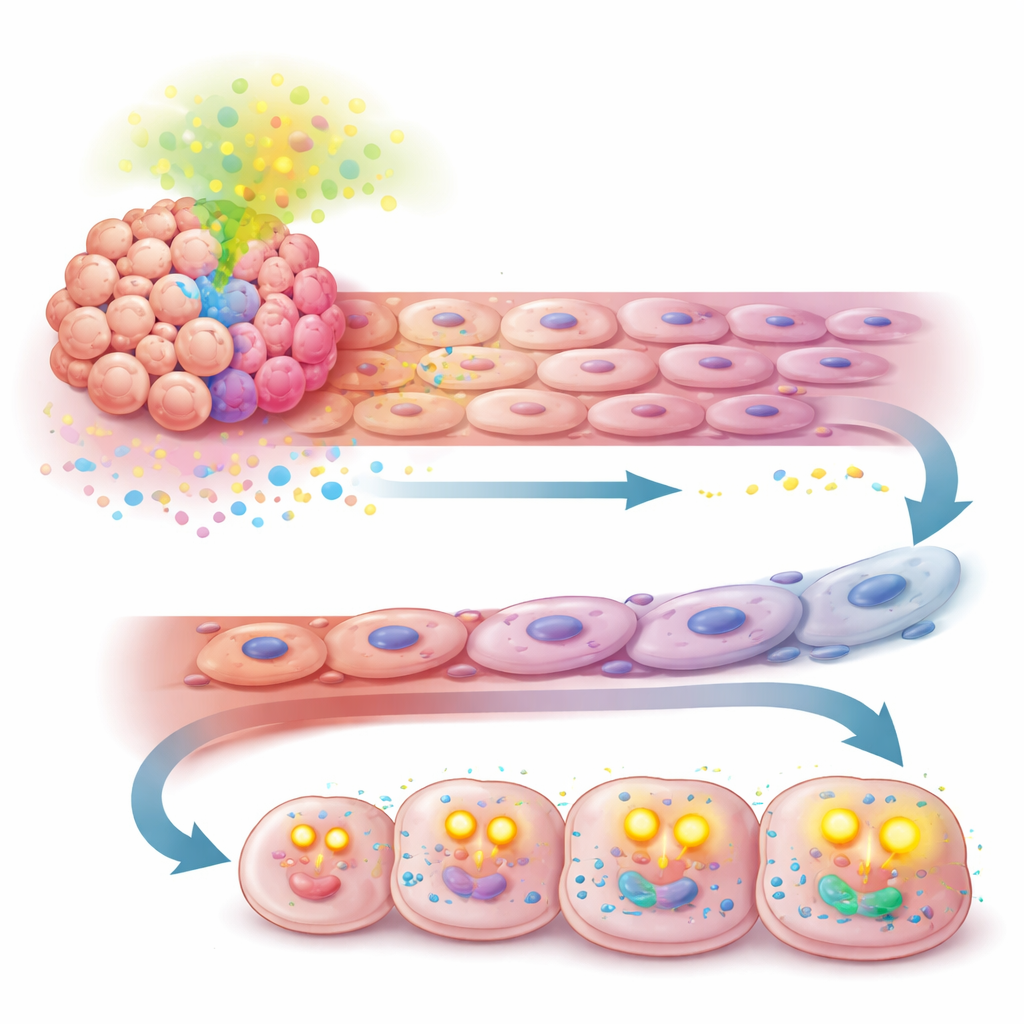
Eine Schwäche in ein neues Therapieziel verwandeln
Entscheidend war: Als die Forschenden TGF-β blockierten, lösten sich die durch APOA2 verliehenen Vorteile auf. Die Hemmung dieses Signals in Mausmodellen reduzierte die abnormalen Gefäßveränderungen, stellte die Empfindlichkeit gegenüber der Therapie wieder her und verlangsamte das Tumorwachstum. Noch vielversprechender wirkte ein dualer Antikörper, der gleichzeitig TGF-β und den Immun-Checkpoint PD-1 blockiert, besser als jede einzelne Intervention allein in APOA2-hohen Tumoren. Diese Ergebnisse legen nahe, dass sich in einem Subtyp von Leberkrebserkrankungen mit hohem APOA2-Spiegel die Abhängigkeit stillschweigend vom üblichen VEGF-Weg auf einen TGF-β-zentrierten Pfad verlagert hat, der sowohl Gefäße als auch Tumormetabolismus stützt.
Was das für die zukünftige Behandlung von Leberkrebs bedeutet
Für Laien lautet die Kernbotschaft: Manche Lebertumore entkommen den derzeitigen gefäßgerichteten Medikamenten, indem sie sowohl ihre „Rohrleitungen“ als auch ihre „Energieversorgung“ umverdrahten. Ein mit Fett assoziiertes Protein, APOA2, kurbelt das TGF-β-Signal an, das wiederum Blutgefäße so maskiert, dass bestehende Medikamente sie nicht mehr erkennen, und Krebszellen beibringt, von Fetten statt von Zucker zu leben. Die Studie legt nahe, Tumore auf APOA2 zu testen, um Patientinnen und Patienten zu identifizieren, die wahrscheinlich nicht von Standard-Antiangiogenika profitieren, aber auf TGF-β-Blocker reagieren könnten, insbesondere in Kombination mit moderner Immuntherapie. Kurz: Indem diese Arbeit zeigt, wie Tumore sich anpassen, weist sie auf eine gezieltere Strategie hin, die sowohl die Gefäße als auch die Energiequelle dieser widerstandsfähigen Tumore angreift.
Zitation: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Schlüsselwörter: hepatozelluläres Karzinom, Resistenz gegen Antiangiogenese, APOA2, TGF-beta-Signalgebung, lipidstoffwechsel von Krebs