Clear Sky Science · de
Irisin hemmt die adipozytäre Differenzierung von Knochenmarksmesenchymalen Stammzellen über die SIRT1/RANBP2/FTO-Signalachse und schützt vor Osteoporose
Warum ein Muskelhormon für brüchige Knochen wichtig ist
Osteoporose wirkt oft wie ein simples Problem von „schwachen Knochen“, doch tief in unserem Skelett findet ein stiller Tauziehen statt. Dieselben Stammzellen im Knochenmark können entweder zu knochenbildenden Zellen oder zu Fettzellen werden. Mit dem Alter, besonders nach den Wechseljahren, verschiebt sich dieses Gleichgewicht zugunsten von Fett, sodass die Knochen dünner und brüchiger werden. Diese Studie untersucht, wie ein von arbeitenden Muskeln freigesetztes Hormon, genannt Irisin, diese Stammzellen zurück in Richtung Knochenbildung lenken kann, was auf eine Zukunft hindeutet, in der ein „Trainingshormon“ zum Schutz vor Osteoporose beitragen könnte.
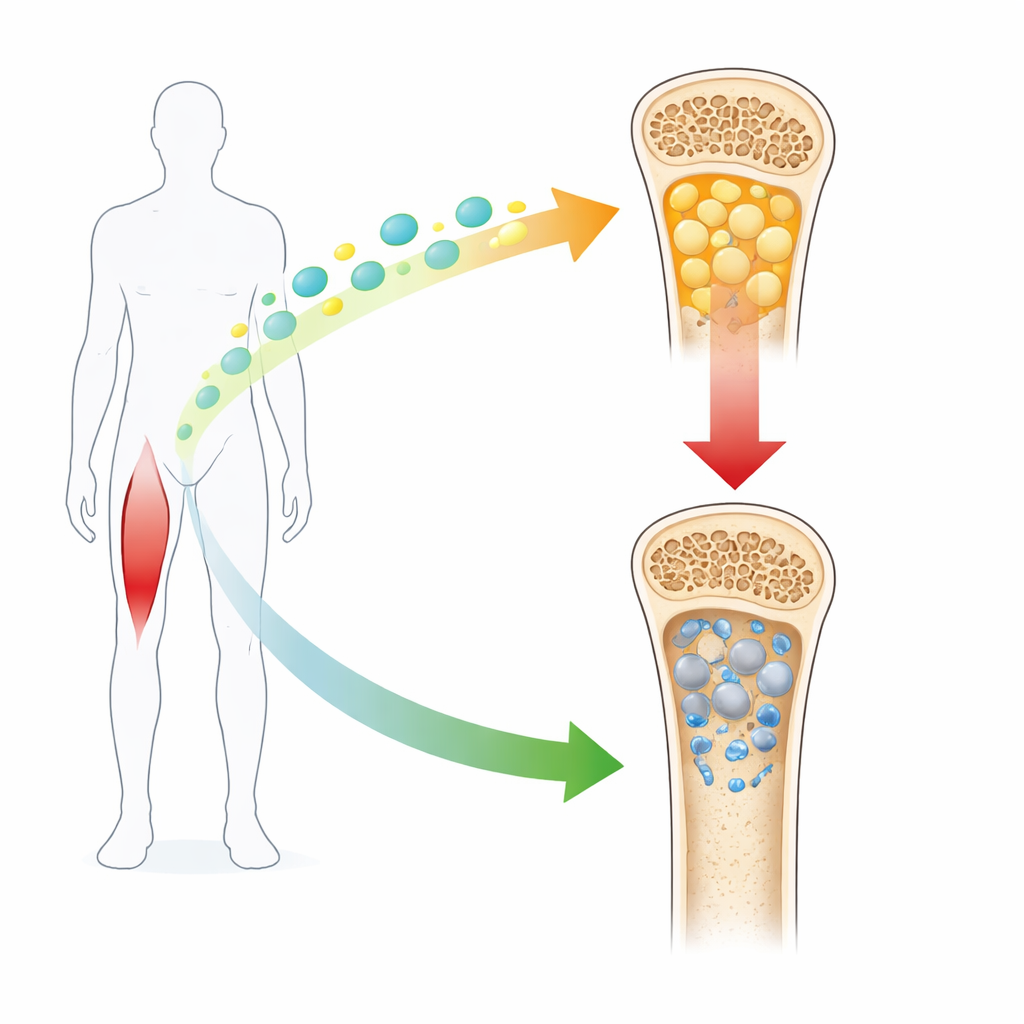
Wenn Knochen zu Fett werden
Das Knochenmark ist nicht nur eine leere Höhlung, sondern eine geschäftige Werkstatt von Stammzellen, die verschiedene Schicksale wählen können. Bei gesunden Erwachsenen werden ausreichend viele dieser Zellen zu knochenbildenden Baumeistern, um das Skelett stark zu halten. Bei Osteoporose, insbesondere bei postmenopausalen Frauen, werden mehr dieser Zellen zu fett-speichernden Zellen. Diese „Knochenmarksfettleibigkeit“ geht einher mit brüchigen Knochen und Frakturen. Die Forschenden begannen damit zu bestätigen, dass diese Verschiebung hin zu Fett mit niedrigeren Irisinspiegeln einhergeht, sowohl bei Mäusen mit Östrogenmangel als auch bei menschlichen Patientinnen mit Osteoporose, und verbinden damit einen Abfall dieses Hormons mit einer Verschlechterung der Knochengesundheit.
Ein trainingsverknüpftes Signal mit doppelter Rolle
Irisin wird von Muskeln während körperlicher Aktivität freigesetzt und wurde auf seine Auswirkungen auf Stoffwechsel und Energieverbrauch untersucht. Hier fragten die Forschenden, ob Irisin auch mitentscheidet, ob Knochenmarkstammzellen zu Fett oder zu Knochen werden. In Zellkulturen gaben sie Irisin zu Maus-Knochenmarkstammzellen und beobachteten die Folgen. Irisin förderte die Fähigkeit der Zellen, zu knochenbildenden Zellen zu werden, erhöhte die Mineralablagerungen und die Aktivität wichtiger Knochen-Gene. Gleichzeitig unterdrückte es stark ihre Umwandlung in Fettzellen, reduzierte Fetttröpfchen und dämpfte Gene und Proteine, die die Fettbildung antreiben. In lebenden Mäusen, denen die Eierstöcke entfernt worden waren, um postmenopausalen Knochenverlust zu simulieren, bewahrten wöchentliche Irisin-Injektionen die Knochenmasse und Mikrostruktur und verringerten die Ansammlung von Fett im Markraum.
Im Inneren der zellulären Entscheidungsmechanik
Um zu verstehen, wie Irisin diese Kontrolle ausübt, untersuchten die Forschenden Änderungen in der Genaktivität, als Stammzellen während der Fettbildung Irisin ausgesetzt wurden. Ein herausragender Akteur war SIRT1, ein Protein, das für die Regulierung von Altern, Stoffwechsel und Stressantworten bekannt ist. Das Team zeigte, dass eine Herunterregulierung von SIRT1 die Zellen eher dazu brachte, zu Fett zu werden, während eine Verstärkung von SIRT1 den gegenteiligen Effekt hatte. Wichtig ist, dass, wenn SIRT1 reduziert wurde, Irisin die Fettbildung weder in Zellen noch in Mäusen effektiv blockieren konnte, was zeigt, dass SIRT1 eine Schlüsselstelle in Irisins knochenschützendem Signal ist.
Eine molekulare Kette, die ein „Fett“-Protein entwaffnet
Bei tieferer Betrachtung konzentrierte sich die Studie auf ein weiteres Protein, FTO, das mit Adipositas und Fettspeicherung in Verbindung gebracht wurde. Hohe FTO-Spiegel fördern die Entwicklung von Fettzellen, teilweise indem sie einen master-Regulator des Fettgewebes namens PPARγ stabilisieren. Die Forschenden fanden heraus, dass SIRT1 nicht die Genproduktion von FTO veränderte, sondern die Stabilität des FTO-Proteins beeinflusste. Durch Irisin aktiviertes SIRT1 erhöhte die Aktivität eines dritten Proteins, RANBP2, das FTO auf eine Weise markiert, die es zum Abbau freigibt. Wenn RANBP2 reduziert wurde, konnte SIRT1 die FTO-Proteinspiegel nicht länger senken und die Fettbildung kehrte zurück. Durch diese Kette — Irisin zu SIRT1, SIRT1 zu RANBP2 und RANBP2 zur FTO-Degradation — wandten die Zellen sich von der Differenzierung zu Fettzellen ab und hin zu knochenbildenden Aufgaben.
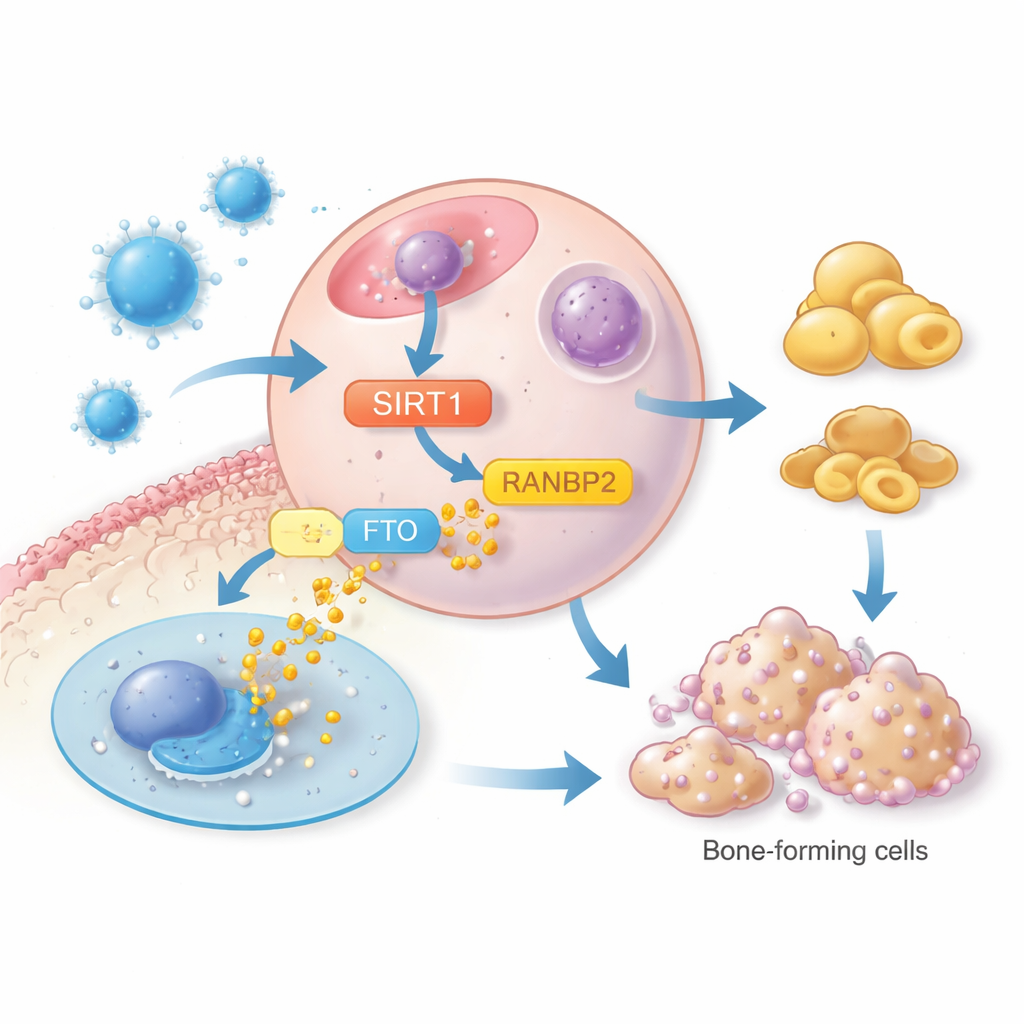
Was das für die zukünftige Knochenpflege bedeuten könnte
Indem die Studie diesen schrittweisen Signalweg nachzeichnet, zeigt sie Irisin als mehr als nur ein einfaches Trainingshormon. Es wirkt wie ein molekularer Verkehrsregler im Knochenmark und lenkt Stammzellen von der Fettbildung weg und hin zur Knochenbildung, über eine SIRT1–RANBP2–FTO-Signalachse. Für Laien bedeutet das, dass die Aufrechterhaltung oder das Nachahmen des natürlichen Irisin-Signals des Körpers eines Tages eine Strategie zur Vorbeugung oder Behandlung von Osteoporose werden könnte, ergänzend zu Lebensstilmaßnahmen wie Bewegung. Obwohl weitere Untersuchungen in größeren Humanstudien nötig sind, deuten die Erkenntnisse auf eine vielversprechende neue Reihe molekularer Ziele hin, um Knochen länger stärker zu halten.
Zitation: Chen, J., Liu, J., Fu, Q. et al. Irisin inhibits adipogenic differentiation of bone marrow mesenchymal stem cells through the SIRT1/RANBP2/FTO signaling axis and protects against osteoporosis. Cell Death Discov. 12, 114 (2026). https://doi.org/10.1038/s41420-026-02976-5
Schlüsselwörter: Osteoporose, Irisin, Knochenmarkstammzellen, Gleichgewicht von Knochen und Fett, SIRT1-Signalgebung