Clear Sky Science · de
KCTD1 stabilisiert c-Myc, um PD-L1 hochzuregulieren und die antitumorale Immunität beim hepatozellulären Karzinom zu unterdrücken
Warum das für die künftige Krebsbehandlung wichtig ist
Viele Menschen mit Leberkrebs profitieren nicht von den derzeit vielversprechendsten Immuntherapien, die darauf abzielen, die körpereigenen T-Zellen gegen Tumoren zu mobilisieren. Diese Studie untersucht, warum eine häufige Form von Leberkrebs, das hepatozelluläre Karzinom, sich trotz Behandlung der Immunangriffe entziehen kann — und identifiziert einen neuen molekularen Schalter namens KCTD1, der bestehende Immuntherapien wirksamer machen könnte.
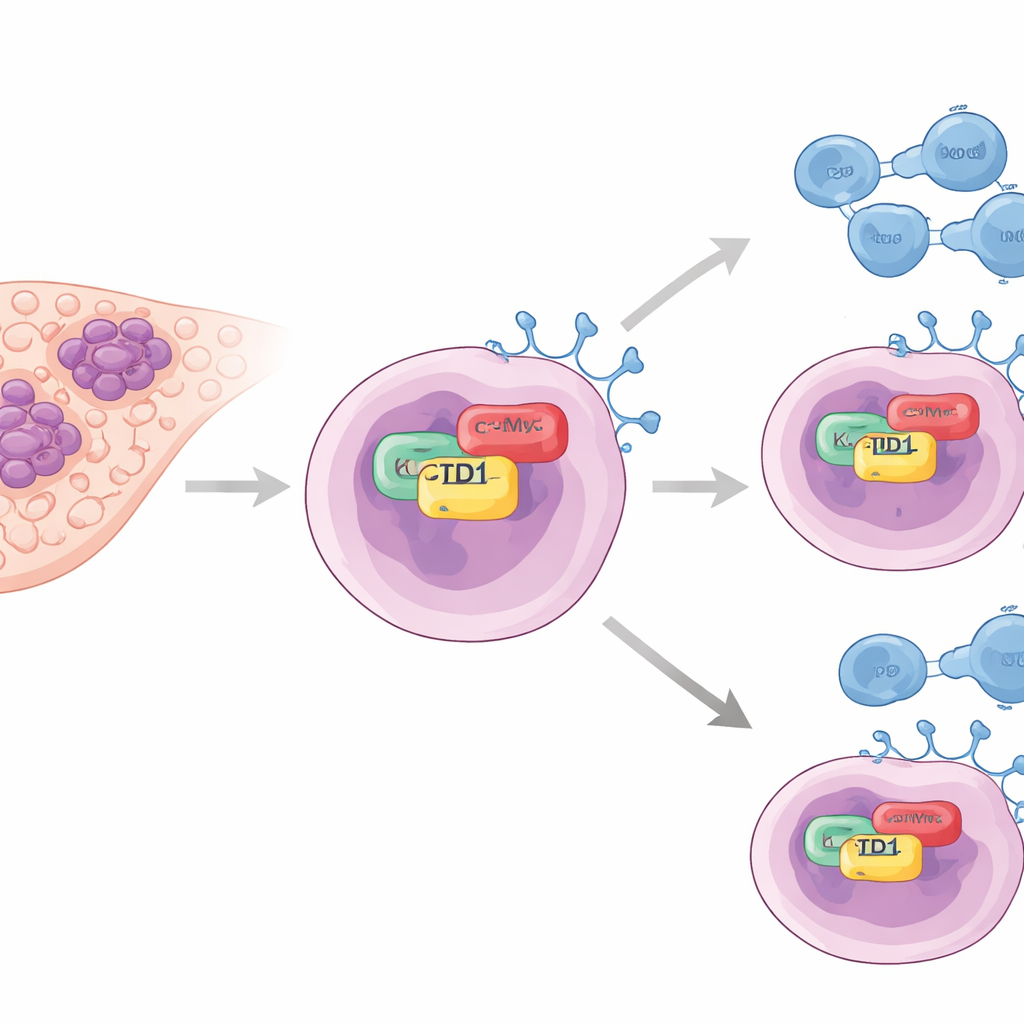
Ein versteckter Helfer der Tumor‑„Ausschalter“
Die Autoren konzentrierten sich auf ein Protein namens KCTD1, das zuvor mit dem Wachstum von Lebertumoren in Verbindung gebracht worden war, aber in Bezug auf die Immunflucht wenig untersucht ist. In Tumorproben von Patientinnen und Patienten fanden sie, dass die KCTD1-Spiegel im Krebsgewebe deutlich höher waren als in normaler Leber. Wichtig ist, dass Tumoren mit hohem KCTD1 auch hohe PD-L1-Level aufwiesen — ein Oberflächenprotein von Krebszellen, das an PD-1 auf T-Zellen bindet und dem Immunsystem effektiv signalisiert, sich zurückzuhalten. Patientinnen und Patienten, deren Tumoren geringere KCTD1-Werte hatten, lebten tendenziell länger, was darauf hindeutet, dass dieses Protein sowohl mit dem Schweregrad der Erkrankung als auch mit der Stärke des tumorigenen Immunschutzes verknüpft ist.
Die molekularen Verbindungen innerhalb der Krebszellen
Um zu verstehen, wie KCTD1 PD-L1 fördert, arbeiteten die Forschenden mit im Labor gezüchteten Leberkrebszelllinien. Würden sie KCTD1 vermindern, sanken die PD-L1-Proteinmengen und das verbleibende PD-L1 wurde schneller abgebaut — ein Hinweis darauf, dass KCTD1 PD-L1 stabilisiert, statt bloß dessen Gen an- zu schalten. Mit biochemischen Pull‑down‑Experimenten und Fluoreszenzmicroskopie zeigten sie, dass KCTD1 physisch an einen weiteren wichtigen Krebsantreiber, das Onkoprotein c‑Myc, im Zellkern bindet. Diese Interaktion erfolgt über spezifische Kontaktbereiche beider Proteine und führt zu einem stabileren c‑Myc, das wiederum die PD-L1‑Produktion verstärkt. Wurde c‑Myc allein reduziert, fiel PD-L1, selbst wenn KCTD1 reichlich vorhanden war — was c‑Myc als entscheidende mittlere Verbindung in einer KCTD1–c‑Myc–PD-L1‑Kette positioniert.
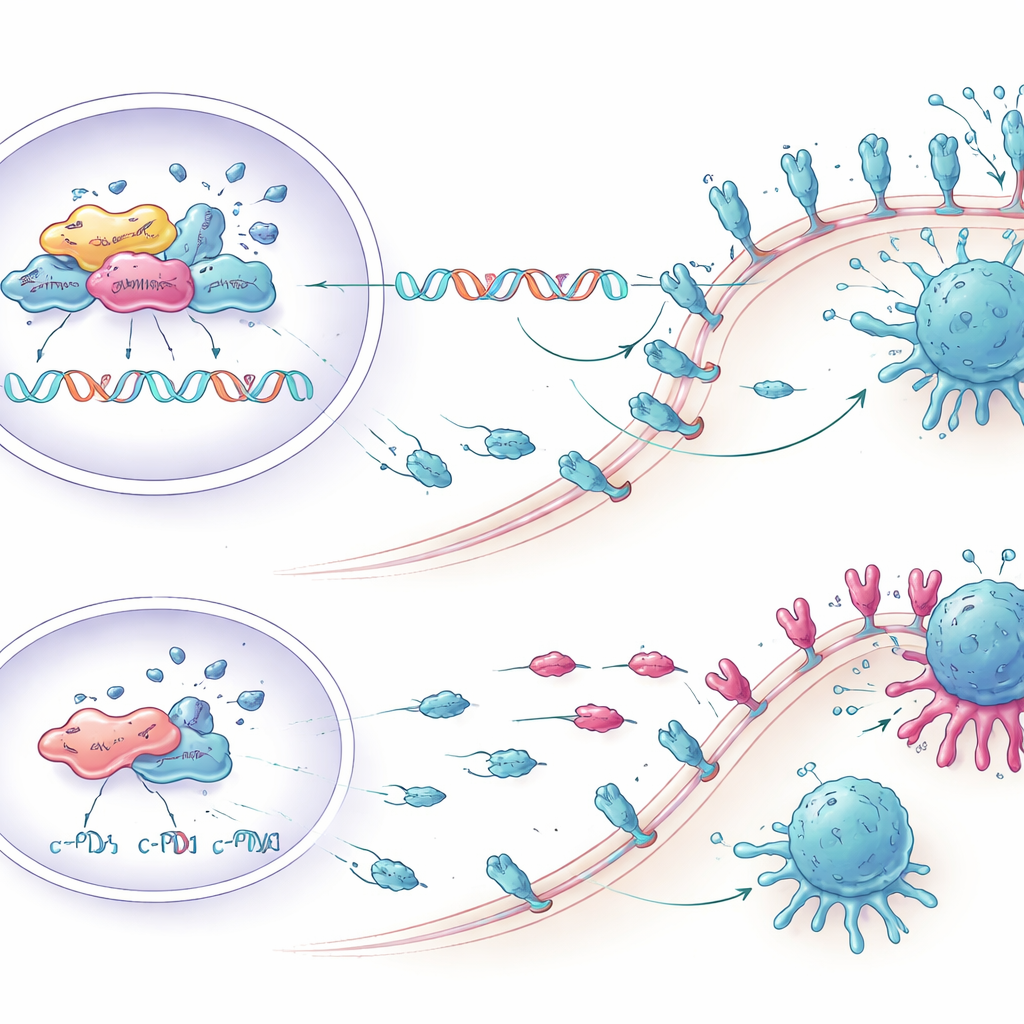
T‑Zellen im Labor wieder wecken
Die Forschenden fragten dann, ob die Senkung von KCTD1 tatsächlich die Immunantwort stärken könne. Sie kultivierten menschliche Leberkrebszellen zusammen mit Immunzellen aus Blutspendern. Tumorzellen, bei denen KCTD1 reduziert und damit PD-L1 verringert war, riefen stärkere Reaktionen von CD8‑T‑Zellen hervor — den wichtigsten Zerstörern von Krebszellen im Immunsystem. Mehr dieser T‑Zellen produzierten entzündliche Moleküle wie TNF‑α und Interferon‑gamma, zeigten höhere Wachstums‑ und Aktivierungsmarker und wiesen weniger Erschöpfungszeichen auf. Folglich durchliefen mehr Tumorzellen den programmierten Zelltod, wenn KCTD1 unterdrückt war, was beweist, dass die molekularen Veränderungen in realen Zuwächsen an immunvermittelter Tumorzellvernichtung mündeten.
Den Mechanismus im Tiermodell geprüft
Um zu prüfen, ob das Muster auch in lebenden Organismen gilt, setzten die Forschenden Mäusen Leberkrebszellen ohne KCTD1 direkt in die Leber. Tumoren mit reduziertem KCTD1 bildeten weniger und kleinere Knoten, zeigten langsamere Zellteilung und mehr Tumorzellen in programmierter Zellauflösung. Diese Tumoren exprimierten außerdem weniger c‑Myc und PD‑L1. Die Entfernung von CD8‑T‑Zellen aus den Mäusen beseitigte einen großen Teil dieses Vorteils, was darauf hindeutet, dass die Tumorverlangsamung stark von T‑Zell‑Aktivität abhängig war. Schließlich führten KCTD1‑Knockdown kombiniert mit einem Anti‑PD‑1‑Antikörper — einem bereits existierenden Checkpoint‑Inhibitor — bei den Mäusen zur geringsten Tumorlast und zu den höchsten Infiltrationsraten von CD4‑ und CD8‑T‑Zellen in den Tumoren.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt zeigt die Arbeit, dass KCTD1 als zentraler Koordinator fungiert, der c‑Myc stabilisiert, PD‑L1 auf Leberkrebszellen erhöht und den Angriff von CD8‑T‑Zellen abschwächt. Die Störung dieses Weges macht Tumoren sowohl verwundbarer für das Immunsystem als auch in Mäusen empfänglicher für PD‑1‑blockierende Therapien. Für Patientinnen und Patienten deutet dies darauf hin, dass Wirkstoffe, die auf KCTD1 oder seine Kontaktfläche mit c‑Myc abzielen, künftig in Kombination mit bestehenden Immuntherapien eingesetzt werden könnten, um mehr Menschen mit Leberkrebs von einer dauerhaften immunologischen Kontrolle ihrer Erkrankung profitieren zu lassen.
Zitation: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Schlüsselwörter: hepatozelluläres Karzinom, Tumorimmuntherapie, PD-1/PD-L1-Signalweg, c-Myc-Signaling, T-Zell-Antitumor-Immunität