Clear Sky Science · de
Molekulare Einblicke in die krebshemmenden Effekte von Silodosin: eine vielversprechende Umwidmungsstrategie für Brustkrebs
Warum ein altes Medikament neue Aufmerksamkeit erhält
Brustkrebs bleibt eine der häufigsten und tödlichsten Krebserkrankungen bei Frauen, und viele Patientinnen laufen schließlich die wirksamen Behandlungsoptionen aus. Diese Studie untersucht, ob Silodosin, eine Pille, die bereits sicher zur Behandlung von Harnproblemen bei Männern eingesetzt wird, für die Bekämpfung von Brustkrebs umgewidmet werden könnte. Da es sich um ein zugelassenes, preisgünstiges Medikament mit bekannter Sicherheitsbilanz handelt, könnte der Nachweis, dass es das Wachstum von Brustkrebszellen verlangsamt oder sie abtötet, den Weg zu neuen Therapien beschleunigen — besonders für Patientinnen mit aggressiver Erkrankung.
Ein vertrautes Medikament in neuer Rolle
Silodosin wird derzeit verschrieben, um Harnsymptome zu lindern, die durch eine vergrößerte Prostata verursacht werden, indem es bestimmte Nervensignale blockiert, sogenannte adrenerge Signale. Diese Signale steuern nicht nur Muskeln; zunehmend deutende Hinweise legen nahe, dass sie auch Tumoren beim Wachsen, Ausbreiten und bei der Bildung neuer Blutgefäße helfen können. Die Autorinnen und Autoren fragten sich, ob Silodosin diese schädlichen Signale auch in Brustkrebszellen stören könnte. Sie testeten das Medikament an mehreren humanen Brustkrebszelllinien, die im Labor gezüchtet wurden und sowohl hormonempfindliche Tumoren als auch schwer zu behandelnde triple-negative Tumoren repräsentieren, und verglichen die Effekte mit denen an gesunden Brustzellen.
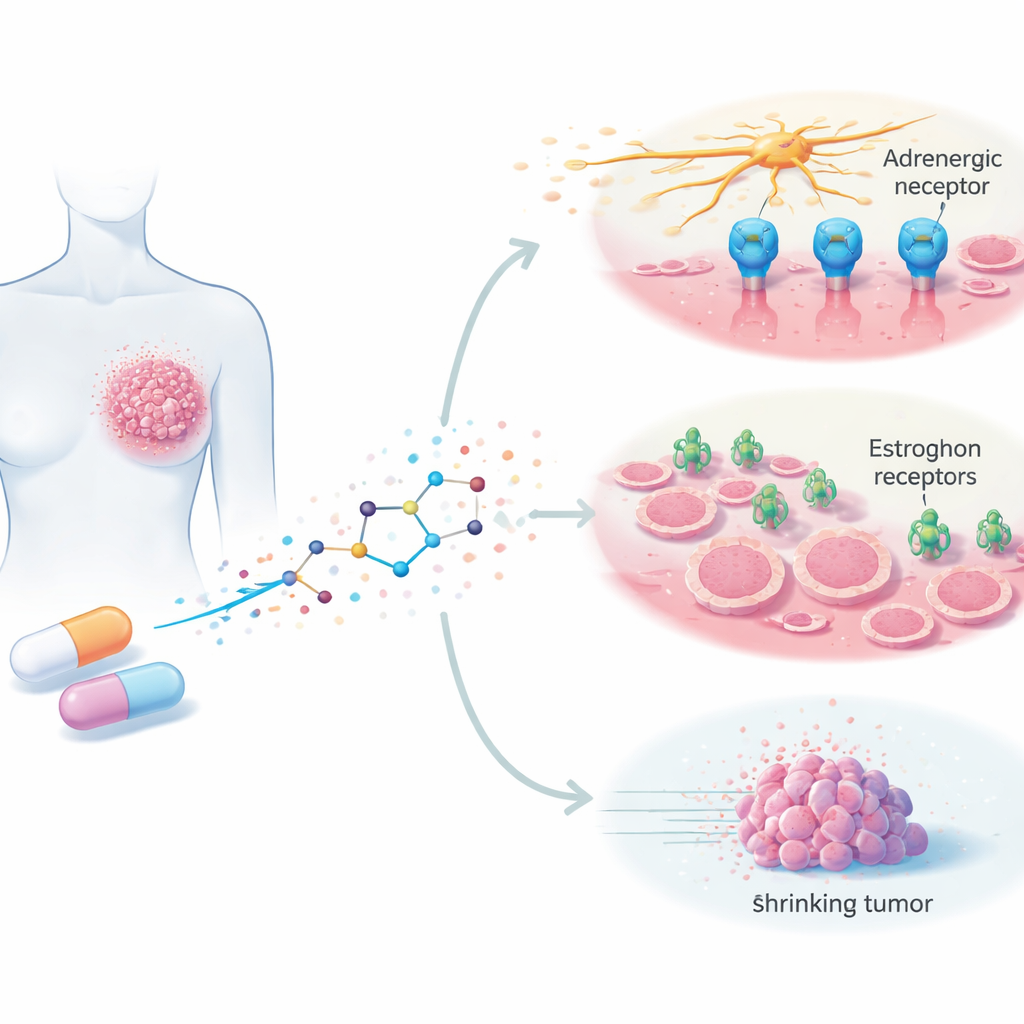
Wachstumsverlangsamung und Auslösung von Zelltod
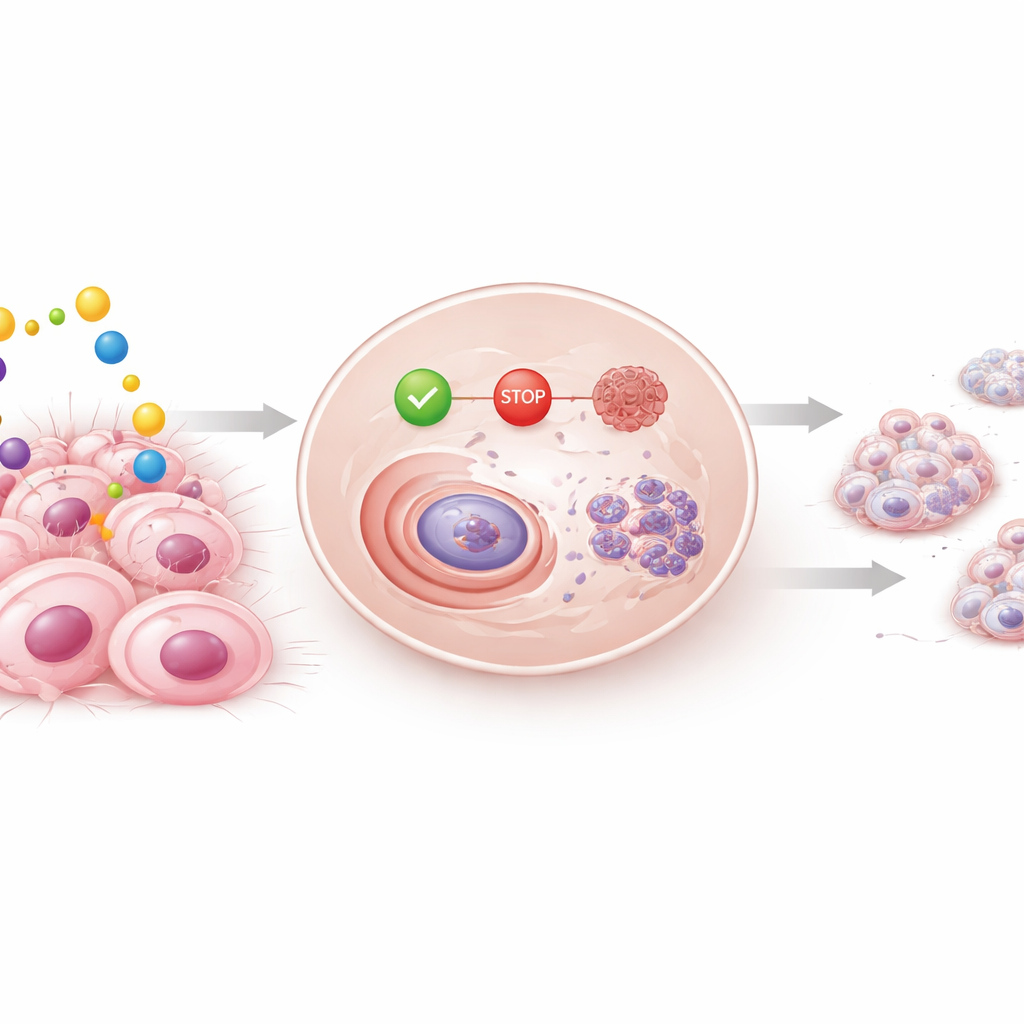
Wurden Brustkrebszellen Silodosin ausgesetzt, verlangsamte sich ihr Wachstum zeit- und dosisabhängig. Besonders betroffen waren hormonempfindliche Zellen, doch auch aggressive triple-negative Zellen zeigten eine verringerte Überlebensfähigkeit und reduzierte Fähigkeit, Kolonien zu bilden, während normale Brustzellen weitgehend geschont blieben. Weitere Experimente enthüllten die inneren Vorgänge: Silodosin brachte die Zellen in einer frühen Phase des Zellzyklus zum Stillstand, der Abfolge von Schritten, die Zellen zur Teilung durchlaufen müssen. Wichtige "Start"-Proteine, die die Zellteilung vorantreiben, nahmen ab, während "Stopp"-Proteine und das bekannte Wächterprotein p53 zunahmen. Das Medikament trieb die Krebszellen außerdem in den programmierten Zelltod, erkennbar an einer zunehmenden Zahl von Zellen mit fragmentierter DNA.
Blockade von Bewegung und 3D-tumorähnlichem Wachstum
Krebs wird lebensbedrohlich, wenn Zellen migrieren und an anderen Stellen neue Tumoren bilden. Mittels eines kratzähnlichen Versuchs in einer Zellschicht fanden die Forschenden heraus, dass Silodosin die Geschwindigkeit verlangsamte, mit der sich sowohl hormonempfindliche als auch triple-negative Brustkrebszellen in die Lücke bewegten. Das Team nutzte außerdem dreidimensionale Sphäroide, winzige kugelförmige Zellverbände, die reale Tumoren besser nachahmen als flache Zellschichten. Silodosin reduzierte deutlich die Bildung und Größe dieser Sphäroide. Zugleich senkte es die Spiegel von E‑Cadherin, einem Molekül, das Zellen zusammenhält und ebenfalls an Wachstums- und Überlebenssignalen beteiligt ist, was darauf hindeutet, dass die Störung von Zell‑Zell-Kontakten ein Weg sein könnte, auf dem das Medikament die Tumororganisation und -ausbreitung beeinträchtigt.
Ein überraschendes zweites Ziel innerhalb der Krebszellen
Silodosin wurde entwickelt, um adrenerge Rezeptoren zu blockieren, doch die Daten passten nicht zu einer einfachen "nur ein Ziel"-Erklärung. Einige Brustkrebszellen, die stark auf das Medikament reagierten, wiesen wenig bis keine nachweisbaren adrenergen Rezeptoren des Typs auf, auf den Silodosin abzielt, und Zellen mit mehr von diesem Rezeptor waren nicht immer empfindlicher. Um nach anderen Zielen zu suchen, verwendeten die Autorinnen und Autoren Computermodelle, um zu prüfen, ob Silodosin auch in Östrogenrezeptoren passen könnte, die molekularen Schalter, die viele Brustkrebserkrankungen antreiben und Hauptziele von Medikamenten wie Tamoxifen sind. Ihre Simulationen zeigten, dass Silodosin an beide Hauptformen des Östrogenrezeptors mit relevanter Affinität binden kann und dabei mit denselben Schlüsselkontaktstellen interagiert wie Tamoxifen. Das deutet darauf hin, dass Silodosin zusätzlich zur Blockade nervenbezogener Signale als Modulator der Östrogenrezeptoren wirken könnte.
Was das für Patientinnen bedeuten könnte
In der Summe deuten die Experimente darauf hin, dass Silodosin als vielseitiger Angreifer von Brustkrebszellen wirkt: Es verlangsamt ihr Wachstum, treibt sie in den Selbstzerstörungsmodus, hemmt ihre Bewegung und verhindert, dass sie sich zu tumorähnlichen Sphäroiden organisieren, während es vermutlich sowohl adrenerge als auch östrogengetriebene Signalwege beeinflusst. Die in Zellkulturen wirksamen Dosen liegen über denen, die Patientinnen bei den üblichen urologischen Dosierungen erreichen, weshalb weitere Tierversuche und Kombinationstherapien nötig sind, um das Potenzial in der Praxis zu beurteilen. Da Silodosin jedoch bereits zugelassen und insgesamt gut verträglich ist, legt diese Studie das Fundament für seine Umwidmung als Teil neuer Therapieansätze, insbesondere für Patientinnen mit wenigen Optionen, wie etwa diejenigen mit triple-negativem Brustkrebs.
Zitation: Pellegrino, M., Occhiuzzi, M.A., Marra, M. et al. Molecular insights into Silodosin’s anti-cancer effects: a promising repurposing strategy for breast cancer. Cell Death Discov. 12, 128 (2026). https://doi.org/10.1038/s41420-026-02973-8
Schlüsselwörter: Brustkrebs, Arzneimittelumwidmung, Silodosin, Östrogenrezeptor, triple-negativer Brustkrebs