Clear Sky Science · de
Die schützende Hochregulierung von Metallothionein-2A bei Bandscheibendegeneration hemmt Ferroptose von Nukleus-pulposus-Zellen durch Aktivierung des PI3K/AKT/mTOR-Signalwegs
Warum dieses Rückenproblem wichtig ist
Rückenschmerzen betreffen weltweit Hunderte Millionen Menschen und sind eine der Hauptursachen für Behinderungen. Ein wesentlicher Auslöser ist der langsame Abbau der Puffer zwischen den Wirbelknochen, den sogenannten Bandscheiben. Diese Studie stellt eine hoffnungsvolle Frage: Können körpereigene Schutzmoleküle diese Scheiben vor Schäden bewahren, und könnte ihre Stärkung auf neue Behandlungsoptionen für chronische Rückenschmerzen hinweisen? 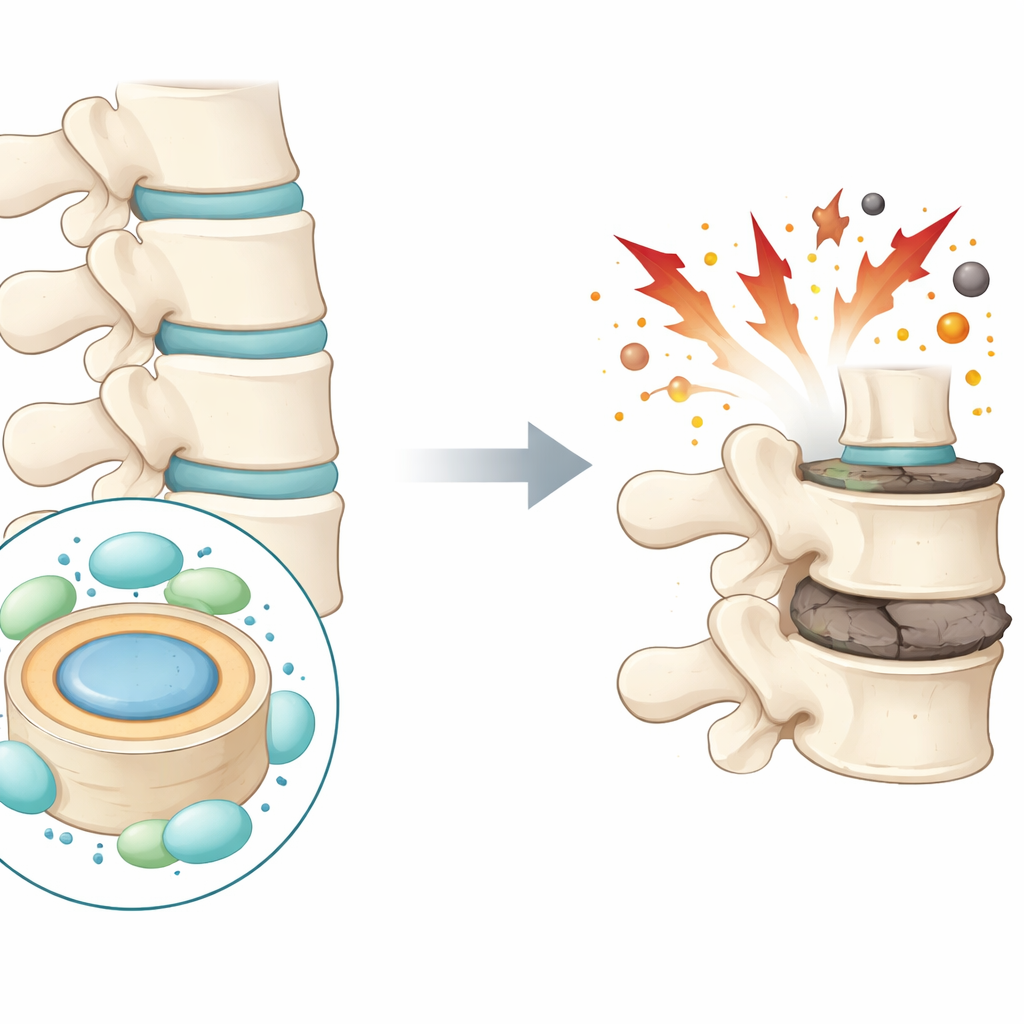
Die Polster innerhalb der Wirbelsäule
Jede Bandscheibe hat einen weichen, gelartigen Kern, den Nukleus pulposus, umgeben von einem zäheren Ring. Diese Strukturen wirken wie Stoßdämpfer der Wirbelsäule. Wenn Bandscheiben degenerieren, sterben die Zellen im zentralen Bereich ab und die stützende Matrix aus Proteinen und Wasser nutzt sich ab. Die Scheibe flacht ab und reißt, was zu Schmerzen und eingeschränkter Beweglichkeit führen kann. Die Autorinnen und Autoren konzentrieren sich auf eine spezifische Form des Zelltods, die erst jüngst in vielen Erkrankungen Beachtung gefunden hat: eisengetriebener, oxidationsbedingter Zelltod, bekannt als Ferroptose. Sie vermuten, dass dieser Prozess eine Schlüsselrolle beim Abbau der Bandscheibe spielt.
Wenn Eisen und Oxidation schiefgehen
Ferroptose wird ausgelöst, wenn freies Eisen und reaktive Sauerstoffmoleküle in Zellen akkumulieren und Lipide in Zellmembranen sowie besonders die kleinen Energiefabriken, die Mitochondrien, schädigen. Das Team analysierte Einzelzell-Genexpressionsdaten aus menschlichem Bandscheibengewebe und fand eindeutige Hinweise darauf, dass ferroptosebezogene Gene in degenerierenden Scheiben verändert sind. Insbesondere waren Marker, die Zellen normalerweise vor dieser Art von Schaden schützen — etwa das Enzym GPX4 — in abgenutzten Scheiben von Patienten und Ratten reduziert. Gleichzeitig stiegen Marker, die Schäden und Entzündungen fördern, sodass das Bild von Zellen unter oxidativem Angriff während der Degeneration entsteht.
Ein eingebauter Metall-bindender Schutz
Unter den vielen Genen, die sich in erkrankten Scheiben veränderten, stach eines hervor: Metallothionein‑2A (MT2A), ein kleines Protein, das Metalle wie Zink bindet und schädliche reaktive Moleküle binden kann. MT2A-Spiegel waren in stärker degenerierten menschlichen Scheiben und in einem Rattenmodell der Bandscheibenverletzung auffällig erhöht. Auf den ersten Blick erscheint das paradox — warum sollte ein schützendes Molekül in geschädigtem Gewebe ansteigen? Die Forschenden vermuteten, dass der Körper eine kompensatorische Antwort startet, um dem Anstieg des eisengetriebenen Stresses entgegenzuwirken. In Zellkulturen stiegen MT2A-Spiegel, wenn Bandscheibenzellen einer Chemikalie ausgesetzt wurden, die oxidativen Stress nachahmt, parallel zum Abfall der Zellgesundheit, was die Idee stützt, dass MT2A als Abwehrreaktion hochreguliert wird.
Schutz herunter- und hochfahren
Um zu prüfen, ob MT2A tatsächlich schützend und nicht schädlich ist, regulierte das Team dessen Spiegel in menschlichen Bandscheibenzellen gezielt herunter oder herauf. Wurde die MT2A-Produktion blockiert, führte oxidativer Stress zu deutlich mehr Zelltod, stärkerer Eisenansammlung, ausgeprägteren Lipidschäden und schwer geschädigten Mitochondrien. Wurde MT2A hingegen gesteigert oder die Zellen mit einem bekannten Ferroptose-Blocker behandelt, wurden viele dieser Probleme gemildert: Eisen und reaktive Moleküle nahmen ab, schützende Antioxidantien erholten sich und die Mitochondrien wirkten gesünder. Diese Veränderungen spiegelten sich auch in einer besseren Erhaltung der stützenden Matrixproteine wider, die entscheidend dafür sind, dass Bandscheiben prall und funktional bleiben. 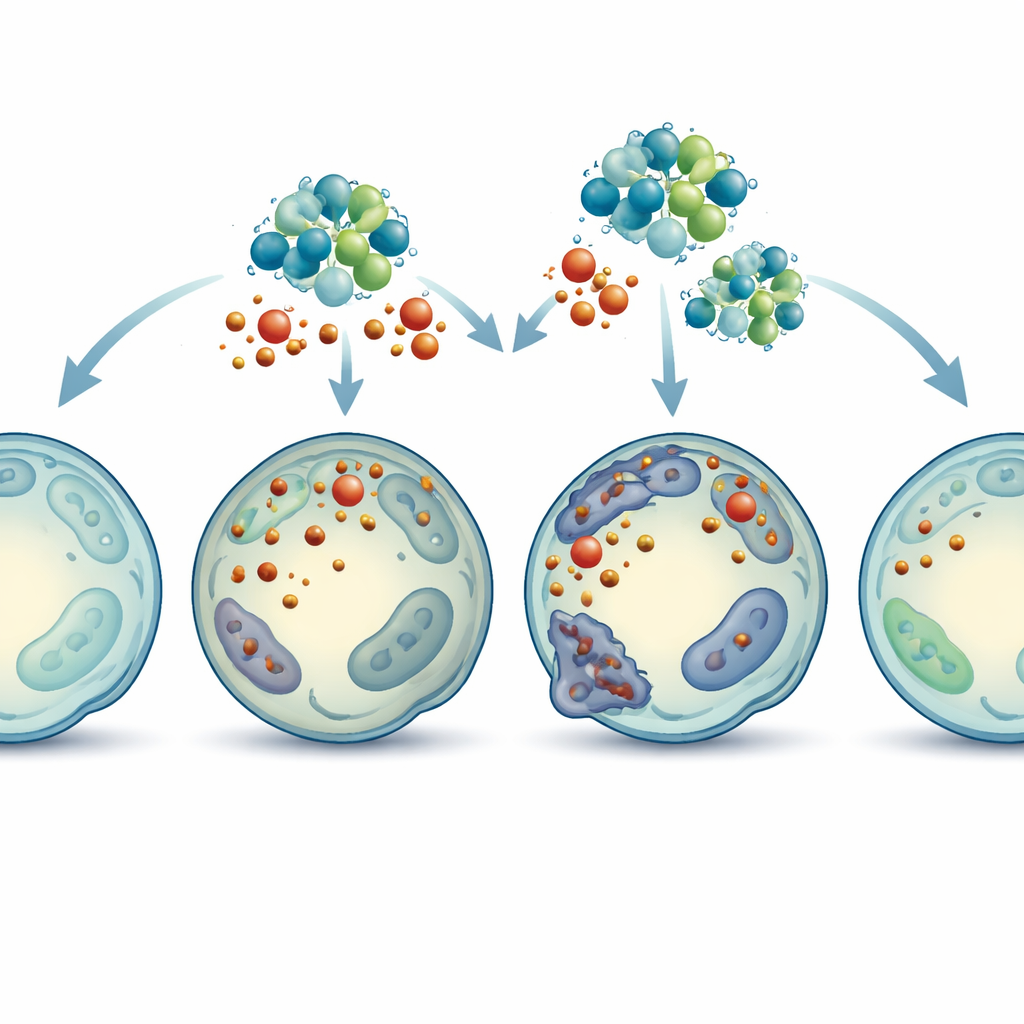
Ein zentraler Signalweg innerhalb der Zelle
Bei tieferer Untersuchung betrachteten die Forschenden, wie MT2A schützende Signale in Zellen vermittelt. Gen-Sequenzierung und Proteinmessungen deuteten auf den PI3K/AKT/mTOR-Signalweg hin, ein bekanntes internes Kontrollsystem, das Wachstum, Stoffwechsel und Überleben beeinflusst. Eine Verringerung von MT2A dämpfte die Aktivität dieses Weges, während eine Erhöhung MT2A aktivierte. Blockierten die Forschenden mit Medikamenten verschiedene Schritte dieses Signalwegs, verschwanden die Vorteile einer MT2A-Überexpression: Ferroptose-Marker stiegen wieder, oxidative Schäden kehrten zurück und Bandscheibenzellen verloren mehr ihrer Strukturproteine. Das legt nahe, dass MT2A die Zellen hauptsächlich schützt, indem es diesen pro‑überlebensfördernden Signalweg aktiviert, der wiederum die Ferroptose bremst.
Machbarkeitsnachweis im Tiermodell
Abschließend prüfte das Team, ob die Hochregulierung von MT2A tatsächlich die Degeneration der Bandscheibe in einem lebenden Organismus verlangsamen kann. Bei Ratten erzeugten sie eine Bandscheibenverletzung durch Nadelstich und injizierten anschließend ein Virus, das MT2A im Inneren der Scheibe erhöhte. Wochen später zeigten Bildgebung und Gewebeanalyse, dass Scheiben mit zusätzlichem MT2A mehr ihrer Höhe behielten, eine klarere innere Struktur aufwiesen und weniger Verlust wichtiger Matrixproteine zeigten als unbehandelte verletzte Scheiben. Auch Marker der Ferroptose waren reduziert, was die Idee stützt, dass MT2A die Bandscheibenpolster vor dem Zusammenbruch durch oxidativen und eisenbedingten Stress schützt.
Was das für die künftige Behandlung von Rückenschmerzen bedeutet
Insgesamt deuten die Ergebnisse darauf hin, dass MT2A nicht nur ein Begleitfaktor ist, sondern einen eingebauten Sicherheitsmechanismus darstellt, der hochfährt, wenn Bandscheiben zu versagen beginnen, und versucht, Zellen gegen schädliche eisengetriebene Oxidation zu verteidigen. Indem MT2A einen internen Überlebensweg aktiviert, begrenzt es eine bestimmte Form des Zelltods, bewahrt die Struktur der Bandscheibe und verlangsamt die Degeneration — zumindest in Tiermodellen und Zellkulturen. Für Patientinnen und Patienten weisen diese Befunde auf MT2A und seine Signalpartner als vielversprechende Ziele für Arzneimittel- oder gentherapieähnliche Ansätze hin, die darauf abzielen, Bandscheiben zu schützen oder zu regenerieren und langfristig mehr zu bieten als nur Schmerzlinderung und Operationen.
Zitation: Cai, H., Zheng, Hl., Chen, Qz. et al. The protective up-regulation of metallothionein-2A in intervertebral disc degeneration inhibits nucleus pulposus cell ferroptosis through activation of the PI3K/AKT/mTOR pathway. Cell Death Discov. 12, 111 (2026). https://doi.org/10.1038/s41420-026-02972-9
Schlüsselwörter: Rückenschmerzen, Bandscheibendegeneration, Ferroptose, Metallothionein-2A, PI3K AKT mTOR Signalweg