Clear Sky Science · de
Multi-Omics zeigt Heterogenität und funktionelle Populationen oligodendrozytärer Vorläuferzellen, induziert durch humane neurale Stammzellen
Warum der Schutz der Gehirnisolierung wichtig ist
Die Verschaltung unseres Gehirns hängt von einer fetthaltigen Schicht namens Myelin ab, die Nervenfasern wie Isolierung um elektrische Kabel umhüllt. Wenn Myelin beschädigt wird, wie bei Multipler Sklerose und anderen Erkrankungen, verlangsamen oder brechen Signale ab, was zu Problemen bei Bewegung, Sehen und Denken führt. Diese Studie untersucht eine spezielle Gruppe menschlicher Zellen, die Myelin wiederaufbauen können, und stellt eine praxisnahe Frage: Welche Zellen sind am besten für künftige Zelltherapien geeignet, um diese wichtige Isolierung zu reparieren?
Von Starterzellen des Gehirns zu Myelinbildnern
Die Forschenden starteten mit humanen neuralen Stammzellen – vielseitigen Ausgangszellen aus fetalem Hirngewebe, die bereits auf den Weg gebracht sind, zu Zellen des Nervensystems zu werden. Im Labor leiteten sie diese Stammzellen zur Differenzierung in oligodendrozytäre Vorläuferzellen (hOPCs) an, die direkte Vorläufer der myelinbildenden Zellen sind. Unter dem Mikroskop wandelten sich die Zellen von einfachen runden Formen zu komplexeren, verzweigten Gestalten und schalteten charakteristische Proteine ein, die Stadien auf dem Weg zu reifen, Myelin produzierenden Zellen anzeigen. Damit stand eine verlässliche, vergleichsweise sichere Quelle menschlicher Myelin-Bauvorläufer für detaillierte Analysen zur Verfügung.
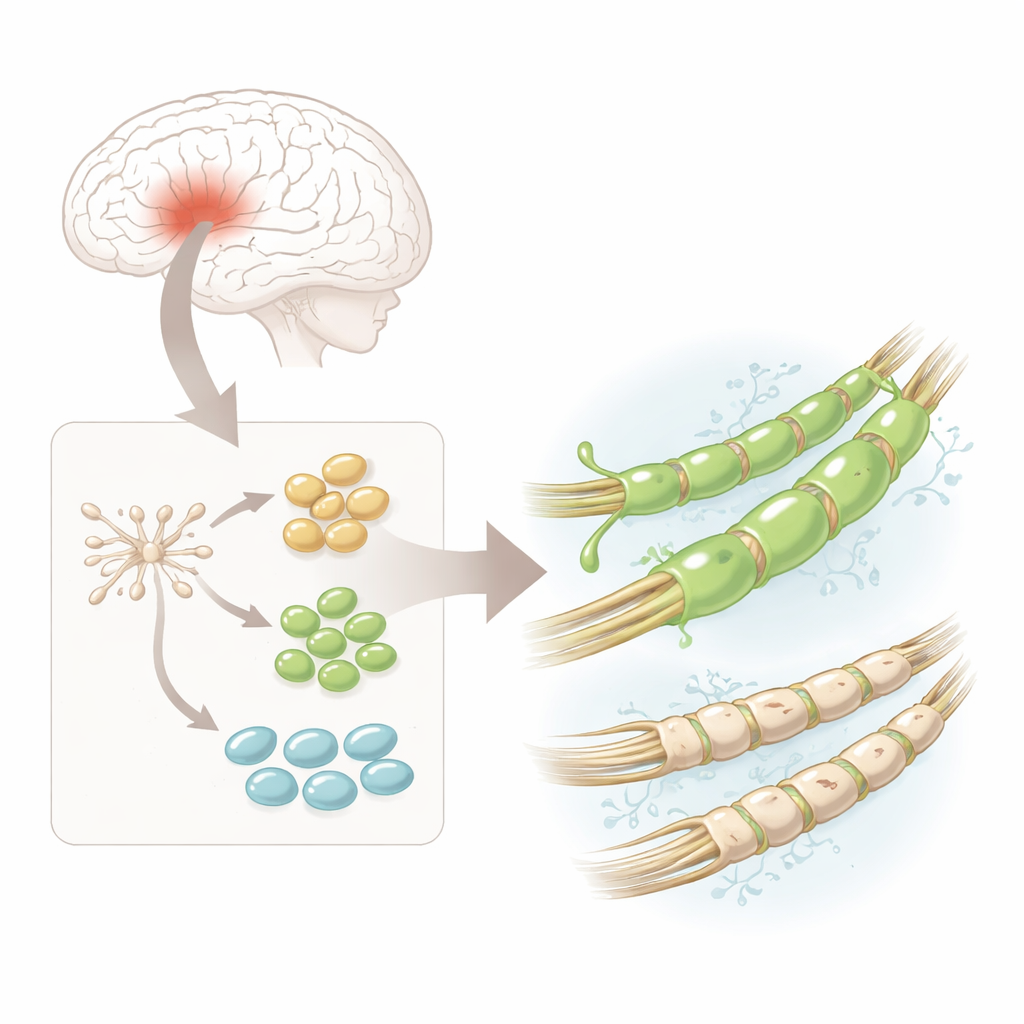
Ein Zelltyp, viele verborgene Varianten
Mithilfe der Einzelzell-RNA-Sequenzierung – einer Methode, die abliest, welche Gene in Tausenden einzelner Zellen aktiv sind – entdeckte das Team, dass die hOPCs nicht alle gleich waren. Stattdessen gruppierten sie sich in drei Hauptstadien: frühe „Pre-Progenitoren“, stärker verpflichtete Progenitoren und Zellen, die einer vollständigen oligodendrozytären Identität näher kamen. Über alle diese Stadien hinweg fiel ein Gen besonders auf: PDGFRA, das einen Rezeptor an der Zelloberfläche codiert. Eine hochempfindliche Bildgebungsmethode namens RNA-Scope bestätigte, dass die PDGFRA-mRNA und das Protein in jeder Phase häufiger vorhanden waren als andere Schlüsselmarker, was darauf hindeutet, dass dieser Rezeptor besonders leistungsfähige myelinbildende Zellen definieren könnte.
Die stärksten Reparaturzellen herausfiltern
Um diese Idee zu prüfen, teilten die Wissenschaftler die hOPCs in zwei Gruppen auf, je nachdem, ob sie den PDGFR-α-Rezeptor an ihrer Oberfläche trugen. Anschließend verglichen sie PDGFR-α–positive Zellen, PDGFR-α–negative Zellen und unsortierte Zellen in einer Reihe funktioneller Tests. Nach Transplantation in sogenannte „Shiverer“-Mäuse – die kein normales Myelin bilden können – erzeugten die PDGFR-α–positiven Zellen dichtere, kompaktere Myelinschichten um Nervenfasern als die anderen Gruppen. Diese Zellen wanderten zudem weiter und teilten sich in Labortests schneller. Anders gesagt: Die PDGFR-α–positive Population war am leistungsfähigsten darin, dorthin zu gelangen, wo sie gebraucht wurde, sich zu vermehren und Isolierung wiederaufzubauen.
Innere Signale, die Wachstum und Reparatur antreiben
Tiefergehend verglich das Team die Genaktivität zwischen PDGFR-α–positiven und -negativen Zellen. Sie fanden, dass in den positiven Zellen Netzwerke von Genen aktiviert waren, die am Wachstum glialer Zellen und an der Myelinbildung beteiligt sind, sowie mehrere zentrale Signalwege innerhalb der Zelle. Besonders zwei Pfade stachen hervor: PI3K–AKT–mTOR, das lange mit Zellwachstum und Myelinproduktion in Verbindung gebracht wird, und TGF-β-Signalgebung, die beeinflusst, wie junge Gehirnzellen ihre Schicksale wählen. Die Daten deuteten darauf hin, dass die Aktivierung von PDGFR-α in PI3K–AKT–mTOR einspeist, was wiederum TGF-β–bezogene Signale verstärkt und zusammen die Zellen in Richtung wirksamer Myelinbildner lenkt.
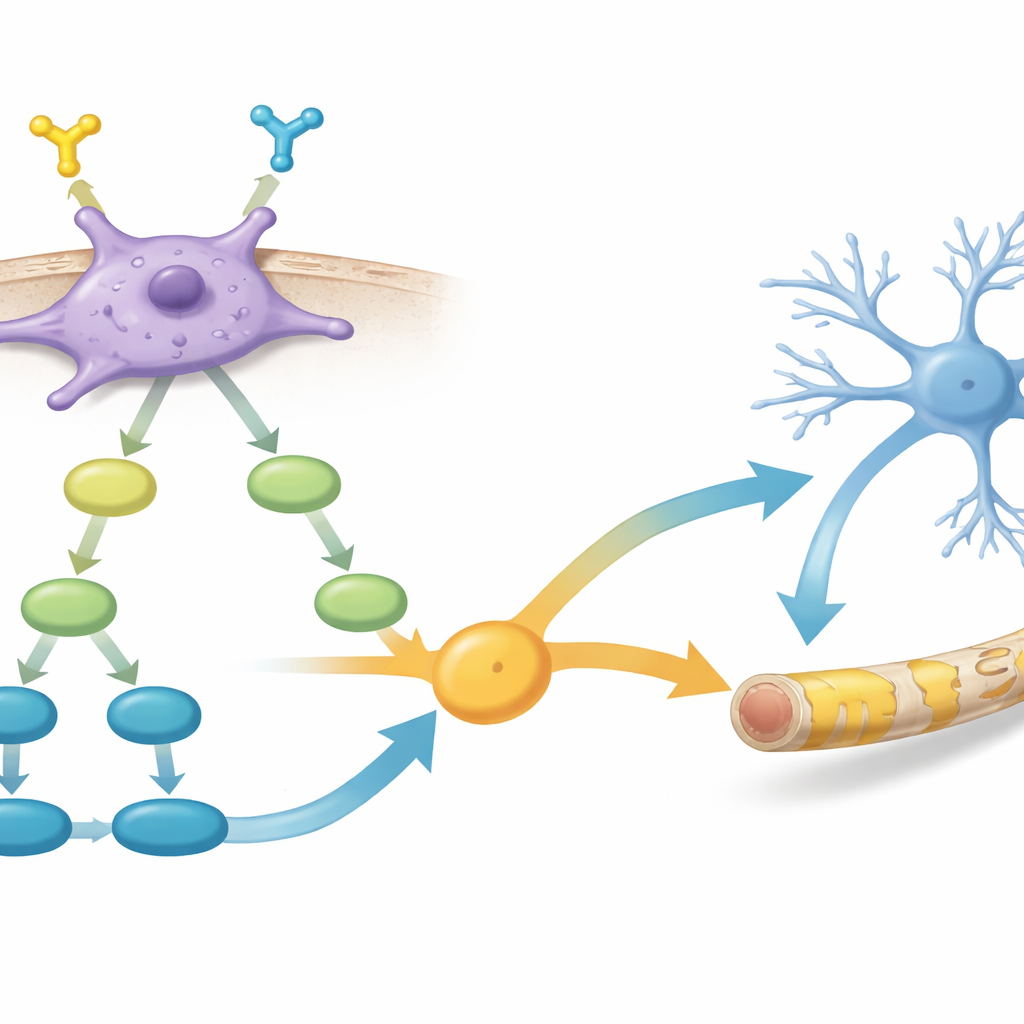
Myelinreparatur mit einem chemischen Helfer verstärken
Die Forschenden fragten dann, ob sich diese vielversprechenden Zellen weiter verbessern lassen. Sie behandelten PDGFR-α–positive hOPCs mit einem kleinen Molekül, das den TGF-β-Weg aktiviert, und untersuchten sowohl Genaktivität als auch Verhalten. Nach der Behandlung zeigten diese Zellen höhere Level mehrerer myelinbezogener Gene und erzeugten bei Transplantation in Shiverer-Mäuse dickere, vollständigere Myelinscheiden im Vergleich zu unbehandelten PDGFR-α–positiven Zellen. Dies stützt die Idee, dass das gezielte Abstimmen interner Signalwege in bereits gut ausgewählten Progenitorzellen deren Leistungsfähigkeit als lebende Werkzeuge zur Myelinreparatur weiter steigern kann.
Was das für künftige Therapien bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft: Nicht alle myelinbildenden Vorläuferzellen sind gleichwertig. Durch die Kombination leistungsstarker Genlese- und Bildgebungsinstrumente identifiziert diese Studie eine herausragende Untergruppe – PDGFR-α–positive hOPCs –, die besser migriert, sich stärker teilt und Myelin wirksamer wiederaufbaut als ihre Kolleginnen und Kollegen. Zudem werden interne Signalwege hervorgehoben, die chemisch angeregt werden können, um diese Zellen noch potenter zu machen. Zusammen liefern diese Erkenntnisse eine Roadmap zur Entwicklung sichererer, effizienterer Zelltherapien, um die Isolierung des Gehirns bei Erkrankungen mit Myelinverlust wiederherzustellen.
Zitation: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Schlüsselwörter: Myelin-Reparatur, oligodendrozytäre Vorläuferzellen, neurale Stammzellen, Zelltherapie, Einzelzell-RNA-Sequenzierung