Clear Sky Science · de
Axin1 stabilisiert S‑Opsin und erhält das Überleben von Zapfenphotorezeptoren durch Hemmung der GSK3β‑Aktivität
Unsere Farbsehfähigkeit erhalten
Jedes Mal, wenn wir ins Sonnenlicht treten oder auf einen hellen Bildschirm blicken, arbeiten winzige Zellen in unseren Augen fieberhaft daran, Licht in Sicht umzuwandeln. Diese Zellen, Photorezeptoren genannt, sind empfindlich und können bei vielen erblindenden Erkrankungen nach und nach zugrunde gehen. Diese Studie zeigt, wie ein wenig bekanntes „Organisations“protein, Axin1, Zapfenphotorezeptoren — die Zellen, die uns Tages‑ und Farbsehen ermöglichen — schützt, indem es wichtige lichtempfindliche Moleküle an ihrem Platz hält und gefährlichen Stress innerhalb der Zelle dämpft.
Wie Zapfen die Welt sehen
Unsere Netzhaut enthält zwei Haupttypen von Photorezeptoren: Stäbchen für schwaches, schwarz‑weißes Sehen und Zapfen für helles, farbiges Sehen. Zapfen tragen spezielle Pigmente, darunter S‑Opsin, das besonders empfindlich gegenüber kurzwelligem (blauem) Licht ist. Diese Pigmente befinden sich in einer schmalen, gestapelten Region an der Spitze jedes Photorezeptors, dem Außensegment, wo eintreffendes Licht in elektrische Signale umgewandelt wird. Da diese Region ständig dem Licht ausgesetzt ist und sich schnell erneuern muss, ist sie besonders anfällig für Schäden und für Stress in der Protein‑Faltungsfabrik der Zelle, dem endoplasmatischen Retikulum (ER). Wird das ER durch fehlgefaltete oder fehlplatzierte Proteine überlastet, kann es den Zelltod auslösen und so zur retinalen Degeneration und zum Sehverlust beitragen.
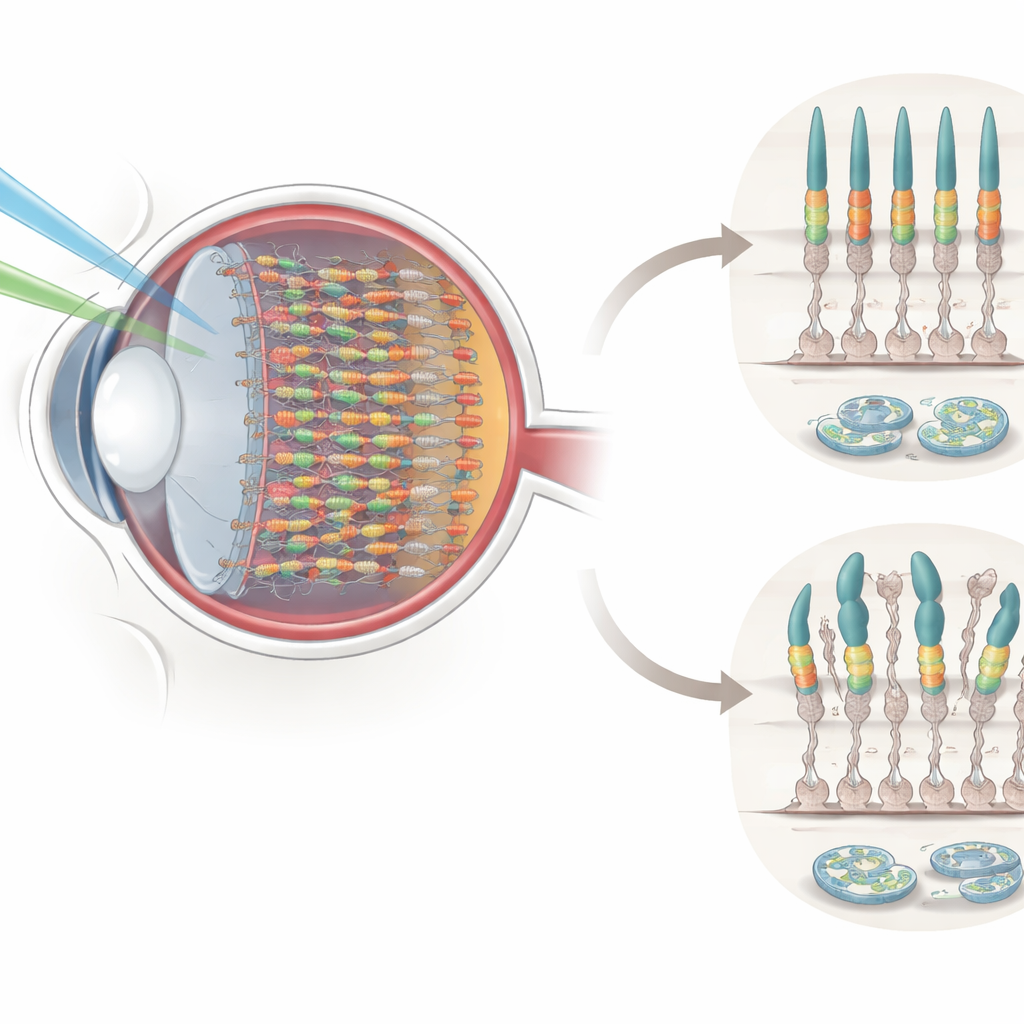
Ein verborgener Organisator in Zapfenzellen
Die Forschenden richteten ihre Aufmerksamkeit auf Axin1, ein Gerüstprotein, das vor allem dafür bekannt ist, Signalkaskaden in anderen Körperbereichen zu organisieren. Mittels hochauflösender Färbung in Mausnetzhäuten fanden sie heraus, dass Axin1 nicht gleichmäßig im Auge verteilt ist. Stattdessen ist es in Zapfenphotorezeptoren angereichert, insbesondere in der ventralen (unteren) Netzhaut, genau dort, wo S‑Opsin am häufigsten vorkommt. Innerhalb jedes Zapfens bildet Axin1 Cluster im Außensegment, die eng mit S‑Opsin überlappen. Im Verlauf der Entwicklung treten Axin1 und S‑Opsin gemeinsam auf und verschieben sich von kleinen Punkten zu länglichen, stabförmigen Strukturen, die reife Zapfenaußensegmente kennzeichnen. Dieses enge räumliche und zeitliche Zusammenspiel deutete darauf hin, dass Axin1 entscheidend dafür sein könnte, S‑Opsin richtig zu positionieren, damit Licht effizient detektiert werden kann.
Was geschieht, wenn Axin1 verloren geht
Um die Bedeutung von Axin1 zu testen, entfernten die Forschenden es gezielt aus Zapfenzellen von Mäusen mittels eines viralen Geneditierungsverfahrens. Diese Axin1‑defizienten Tiere zeigten verzögerte Pupillenverengung bei Blau‑ oder Grünlicht und verhielten sich in einem Licht‑Dunkel‑Präferenztest auffällig, was auf eine eingeschränkte Lichtwahrnehmung hindeutet. Unter dem Mikroskop wirkten ihre Zapfenaußensegmente unorganisiert: Die S‑Opsin‑Spiegel sanken und anstatt glatter, stabförmiger Strukturen zerfiel das Pigment in verstreute Punktstrukturen. Auch das umgebende Netzhautgewebe zeigte frühe Anzeichen von Störungen. Dichtungsstrukturen in der unterstützenden Pigmentschicht waren gestört, synaptische Marker zwischen Zapfen und nachgeschalteten Neuronen waren reduziert, und Gliazellen — normalerweise ruhende Stützzellen — wurden aktiviert, alles Kennzeichen einer fortschreitenden retinalen Degeneration.
Stress innerhalb der Zelle und ein gefährlicher Schalter
Das Fehlen von Axin1 veränderte nicht nur die Struktur; es verschärfte auch biochemischen Stress. In Mausnetzhäuten ohne Axin1 waren Marker für ER‑Stress, wie das Protein CHOP, in den Photorezeptorschichten stark erhöht. In kultivierten, zapfenabgeleiteten 661W‑Zellen machte das Herunterregulieren von Axin1 die Zellen gegenüber Blaulicht und dem chemischen ER‑Stressor Tunicamycin deutlich empfindlicher, was zu einer Hochregulierung von ER‑Stress‑Genen und einer erhöhten Zahl an Zellen mit Apoptose führte. Die Studie verknüpfte diese Verwundbarkeit mit einem Schlüsselenzym, GSK3β, das bei Abfall von Axin1‑Spiegeln aktiver wird. Hyperaktive GSK3β trieb die Zellen weiter in Richtung ER‑Stress und Zelltod. Umgekehrt reduzierten die Stabilisierung von Axin1 durch ein kleines Molekül oder die direkte Hemmung von GSK3β mit Lithiumchlorid Stressmarker, beruhigten die GSK3β‑Aktivität und retteten viele Zellen vor der Apoptose.
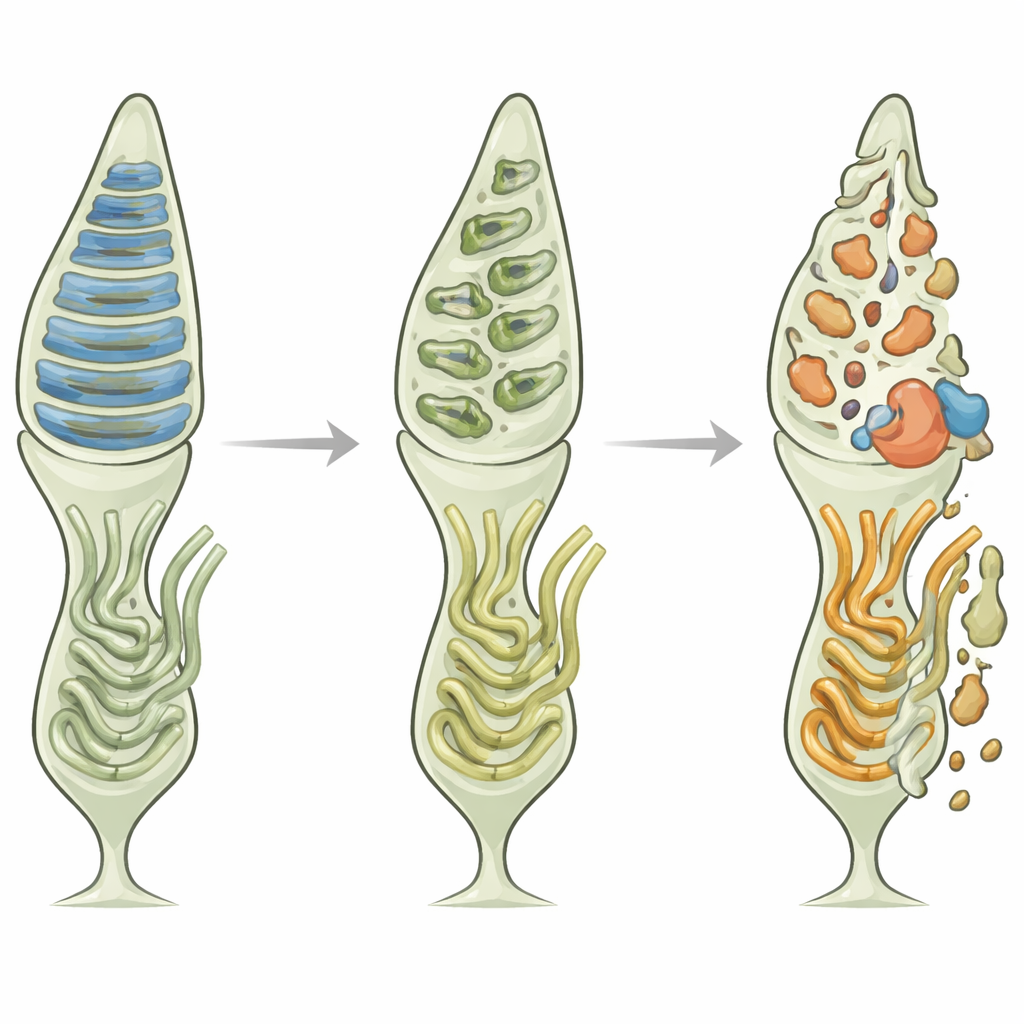
Schutz in Therapie übersetzen
In der Summe zeichnen die Befunde Axin1 als zentralen Wächter der Zapfenphotorezeptoren. Indem es S‑Opsin im Außensegment an seinem richtigen Platz verankert und das stressfördernde Enzym GSK3β in Schach hält, hilft Axin1 den Zapfen, der unablässigen Belastung durch helles und kurzwelliges Licht standzuhalten. Fehlt Axin1 oder ist es instabil, wird S‑Opsin fehl lokalisiert, das ER wird mit problematischen Proteinen überschwemmt, Stresswege schlagen an, und Zapfen werden in Richtung Degeneration gedrängt. Da viele beim Menschen auftretende erblindende Erkrankungen letztlich mit dem Verlust von Zapfen und ER‑Stress‑vermitteltem Zelltod einhergehen, könnten Strategien, die Axin1‑Funktion stärken oder nachahmen — oder GSK3β‑Aktivität sicher dämpfen — neue Wege eröffnen, die retinale Degeneration zu verlangsamen oder zu verhindern und unser Tages‑ und Farbsehen zu erhalten.
Zitation: Xu, J., Man, J., Fan, Y. et al. Axin1 stabilizes S-opsin and maintains cone photoreceptor survival by inhibiting GSK3β activity. Cell Death Discov. 12, 109 (2026). https://doi.org/10.1038/s41420-026-02968-5
Schlüsselwörter: retinale Degeneration, Zapfenphotorezeptoren, Endoplasmatisches Retikulum Stress, Axin1, GSK3 beta